Двойная связь это: ХиМиК.ru — Двойная связь — Большая Советская Энциклопедия
ХиМиК.ru — Двойная связь — Большая Советская Энциклопедия
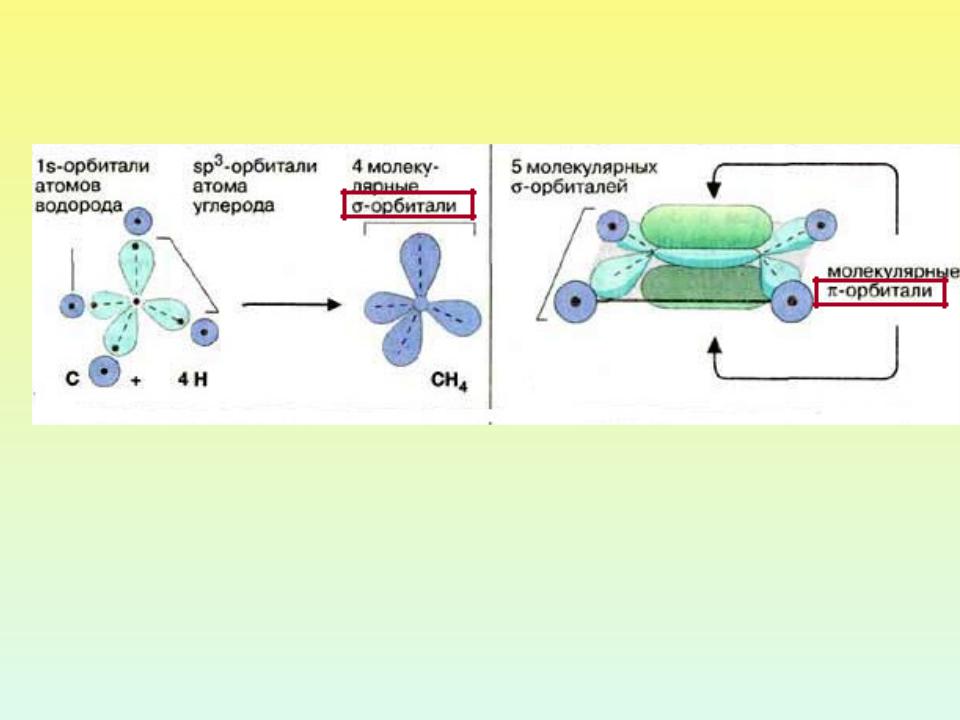
Двойная связь, ковалентная четырёхэлектронная связь между двумя соседними атомами в молекуле. Двойная связь обычно обозначается двумя валентными штрихами: >С=С<, >C=N —, >С=О, >C=S, — N=N —, — Н=О и др. При этом подразумевается, что одна пара электронов с sp2 или sp — гибридизованными орбиталями образует s-связь (см. рис. 1), электронная плотность которой сосредоточена вдоль межатомной оси; s-связь подобна простой связи. Другая пара электронов с р-орбиталями образует p-связь, электронная плотность которой сосредоточена вне межатомной оси. Если в образовании двойной связи принимают участие атомы IV или V группы периодической системы, то эти атомы и атомы, связанные с ними непосредственно, расположены в одной плоскости; валентные углы равны 120°. В случае несимметричных систем возможны искажения молекулярной структуры.
 Это облегчает понимание радикального и ионного механизмов реакций присоединения:
Это облегчает понимание радикального и ионного механизмов реакций присоединения:
В соединениях с двумя двойными связями, разделёнными одной простой связью, имеет место сопряжение p-связей и образование единого p-электронного облака, лабильность которого проявляется вдоль всей цепи (рис. 2, слева). Следствием такого сопряжения является способность к реакциям 1,4-присоединения:
Если три двойных связи сопряжены в шестичленном цикле, то секстет p-электронов становится общим для всего цикла и образуется относительно стабильная ароматическая система (см. рис. 2, справа). Присоединение к подобным соединениям как электрофильных, так и нуклеофильных реагентов энергетически затруднено. (См. также Химическая связь.)
Г. А. Сокольский.
Рис. 1. Схема двойной связи >С = С<
Рис. 2. Системы сопряжённых связей (вид сверху).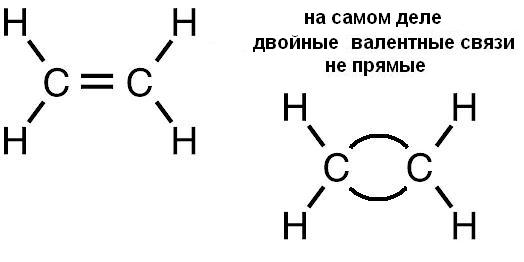
Двойная связь — это… Что такое Двойная связь?
- Двойная связь
-
ковалентная четырёхэлектронная связь между двумя соседними атомами в молекуле. Д. с. обычно обозначается двумя валентными штрихами: >С=СC=N —, >С=О, >C=S, — N=N —, — Н=О и др. При этом подразумевается, что одна пара электронов с sp2 или sp — гибридизованными орбиталями образует σ-связь (см. рис. 1), электронная плотность которой сосредоточена вдоль межатомной оси; σ-связь подобна простой связи. Другая пара электронов с
р-орбиталями образует π-связь, электронная плотность которой сосредоточена вне межатомной оси. Если в образовании Д. с. принимают участие атомы IV или V группы периодической системы, то эти атомы и атомы, связанные с ними непосредственно, расположены в одной плоскости; валентные углы равны 120°.
 В случае несимметричных систем возможны искажения молекулярной структуры. Д. с. короче простой связи и характеризуется высоким энергетическим барьером внутреннего вращения; поэтому положения заместителей при атомах, связанных Д. с., неэквивалентны, и это обусловливает явление геометрической изомерии (См. Изомерия). Соединения, содержащие Д. с., способны к реакциям присоединения. Если Д. с. электронно-симметрична, то реакции осуществляются как по радикальному (путем гомолиза π-связи), так и по ионному механизмам (вследствие поляризующего действия среды). Если электроотрицательности атомов, связанных Д. с., различны или если с ними связаны различные заместители, то π-связь сильно поляризована. Соединения, содержащие полярную Д. с., склонны к присоединению по ионному механизму: к электроноакцепторной Д. с. легко присоединяются нуклеофильные реагенты, а к электронодонорной Д. с. — электрофильные. Направление смещения электронов при поляризации Д. с. принято указывать стрелками в формулах, а образующиеся избыточные заряды — символами
В случае несимметричных систем возможны искажения молекулярной структуры. Д. с. короче простой связи и характеризуется высоким энергетическим барьером внутреннего вращения; поэтому положения заместителей при атомах, связанных Д. с., неэквивалентны, и это обусловливает явление геометрической изомерии (См. Изомерия). Соединения, содержащие Д. с., способны к реакциям присоединения. Если Д. с. электронно-симметрична, то реакции осуществляются как по радикальному (путем гомолиза π-связи), так и по ионному механизмам (вследствие поляризующего действия среды). Если электроотрицательности атомов, связанных Д. с., различны или если с ними связаны различные заместители, то π-связь сильно поляризована. Соединения, содержащие полярную Д. с., склонны к присоединению по ионному механизму: к электроноакцепторной Д. с. легко присоединяются нуклеофильные реагенты, а к электронодонорной Д. с. — электрофильные. Направление смещения электронов при поляризации Д. с. принято указывать стрелками в формулах, а образующиеся избыточные заряды — символами  Это облегчает понимание радикального и ионного механизмов реакций присоединения:
Это облегчает понимание радикального и ионного механизмов реакций присоединения:
В соединениях с двумя Д. с., разделёнными одной простой связью, имеет место сопряжение π-связей и образование единого π-электронного облака, лабильность которого проявляется вдоль всей цепи (рис. 2, слева). Следствием такого сопряжения является способность к реакциям 1,4-присоединения:
Если три Д. с. сопряжены в шестичленном цикле, то секстет π-электронов становится общим для всего цикла и образуется относительно стабильная ароматическая система (см. рис. 2, справа). Присоединение к подобным соединениям как электрофильных, так и нуклеофильных реагентов энергетически затруднено. (См. также Химическая связь.)Г. А. Сокольский.
Рис. 1. Схема двойной связи >С = СРис. 2. Системы сопряжённых связей (вид сверху).
Большая советская энциклопедия.
 — М.: Советская энциклопедия.
1969—1978.
— М.: Советская энциклопедия.
1969—1978.
- Двойная запись
- Двойная точка
Двойная связь — Двойная связь: Двойная связь химическая связь между двумя атомами, образованная двумя парами электронов; частный случай кратной связи. Двойная связь (или двойное послание) психологическая концепция в теории шизофрении Грегори Бейтсона … Википедия
ДВОЙНАЯ СВЯЗЬ — En.: Double bind Согласно Эриксону и Росси, двойная связь это предложение достаточно упрощенного и иллюзорного выбора (Erickson & Rossi, 1976, стр.62.): «Желаете ли вы испытать транс глубокий или средний?» Предлагается альтернатива, но результэт… … Новый гипноз: глоссарий, принципы и метод. Введение в эриксоновскую гипнотерапию
двойная связь — dvigubasis ryšys statusas T sritis chemija apibrėžtis Du kovalentiniai ryšiai tarp dviejų atomų.
 atitikmenys: angl. double bond; ethylene bond rus. двойная связь; этиленовая связь ryšiai: sinonimas – dvilypis ryšys sinonimas – etileninis ryšys … Chemijos terminų aiškinamasis žodynas
atitikmenys: angl. double bond; ethylene bond rus. двойная связь; этиленовая связь ryšiai: sinonimas – dvilypis ryšys sinonimas – etileninis ryšys … Chemijos terminų aiškinamasis žodynasдвойная связь — dvilypis ryšys statusas T sritis fizika atitikmenys: angl. double bond vok. Doppelbindung, f rus. двойная связь, f pranc. liaison double, f … Fizikos terminų žodynas
ДВОЙНАЯ СВЯЗЬ — хим. связь между соседними атомами в молекуле, осуществляемая двумя парами электронов. Характерна гл. обр. для органич. соединений. Графически изображается двумя валентными штрихами, например Соединения с Д. с. (см., напр., Этилен, Бутены,… … Большой энциклопедический политехнический словарь
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Химическая энциклопедия
ДВОЙНАЯ СВЯЗЬ — см. Кратные связи … Естествознание. Энциклопедический словарь
Двойная связь — Нарушения общения, наблюдающиеся в семьях больных шизофренией.

Двойная связь — нарушение в сфере коммуникации ребёнка и родителя, когда ребёнок получает от последнего противоречивые послания. Например, мать, не принимая своего нежного чувства к ребёнку, отталкивает ребёнка своей холодностью, а затем выражает показную любовь … Энциклопедический словарь по психологии и педагогике
Двойная связь (химия) — У этого термина существуют и другие значения, см. Двойная связь. Рис.1.Сигма связь … Википедия
Смотреть что такое «Двойная связь» в других словарях:
Впервые создан комплекс одновременно с одинарной, двойной и тройной связью металл-азот
Структура полученного комплексаИзображение: Evan P. Beaumier et al. / RSC / Chemical Science, 2016
Beaumier et al. / RSC / Chemical Science, 2016
Химики из Университета Мичигана впервые синтезировали комплекс, в котором центральный атом металла одновременно образует одинарные, двойную и тройную связи с атомами азота лигандов. Нитридо-имидо-амидный комплекс хрома был получен в двухстадийном синтезе и оказался янтарно-желтым кристаллическим соединением. Синтез необычного вещества приведен в Chemical Science, кратко о нем сообщает блог Королевского химического общества (Великобритания).
Порядок связи в химии — величина, определяющая какое количество электронов ответственно за образование этой связи. К примеру, обыкновенную, одинарную связь, образуют два электрона. Такой тип связи можно встретить, например, у молекулы водорода, H2. Двойная связь требует уже четырех электронов, такое наблюдается, к примеру в кислороде, O2. Тройные связи, требующие шесть электронов для «скрепления» двух атомов, встречаются в привычной нам молекуле азота, N2. Они делают ее необычайно прочной, но встречаются уже не так часто как одинарные и двойные. Порядки связи выше четвертого — большая редкость, встречающаяся, к примеру, в комплексах хрома, молибдена, вольфрама и урана (вплоть до шестого порядка).
Такой тип связи можно встретить, например, у молекулы водорода, H2. Двойная связь требует уже четырех электронов, такое наблюдается, к примеру в кислороде, O2. Тройные связи, требующие шесть электронов для «скрепления» двух атомов, встречаются в привычной нам молекуле азота, N2. Они делают ее необычайно прочной, но встречаются уже не так часто как одинарные и двойные. Порядки связи выше четвертого — большая редкость, встречающаяся, к примеру, в комплексах хрома, молибдена, вольфрама и урана (вплоть до шестого порядка).
То, какие именно связи образуются в молекуле, сильно влияет на ее свойства. Поэтому очень важно уметь предсказывать распределение электронов соответствующее наиболее устойчивым частицам. Для того, чтобы проверить и уточнить существующие теории, химики ищут частицы с исключительными свойствами, например необычным распределением связей. Впервые комплекс, в котором центральный атом образует сразу три связи разной кратности с атомами одного типа был синтезирован в 1978 году. Это было соединение вольфрама, содержавшее одинарную, двойную и тройную связи с атомами углерода.
Это было соединение вольфрама, содержавшее одинарную, двойную и тройную связи с атомами углерода.
Синтез промежуточного комплекса с одинарными и тройной связью
Изображение: Evan P. Beaumier et al. / RSC / Chemical Science, 2016
Изначально авторы новой работы планировали изучить свойства другого комплекса, в котором вокруг одного атома хрома присутствуют одна тройная связь с атомом азота и три обыкновенных. Целевое вещество, как предполагали химики, могло существовать в двух формах, «перебрасывая» электроны и атом водорода внутри молекулы — вторая форма содержала две двойные связи и две обыкновенные.
В качестве отправной точки к его синтезу ученые выбрали нитридо-комплекс хрома. В этом соединении присутствует тройная связь хром-азот, два амидных заместителя, связанных с атомом хрома одинарными связями и атом иода. На первой стадии авторы заместили атом иода на еще один амидный фрагмент (фениламидный). В результате образовался комплекс, в котором атом хрома окружен четырьмя атомами азота и двумя типами связей — тройной и одинарными. Спектроскопические исследования показали, что второй формы у этого комплекса нет.
На первой стадии авторы заместили атом иода на еще один амидный фрагмент (фениламидный). В результате образовался комплекс, в котором атом хрома окружен четырьмя атомами азота и двумя типами связей — тройной и одинарными. Спектроскопические исследования показали, что второй формы у этого комплекса нет.
Синтез комплекса с одинарной, двойной и тройной связью хром-азот
Изображение: Evan P. Beaumier et al. / RSC / Chemical Science, 2016
Однако интересный результат дало исследование его химических свойств. При обработке гидридом калия — чрезвычайно сильной щелочью — происходил отрыв атома водорода, располагавшегося на одном из трех амидных атомов азота. В результате этого, в молекуле, в которой все электроны уже были распределены, появилась еще одна «лишняя» пара электронов. Она и превратила одну из одинарных связей в двойную. Авторам удалось получить два соединения с таким строением — калиевую соль (темно-красная) и более сложную, в которой калий входит в состав криптанда — специальной органической «шубы» (янтарно-желтая). Последнюю удалось выделить в кристаллическом виде.
Она и превратила одну из одинарных связей в двойную. Авторам удалось получить два соединения с таким строением — калиевую соль (темно-красная) и более сложную, в которой калий входит в состав криптанда — специальной органической «шубы» (янтарно-желтая). Последнюю удалось выделить в кристаллическом виде.
Ранее химические журналы сообщали и о других синтезах веществ с необычными свойствами, к примеру, полностью неорганических ароматических анионов, самовоспроизводящихся ротаксанов, молекулярных насосов и других соединений, относящихся к химической экзотике.
Что такое двойная связь? — CodeRoad
Прежде чем ответить, нам нужно записать некоторые определения и понятия.
В контексте упомянутой статьи рассматриваются два понятия списка.
- Неизменяемый список, используемый в функциональных языках, таких как ML.

- Связанный список (mutable list), используемый в императивных языках, таких как C, C++, Java.
Кроме того, способы построения, уничтожения и использования списков различны.
Хотя каждый список должен быть построен, неизменяемый список строится только путем добавления новых элементов в начало списка, в то время как связанный список может быть построен путем добавления элементов в любое место списка, хотя обычно новые элементы добавляются в конец связанного списка.
Неизменяемый список пересекается только в одном направлении, вперед от головы к хвосту, в то время как связанный список может пересекаться как в прямом, так и в обратном направлении и даже может менять направление во время обхода.
Неизменяемый список не уничтожается с помощью операторов в исходном коде, а автоматически уничтожается с помощью сборки мусора, в то время как связанный список должен быть уничтожен с помощью оператора деструктора.
Кроме того, все неизменяемые списки имеют один и тот же тип, в то время как связанный список может содержать элементы различных типов.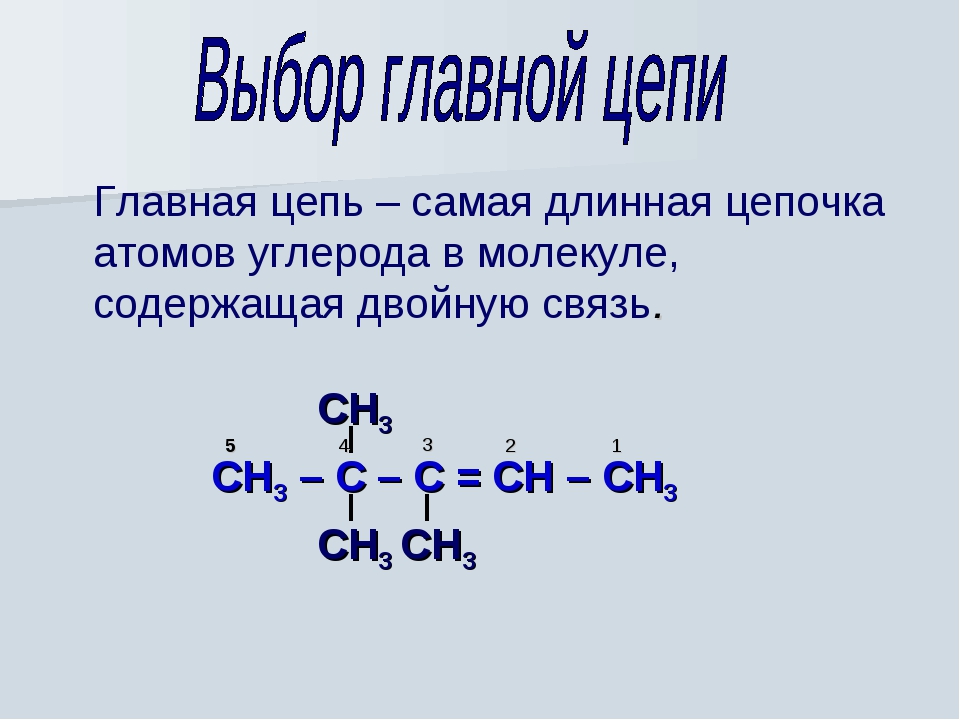
Из-за ограничений неизменяемого списка операция над любым элементом является O (1). Например, добавить элемент в список — Это O (1), потому что он всегда добавляется в заголовок. Использовать элемент в списке — Это O (1), потому что он является текущим заголовком списка. Это достигается тем, что при использовании списка на функциональном языке используется элемент head , а хвост списка передается так, что хвост передаваемого списка имеет новую головку, то есть для списка 1,2,3 мы используем головку списка 1, а затем передаем список 2,3 , где 2 -новая головка. Да, в концепции это два разных списка, но детали того, как это реализовано, — это другой вопрос.
Что автор имеет в виду, когда
говорит, что «double-links»? «double-links» имеет в виду двусвязный список , который является списком в языках, которые позволяют строить элементы в списке, чтобы иметь указатели как на предыдущий, так и на следующий элемент.

OP в комментариях тоже спрашивают:
Что именно в одинарном звене делает его более быстрым, чем двойное звено?
Как я уже отмечал в предыдущем разделе, Все операции над списком являются O(1).
Экзоциклическая двойная связь — Большая Энциклопедия Нефти и Газа, статья, страница 1
Экзоциклическая двойная связь
Cтраница 1
Экзоциклическая двойная связь — это связь, соединенная с атомом углерода кольца таким образом, как это показано в формуле внизу слева. Двойная связь в формуле справа является экзоциклической для кольца А и эидоциклической по отношению к кольцу В. Поскольку двойная связь экзоциклична к кольцу А, то к 215 нм нужно прибавить 5 24 29 нм, и тогда вычисленное положение максимума исходного соединения составит 244 нм. [1]
Каждая экзоциклическая двойная связь вызывает аналогичный батохромный эффект ( смещение на 5 тр. Аналогичным образом для соединения № 7 получаем: 217 [ 3X5 ] [ 2X5 ] 242 тр. В этих ( как и в других) случаях: вычисленные значения максимума достаточно близки к опытным данным, что подтверждает правила Вудварда.
[2]
Аналогичным образом для соединения № 7 получаем: 217 [ 3X5 ] [ 2X5 ] 242 тр. В этих ( как и в других) случаях: вычисленные значения максимума достаточно близки к опытным данным, что подтверждает правила Вудварда.
[2]
Радикальная атака экзоциклической двойной связи направлена преимущественно в / прайс-положение к изопропильной группе вследствие значительных размеров диэтоксифосфорильного радикала. [3]
Метод введения экзоциклических двойных связей с помощью реакции Виттига был также использован в химии стероидов. [4]
Селективное восстановление экзоциклической двойной связи может быть также осуществлено литием в диэтиламине; иллюстрацией может служить синтез а-амирина из глицирретовой кислоты, которая является производным ( 3-амирина известной конфигурации. [5]
Метод введения экзоциклических двойных связей с помощью реакции Витти га был также использован в химии стероидов. [6]
[6]
Селективное восстановление экзоциклической двойной связи может быть также осуществлено литием в диэтиламине; иллюстрацией может служить синтез а-амирина из глицирретовой кислоты, которая является производным р-амирина известной конфигурации. [7]
Реакция циклопропанирования протекает исключительно по экзоциклической двойной связи с образованием смеси син — и анти-изомеров. [8]
Стирол и аналогичные соединения с экзоциклической двойной связью функционируют как диены в результате участия в реакции одной из связей ароматического кольца. [9]
Как уже отмечалось выше, введение второй экзоциклической двойной связи к циклопропановому кольцу увеличивает энергию напряжения системы, хотя и не так значительно, как в случае введения первой двойной экзосвязи. [10]
[10]
Один из этих кетонов содержит в а-положении экзоциклическую двойную связь, второй является а р-ненасыщенным кетоном с двойной связью в цикле. Согласно правилам Вудворда, введение алкильного заместителя в а-положение к двойной связи вызывает батохромный сдвиг на 10 нм, который возрастает на 5 нм, если двойная связь является экзоциклической. Теоретическая разность для двух указанных соединений должна поэтому составлять 5 нм. Экспериментальная величина ( 3 нм) слишком мала и не позволяет сделать однозначного отнесения, но дает основание для предварительной идентификации соединения I как пинокарвона. Напротив, сравнение интенсквностей поглощения ( емакс) не оставляет никакого сомнения в выборе структуры. Действительно, известно, что переходы я — — л в s — чис-кетонах менее интенсивны, чем в s — грянс-кетонах. [11]
Можно предсказать, и это было подтверждено экспериментально, что в случае экзоциклической двойной связи будет происходить обратный процесс. Однако детальный анализ имеющихся теперь данных приводит к заключению, что этот эффект может быть много меньше, чем предполагалось до сих пор. [12]
Синтез этого соединения сравнительно прост; можно сделать замечания только относительно положения экзоциклической двойной связи. [13]
Ниже излагаются литературные данные о методах получения и свойствах циклопропановых углеводородов с экзоциклическими двойными связями. Многочисленные попытки синтеза метиленциклопропана или его производных основываются главным образом на введении двойной связи в трехчленный цикл, либо на замыкании в трехчленный цикл соединений с открытой цепью, имеющих этиленовую связь. Наиболее привычными методами получения метиленциклопропана являлись методы дегидратации различных циклопропилкарбинолов или элиминирования галогеноводорода из галогенгидринов этих спиртов. [14]
Хромофорная система а-дикетонов несколько напоминает систему гомоаннулярного диена с двумя заместителями и двумя экзоциклическими двойными связями; однако по сравнению с последней ( АмаксУ273 тр. [15]
Страницы: 1 2 3 4
Двойная связь — Double bond
Химическая связь с участием четырех связывающих электронов; имеет одну сигму плюс одну пи-облигацию
В химии двойная связь — это ковалентная связь между двумя атомами с участием четырех связывающих электронов, а не двух в одинарной связи . Двойные связи чаще всего возникают между двумя атомами углерода, например, в алкенах . Между двумя разными элементами существует множество двойных связей: например, в карбонильной группе между атомом углерода и атомом кислорода. Другие общие двойные связи обнаружены в азосоединениях (N = N), иминах (C = N) и сульфоксидах (S = O). В скелетной формуле двойная связь изображается как две параллельные линии (=) между двумя соединенными атомами; типографически для этого используется знак равенства . Двойные связи были впервые введены в химическую систему обозначений русским химиком Александром Бутлеровым .
Двойные связи с участием углерода прочнее и короче одинарных . Порядок облигаций — два. Двойные связи также богаты электронами, что делает их потенциально более реактивными в присутствии сильного акцептора электронов (как в реакциях присоединения галогенов).
- Химические соединения с двойными связями
-
Этилен углерод-углеродная двойная связь
-
Ацетон Двойная связь углерод-кислород
-
Диазен Азот-азотная двойная связь
Двойные связи в алкенах
Геометрия этиленаТип связывания можно объяснить с точки зрения орбитальной гибридизации . В этилене каждый атом углерода имеет три sp 2 -орбитали и одну p-орбиталь . Три орбитали sp 2 лежат в плоскости с углами ~ 120 °. Р-орбиталь перпендикулярна этой плоскости. Когда атомы углерода приближаются друг к другу, две орбитали sp 2 перекрываются, образуя сигма-связь . В то же время две p-орбитали сближаются (снова в одной плоскости) и вместе они образуют пи-связь . Для максимального перекрытия p-орбитали должны оставаться параллельными, и, следовательно, вращение вокруг центральной связи невозможно. Это свойство приводит к цис-транс-изомерии . Двойные связи короче одинарных, потому что перекрытие p-орбиталей максимально.
-
2 sp 2 орбитали (всего 3 таких орбитали) подходят для образования sp 2 -sp 2 sigma-связи
-
Две p-орбитали перекрываются, образуя пи-связь в плоскости, параллельной плоскости сигма.
При 133 пм длина связи С = С этилена короче, чем длина С-С в этане с 154 пм. Двойная связь также сильнее, 636 кДж моль -1 по сравнению с 368 кДж моль -1, но не вдвое больше, поскольку пи-связь слабее сигма-связи из-за менее эффективного пи-перекрытия.
В альтернативном представлении двойная связь возникает в результате двух перекрывающихся sp 3 -орбиталей, как в изогнутой связи .
Вариации
В молекулах с чередующимися двойными связями и одинарными связями перекрытие p-орбиталей может существовать над несколькими атомами в цепи, что приводит к возникновению сопряженной системы . Конъюгацию можно найти в таких системах, как диены и еноны . В циклических молекулах конъюгация может приводить к ароматичности . В кумуленах две двойные связи смежны.
Двойные связи характерны для элементов 2 периода, углерода , азота и кислорода , и менее распространены для элементов более высоких периодов . Металлы также могут участвовать в множественной связи в множественной связи металлического лиганда .
Гомологи алкена 14 группы
Соединения с двойной связью, гомологи алкена , R 2 E = ER 2 теперь известны для всех более тяжелых элементов группы 14 . В отличие от алкенов эти соединения не плоские, а имеют скрученную и / или трансбентную структуру. Эти эффекты становятся более выраженными для более тяжелых элементов. Дистаннен (Me 3 Si) 2 CHSn = SnCH (SiMe 3 ) 2 имеет длину связи олово-олово немного короче, чем одинарная связь, прозрачную структуру с пирамидальной координацией у каждого атома олова и легко диссоциирует в растворе до форма (Me 3 Si) 2 CHSn: (станнандиил, аналог карбена). Связь включает две слабые донорно-акцепторные связи, неподеленная пара на каждом атоме олова перекрывается с пустой p-орбиталью на другом. Напротив, в дисиленах каждый атом кремния имеет плоскую координацию, но заместители скручены, так что молекула в целом не является плоской. В диплумбенах длина связи Pb = Pb может быть больше, чем у многих соответствующих одинарных связей. Плюмбены и станнены обычно диссоциируют в растворе на мономеры с энтальпиями связи, которые составляют лишь часть соответствующих одинарных связей. Некоторые плюмбены и станнены с двойными связями аналогичны по прочности водородным связям. Модель Картера-Годдарда-Мальье-Тринкье может быть использована для предсказания природы связи.
Типы двойных связей между атомами
Рекомендации
- Пюкко, Пекка; Ридель, Себастьян; Пацшке, Майкл (2005). «Ковалентные радиусы с тройной связью». Химия: Европейский журнал . 11 (12): 3511–20. DOI : 10.1002 / chem.200401299 . PMID 15832398 .
Урок 3. непредельные углеводороды – алкены — Химия — 10 класс
Химия, 10 класс
Урок № 3 Непредельные углеводороды – алкены
Перечень вопросов, рассматриваемых в теме
Урок посвящён непредельным углеводородам, их номенклатуре, физическим и химическим свойствам, а также роли в жизни человека. В ходе урока учащиеся познакомятся с представителями данного класса органических веществ.
Глоссарий
Алкены – непредельные углеводороды ряда этилена, имеющие одну двойную углерод-углеродную связь
Гибридизация – процесс взаимодействия разных, но близких по энергии электронных орбиталей, приводящий к их выравниванию по форме и энергии.
Гомология – явление сходства по составу, строению, химическим свойствам и принадлежности к тому же классу одного вещества с другим веществом, но различающиеся дуг от друга на одну или несколько групп СН2. Группу СН2 называют гомологической разностью.
Горение – быстро протекающий процесс окисления вещества, сопровождающийся большим выделением тепла и ярким свечением.
Полимеризация – реакция, при которой одинаковые молекулы соединяются между собой в более крупную молекулу
Изомерия – явление существования веществ, одинаковых по составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и вследствие этого по физическим и химическим свойствам. Такие вещества называются изомерами.
Формула структурная – изображение молекулы, в котором показан порядок связывания атомов между собой. Химические связи в таких формулах обозначаются черточками.
Основная литература: Рудзитис, Г. Е., Фельдман, Ф. Г. Химия. 10 класс. Базовый уровень; учебник/ Г. Е. Рудзитис, Ф. Г, Фельдман – М.: Просвещение, 2018. – 224 с.
Дополнительная литература:
1. Рябов, М.А. Сборник задач, упражнений и тестов по химии. К учебникам Г.Е. Рудзитис, Ф.Г. Фельдман «Химия. 10 класс» и «Химия. 11 класс»: учебное пособие / М.А. Рябов. – М.: Экзамен. – 2013. – 256 с.
2. Рудзитис, Г.Е. Химия. 10 класс : учебное пособие для общеобразовательных организаций. Углублённый уровень / Г.Е. Рудзитис, Ф.Г. Фельдман. – М. : Просвещение. – 2018. – 352 с.
Открытые электронные ресурсы:
Единое окно доступа к информационным ресурсам [Электронный ресурс]. М. 2005 – 2018. URL: http://window.edu.ru/ (дата обращения: 01.06.2018).
ТЕОРЕТИЧЕСКИЙ МАТЕРИАЛ ДЛЯ САМОСТОЯТЕЛЬНОГО ИЗУЧЕНИЯ
Алкены – непредельные углеводороды, в молекулах которых между атомами углерода имеется одна двойная углерод-углеродная связь. Общая формула алкенов СnH2n, где n≥2.
Простейшим представителем алкенов является этен, или этилен С2Н4.
Структурная формула этилена:
(сокращенная: СН2=СН2).
Особенности пространственного и электронного строения алкенов на примере молекулы этилена
Рассмотрим особенности электронного и пространственного строения алкенов на примере молекулы этилена. Все атомы углерода в молекуле этилена находятся в состоянии sp2-гибридизации. Три гибридных орбитали участвуют в образовании трех достаточно прочных сигма связей (по две связи у каждого атома углерода с атомами водорода и одна общая между собой). Оставшаяся негибридная р-орбиталь образует менее прочную пи-связь между атомами углерода. Таким образом, в молекуле этилена присутствуют 5 сигма-связей и одна пи-связь, причем двойная связь между атомами углерода образована одной сигма и и одно пи-связями. Наличие пи-связей в молекулах алкенов делает невозможным вращение атомов углерода друг относительно друга (имеются ввиду те атомы, при которых находится двойная связь)
Каждый атом углерода в молекуле этилена имеет треугольное строение.
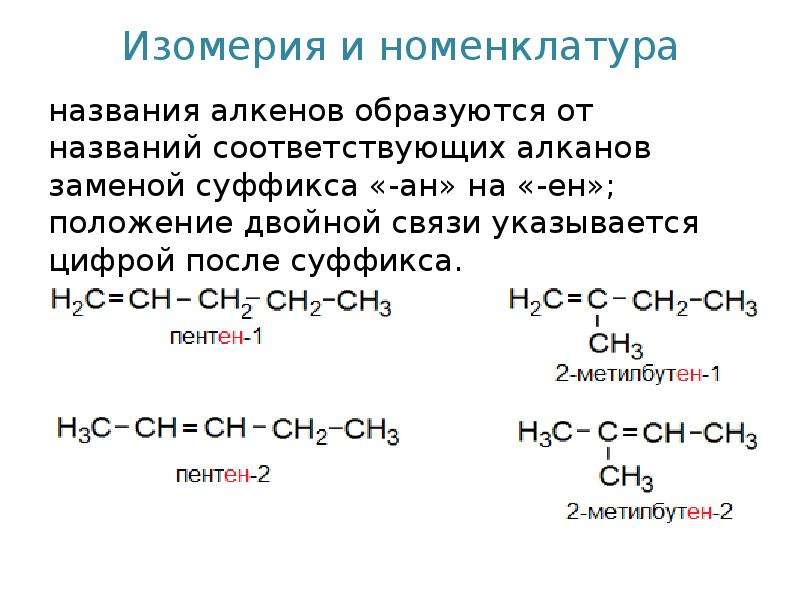
Номенклатура алкенов
Особенности номенклатуры алкенов заключаются в следующем:
1. Нумерация углеродной цепи начинается с того конца, где ближе расположена двойная связь
2. В конце названия изменяется суффикс -ан соответствующего предельного углеводорода на -ен или -илен, и, если это необходимо, указывается атом углерода, при котором находится двойная связь
Рассмотрим пример:
1. Нумерация главной цепи начинается слева направо, так как двойная связь ближе к левой части молекулы.
2. Называем радикал, расположенный у второго атома углерода: 2-метил
3. В главной цепи находится четыре атома углерода, следовательно, она соответствует предельному углеводороду – бутану.
4. Так как присутствует двойная связь, то суффикс – ан меняется на суффикс -ен и указывается положение двойной связи: бутен-1.
5. Соединяем суффикc с корнем и получаем название 2-матилбутен-1.
Гомология алкенов и изомерия алкенов.
Ближайшие гомологи этилена:
С3Н6 пропен (пропилен)
С4Н8 бутен (бутилен)
С5Н10 пентен (амилен)
Для алкенов характерны следующие виды изомерии:
1. Изомерия углеродного скелета
2. Изомерия положения кратной связи
3. Пространственная геометрическая изомерия
4. Межклассовая (с циклоалканами)
Рассмотрим каждый вид изомерии на примере вещества состава С4Н8:
При построении структурной формулы данного вещества возможно расположение двойной связи как между первым и вторым атомами углерода, так и между вторым и третьим, тогда возможно получить две структурные формулы
Данный вид изомерии называется изомерией положения кратных связей.
Для данного вещества возможно построить единственный разветвлённый изомер – изомер углеродного скелета – 2-метилпропен:
Межклассовый изомер бутена – циклобутан:
Также для бутена-2 возможно существование геометрических изомеров, это связано с тем, что метильная группа СН3— может располагаться относительно плоскости двойной связи в двух разных положениях, что приводит к образованию цис- (если эти группы расположены по одну линию связи) и транс-изомеров (если метильные группы расположены по разные линии связи):
Физические свойства алкенов
Этилен – бесцветный газ, почти без запаха, легче воздуха, плохо растворим в воде. Пропен и бутен – также газы. От пентена до октадецена – жидкости. Остальные – твердые вещества. Все агрегатные состояния указаны при нормальных условиях.
Способы получения алкенов
1. Внутримолекулярная дегидратация спиртов:
Данный способ является основным способом получения этилена в лабораторных условиях. Реакция протекает при температуре выше 140 градусов и в присутствии концентрированной серной кислоты, выполняющей роль катализатора. При дегидратации этанола получают этилен, а при дегидратации пропанола – пропилен:
2. Дегидрирование предельных углеводородов.
Данная реакция протекает при нагревании в присутствии катализаторов: никеля, платины, оксида хрома (III). При этом получают соответствующие алкены:
Химические свойства алкенов
Химические свойства алкенов обусловлены наличием в их молекулах двойных углерод-углеродных связей. Дело в том, что пи-связь, как было сказано ранее, является менее устойчивой, чем сигма связь. Поэтому при атаке её каким-либо реагентом она легко разрывается. Это объясняет основные химические свойства алкенов: они способны вступать в реакции присоединения и окисления.
Реакции присоединения
Гидрирование – присоединение водорода | Протекает при нагревании в присутствии катализаторов: платина, никель, оксид хрома (III). Продуктом реакции всегда является алкан. | |
Галогенирование – присоединение галогенов | Реакция протекает при обычных условиях. Продукт реакции – дигалогеналкан (1,2 — дибромэтан) | Признак реакции – обесцвечивание раствора брома, поэтому данную реакцию используют как качественную на двойную связь. |
Гидрогалогенирование – присоединение галогенводородов | Продукт реакции – галогеналкан (хлорэтан) | |
Гидратация – присоединение воды | Продукт реакции — спирт |
Реакция полимеризации
Полимеризация – реакция, при которой одинаковые молекулы соединяются в более крупные молекулы. | Условия реакции – высокая температура и давление Продукт реакции – полимер (полиэтилен) | Продукты реакции полимеризации используются для производства пластмасс и синтетических волокон |
Окисление
«Мягкое» — реакция Вагнера: взаимодействие с водным раствором перманганата калия | Продукт реакции – многоатомный спирт (этиленгликоль) | Признак реакции – обесцвечивание раствора перманганата калия , поэтому данную реакцию используют как качественную на двойную связь. |
Каталитическое – окисление кислородом в присутствии катализаторов | Продукт реакции – оксид алкена (оксид этилена) | |
Горение | Продуктами полного горения алкенов являются углекислый газ и вода |
Особенности реакций гидрогалогенирования и гидратации у пропилена и других гомологов этилена
Реакции присоединения галогеналканов и воды у гомологов этилена протекают по правилу Марковникова: водород присоединяется по месту разрыва двойной связи к более гидрированному атому углерода. Например, при присоединении хлороводорода к молекуле пропилена, образуется не 1-хлорпропан, а 2-хлорпропан:
Аналогично протекает реакция гидратации:
Применение этилена и его соединений
Производство пластмасс, взрывчатых веществ, антифриза, растворителей, синтетического каучука, ацетальдегида, для ускорения созревания плодов.
ПРИМЕРЫ И РАЗБОР РЕШЕНИЯ ЗАДАНИЙ ТРЕНИРОВОЧНОГО МОДУЛЯ
- Решение задачи на нахождение массы раствора.
Масса 2%-го раствора бромной воды, которая вступает в реакцию с 2,24 л пропилена равна
Шаг первый: Составляем уравнение химической реакции С2Н4 + Br2 = C2H4Br2
Шаг второй: Находим количество вещества пропилена по формуле n=V\Vm= 2,24 л / 22,4 л/моль = 0,1 моль
Шаг третий: По уравнению реакции количество вещества пропилена равно количеству вещества брома: n(С2Н4)=n(Br2)=0,1 моль
Шаг четвёртый: Находим массу брома по формуле: m=Mn=160 г/моль*0,1 моль= 16 г
Шаг пятый: Находим массу раствора бромной воды по формуле: m (раствора)=m/ω = 16г / 0,02 = 800г
- Решение упражнения на химические свойства алкенов
Вставьте в таблицу пропущенные продукты реакции
H2 | Br2 | H2O | HCl | |
этилен | ||||
пропилен |
Варианты ответов: этан, пропан, бутан, 1,2-дибромэтан, 1,2-дибромпропан, 1,3-дибромпропан, этанол, пропанол-1, пропанол-2, хлорэтан, 1-хлорпропан, 2-хлорпропан.
Решение:
Первый шаг: При гидрировании алкенов водородом образуются предельные углеводороды – алканы с соответствующим числом атомов углерода. Поэтому первая колонка заполняется продуктами реакции – этан и пропан:
Второй шаг: При галогенировании алкенов галогены, в данном случае бром, присоединяются по месту разрыва двойной связи, образуя дигалогенпроизводные, например:
Поэтому второй столбец заполняется следующими веществами: 1,2-дибромэтан, 1,2-дибромпропан.
Третий шаг: При гидратации (присоединении воды) образуются спирты. При реакции пропилена с водой важно помнить о правиле Марковникова, поэтому продуктами реакции будут этанол и пропанол-2:
4. При гидрогалогенировании алкенов продуктом реакции будут галогеналканы. И опять нужно помнить о правиле Марковникова для гидрогалогенирования пропилена:
Поэтому правильный ответ в этом задании: хлорэтан и 2-хлорпропан
|
КОВАЛЕНТНАЯ СВЯЗЬ — ДВОЙНАЯ ОБЛИГАЦИЯ На этой странице объясняется, как возникают двойные ковалентные связи. Он начинается с простой картины двойной ковалентной связи, а затем представляет собой более сложный взгляд на связь в этене. | |
|
Внимание! На этой странице предполагается, что вы уже читали страницу об одинарных ковалентных связях. Если вы попали прямо на эту страницу через поисковую систему, перейдите по этой ссылке, прежде чем продолжить. | |
|
Простой вид двойных ковалентных связей Двойная ковалентная связь — это когда две пары электронов разделяются между атомами, а не только одна пара. Некоторые простые молекулы, содержащие двойные связи Кислород, O 2 Два атома кислорода могут образовывать стабильную структуру, разделяя две пары электронов, как показано на диаграмме.
Двойная связь условно показана двумя линиями, соединяющими атомы. Каждая линия представляет одну пару общих электронов. Двуокись углерода, CO 2
Ethene, C 2 H 4 Этен имеет двойную связь между двумя атомами углерода.
Более сложный вид связи в этене Важно изучить связь в этене более подробно, потому что она оказывает прямое влияние на его химический состав.Если вы не понимаете истинную природу двойной связи, вы не сможете понять, как ведет себя этен. Орбитальный вид соединения в этене Этен состоит из атомов водорода (1s 1 ) и атомов углерода (1s 2 2s 2 2p x 1 2p y 1 ). Продвижение электрона У атома углерода недостаточно неспаренных электронов для образования необходимого количества связей, поэтому ему необходимо продвинуть одну из пар 2s 2 на пустую орбиталь 2p z .Это в точности то же самое, что и всякий раз, когда углерод образует связи — независимо от того, к чему еще он присоединяется. Атом углерода сейчас находится в возбужденном состоянии .
Гибридизация В случае этена есть отличие от метана, потому что каждый углерод присоединяется только к трем другим атомам, а не к четырем. Когда атомы углерода гибридизуют свои внешние орбитали перед образованием связей, на этот раз они гибридизуют только три и орбиталей, а не все четыре.Они используют 2s-электрон и два 2p-электрона, но оставляют другой 2p-электрон без изменений.
| |
|
Примечание: Вы можете задаться вопросом, почему он решил гибридизовать эти три орбитали, а не просто использовать три p-орбитали, которые уже имеют одинаковую энергию. Это потому, что он сначала использует орбитали с наименьшей энергией. | |
|
Образованные новые орбитали называются sp 2 гибридов , потому что они образованы s-орбиталью и двумя p-орбиталями, реорганизуясь сами.Орбитали sp 2 выглядят скорее как орбитали sp 3 , которые мы обсуждали при связывании в метане на странице одинарных связей, за исключением того, что они короче и толще. Три гибридных орбитали sp 2 располагаются как можно дальше друг от друга — под углом 120 ° друг к другу в плоскости. Оставшаяся p-орбиталь расположена под прямым углом к ним. Два атома углерода и четыре атома водорода до соединения выглядели бы так:
Различные атомные орбитали, направленные друг к другу, теперь сливаются, образуя молекулярные орбитали, каждая из которых содержит пару связывающих электронов.Молекулярные орбитали, образованные сквозным перекрытием атомных орбиталей, называются сигма-связями . Орбитали p на каждом атоме углерода не направлены друг к другу, поэтому мы оставим их на мгновение. На схеме черные точки представляют ядра атомов. Обратите внимание, что p-орбитали настолько близки, что перекрываются боками. Это боковое перекрытие также создает молекулярную орбиталь, но другого типа. В этом электроны удерживаются не на линии между двумя ядрами, а над и под плоскостью молекулы.Образованная таким образом облигация называется облигацией пи. Для ясности сигма-связи показаны линиями, каждая из которых представляет одну пару общих электронов. Различные виды линий показывают направления, в которых указывают связи. Обычная линия представляет собой связь в плоскости экрана (или бумаги, если вы ее распечатали), пунктирная линия — это связь, уходящая от вас, и клин показывает выходящую к вам связь. | |
|
Примечание: Действительно интересной связью в этене является связь пи.Почти во всех случаях, когда вы рисуете структуру этена, сигма-связи будут показаны линиями. | |
|
Четко объясните, что такое пи-связь. Это область пространства, в которой вы можете найти два электрона, образующих связь. Эти два электрона могут жить где угодно в этом пространстве. Было бы ошибкой думать, что один живет наверху, а другой внизу. | |
|
Продолжая химию: Это хороший пример любопытного поведения электронов.Как электроны попадают от одной половины пи-связи к другой, если их никогда не найти между ними? На этот вопрос невозможно ответить, если вы думаете об электронах как о частицах. Если вы хотите проследить это, вам придется прочитать несколько довольно важных материалов о волновой природе электронов. | |
|
Даже если ваш учебный план не предполагает, что вы знаете, как формируется пи-связь, вы должны знать, что он существует. Связь пи доминирует в химии этена.Он очень уязвим для атаки — очень отрицательная область пространства выше и ниже плоскости молекулы. Это также несколько далеки от контроля ядер, и поэтому связь более слабая, чем сигма-связь, соединяющая два атома углерода. | |
|
Важно! Проверьте свой учебный план! Узнайте, действительно ли вам нужно знать, как образуется пи-связь. Не забудьте заглянуть под этен, а также в связующий раздел вашего учебного плана. Если вам это не нужно знать, нет смысла учить это! Однако вам необходимо знать, что существует пи-связь — что две связи между атомами углерода в этене не одинаковы. Если вы работаете по учебной программе для Великобритании, но у вас нет ее копии, узнайте, как ее загрузить. | |
|
Все двойные связи (какие бы атомы они ни соединяли) будут состоять из сигма-связи и пи-связи. Этот орбитальный взгляд на двойную связь действительно важен на этом уровне только в отношении органических соединений. Если вы хотите узнать больше об этом, перейдите по первой ссылке ниже, которая приведет вас к меню с разделом, посвященным органическому склеиванию.Вы найдете повторение описания этена, но также найдете информацию о связи в бензоле и двойной связи углерод-кислород.
© Джим Кларк 2000 (изменено в сентябре 2012 г.) |
|
Двойные и тройные ковалентные облигации
Цель обучения
- Опишите типы перекрытия орбиталей, которые возникают в одинарных, двойных и тройных связях
Ключевые моменты
- Двойные и тройные ковалентные связи сильнее одинарных ковалентных связей, и для них характерно разделение четырех или шести электронов между атомами, соответственно.
- Двойные и тройные связи состоят из сигма-связей между гибридизированными орбиталями и пи-связей между негибридизированными p-орбиталями. Двойные и тройные связи придают соединениям дополнительную стабильность и ограничивают любое вращение вокруг оси связи.
- Длины связей между атомами с кратными связями короче, чем между атомами с одинарными связями.
Условия
- прочность связи Непосредственно связана с количеством энергии, необходимой для разрыва связи между двумя атомами.Считается, что чем больше энергии требуется, тем прочнее связь. Длина связи
- Расстояние между ядрами двух связанных атомов. Это можно определить экспериментально.
- орбитальная гибридизация: концепция смешения атомных орбиталей для образования новых гибридных орбиталей, подходящих для качественного описания свойств и геометрии атомных связей.
- атомных орбиталей — физическая область в пространстве вокруг ядра, в которой, вероятно, находится электрон.
Двойные и тройные ковалентные связи
Ковалентная связь возникает, когда электроны разделяются между атомами.Двойные и тройные ковалентные связи возникают, когда четыре или шесть электронов разделяются между двумя атомами, и они обозначены в структурах Льюиса двумя или тремя линиями, соединяющими один атом с другим. Важно отметить, что только атомы, которым необходимо получить или потерять как минимум два валентных электрона в результате обмена, могут участвовать в нескольких связях.
Связующие концепции
Гибридизация
Двойные и тройные связи можно объяснить орбитальной гибридизацией или «смешиванием» атомных орбиталей с образованием новых гибридных орбиталей.Гибридизация описывает ситуацию связывания с точки зрения конкретного атома. Комбинация s- и p-орбиталей приводит к образованию гибридных орбиталей. Вновь образованные гибридные орбитали имеют одинаковую энергию и определенное геометрическое расположение в пространстве, которое согласуется с наблюдаемой геометрией связи в молекулах. Гибридные орбитали обозначаются как sp x , где s и p обозначают орбитали, используемые для процесса смешивания, а значение верхнего индекса x находится в диапазоне от 1 до 3, в зависимости от того, сколько p орбиталей требуется для объяснения наблюдаемой связи.
Гибридные орбитали Схема результирующей ориентации в пространстве sp 3 гибридных орбиталей. Обратите внимание, что сумма верхних индексов (1 для s и 3 для p) дает общее количество сформированных гибридных орбиталей. В этом случае образуются четыре орбитали, которые указывают в направлении вершин тетраэдра.Пи-облигации
Pi, или [латекс] \ pi [/ латекс], связи возникают, когда существует перекрытие между негибридизованными p-орбиталями двух соседних атомов. Между ядрами атомов не происходит перекрытия, и это ключевое различие между сигма- и пи-связями.Для эффективного образования связи между негибридизованными p-орбиталями должно быть правильное геометрическое соотношение: они должны находиться в одной плоскости.
Образование связи Pi Перекрытие между соседними негибридизованными p-орбиталями дает пи-связь. Электронная плотность, соответствующая общим электронам, не сосредоточена вдоль межъядерной оси (то есть между двумя атомами), в отличие от сигма-связей.Множественные связи между атомами всегда состоят из сигма-связи, а любые дополнительные связи относятся к типу π.
Примеры Пи-облигаций
Простейшим примером органического соединения с двойной связью является этилен или этен, C 2 H 4 . Двойная связь между двумя атомами углерода состоит из сигма-связи и π-связи.
Этиленовая связь Пример простой молекулы с двойной связью между атомами углерода. Указаны длины связей и углы (указывающие на геометрию молекулы).С точки зрения атомов углерода, каждый имеет три гибридных орбитали sp 2 и одну негибридизированную p-орбиталь.Три орбитали sp 2 лежат в одной плоскости под углом 120 градусов. Когда атомы углерода приближаются друг к другу, их орбитали перекрываются и образуют связь. Одновременно p-орбитали сближаются и образуют связь. Для поддержания этой связи p-орбитали должны оставаться параллельными друг другу; следовательно, вращение невозможно.
Тройная связь включает в себя шесть электронов, сигма-связь и две [латексные] \ pi [/ латексные] связи. Простейшим органическим соединением с тройными связями является ацетилен, C 2 H 2 .Тройные связи сильнее двойных из-за наличия двух [латексных] \ pi [/ латексных] связей, а не одной. Каждый углерод имеет две sp-гибридные орбитали, и одна из них перекрывается со своей соответствующей от другого атома углерода, образуя sp-sp сигма-связь. Остальные четыре негибридизованных p-орбитали перекрываются друг с другом и образуют две [латексные] \ pi [/ латексные] связи. Подобно двойным связям, вращение вокруг оси тройной связи невозможно.
Наблюдаемые последствия множественных облигаций
Прочность сцепления
Ковалентные связи можно классифицировать по количеству энергии, которое требуется для их разрыва.Основываясь на экспериментальном наблюдении, что для разрыва связи между двумя атомами кислорода в O 2 требуется больше энергии, чем между двумя атомами водорода в H 2 , мы делаем вывод, что атомы кислорода связаны друг с другом более прочно. Мы говорим, что связь между двумя атомами кислорода на сильнее, чем на , чем связь между двумя атомами водорода.
Эксперименты показали, что двойные связи прочнее одинарных, а тройные связи прочнее двойных. Следовательно, для разрыва тройной связи в N 2 потребуется больше энергии по сравнению с двойной связью в O 2 .Действительно, для разрушения молекулы O 2 требуется 497 ккал / моль, а для разрушения молекулы N 2 требуется 945 кДж / моль.
Длина скрепления
Еще одним следствием наличия кратных связей между атомами является разница в расстоянии между ядрами связанных атомов. Двойные связи имеют на более короткие расстояния, чем одинарные связи, а тройные связи на короче, чем на двойные связи.
Показать источники
Boundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета.Этот конкретный ресурс использовал следующие источники:
9.3: Алкены — Chemistry LibreTexts
Алкены содержат двойные углерод-углеродные связи и представляют собой ненасыщенные углеводороды с молекулярной формулой C n H 2n . Это также та же молекулярная формула, что и циклоалканы. Алкены названы с использованием тех же общих правил именования алканов, за исключением того, что теперь используется суффикс -ene. Есть еще несколько небольших отличий:
- Основная цепь атомов углерода должна содержать оба атома углерода в двойной связи.Основная цепь пронумерована так, чтобы двойная связь получила наименьший номер.
- Перед корневым именем пишется номер атома углерода, у которого начинается двойная связь (меньшее число).
- Если присутствует более одной двойной связи, префиксы ди-, три-, тетра- и т. Д. Используются перед -ene, и (как ни странно) буква «а» добавляется после префикса количества атомов углерода. .
Введение
Алкены и алкины представляют собой углеводороды, которые соответственно имеют углерод-углеродных двойных связей, и углерод-углеродных тройных связей, функциональных групп.Молекулярные формулы этих ненасыщенных углеводородов отражают множественное связывание функциональных групп:
Алкены названы так, как если бы они были алканами, но суффикс «-ан» заменен на «-ен». Если алкен содержит только одну двойную связь и эта двойная связь является концевой (двойная связь находится на одном или другом конце молекулы), то нет необходимости помещать какое-либо число перед названием.
бутан: C 4 H 10 (CH 3 CH 2 CH 2 CH 3 )
бутен: C 4 H 8 (CH 2 = CHCH 2 CH 3 )
Если двойная связь не является концевой (если она находится на атоме углерода где-то в центре цепи), то атомы углерода должны быть пронумерованы таким образом, чтобы дать первому из двух атомов углерода с двойной связью наименьшее возможное число, и это число должно предшествовать суффиксу «ene» с тире, как показано ниже.
правильно: пент-2-ен (CH 3 CH = CHCH 2 CH 3 )
неверно: пент-3-ен (CH 3 CH 2 CH = CHCH 3 )
Второй неверен, потому что переворот формулы по горизонтали приводит к меньшему количеству алкена.
Если в алкене более одной двойной связи, все связи должны быть пронумерованы в названии молекулы — даже концевые двойные связи.Числа должны идти от наименьшего к наибольшему и отделяться друг от друга запятой. Цифровые префиксы IUPAC используются для обозначения количества двойных связей.
окта-2,4-диен: CH 3 CH = CHCH = CHCH 2 CH 2 CH 3
дека-1,5-диен: CH 2 = CHCH 2 CH 2 CH = CHCH 2 CH 2 CH 2 CH 3
Обратите внимание, что нумерация «2-4» выше дает молекулу с двумя двойными связями, разделенными только одной одинарной связью.Двойные связи в таком состоянии называются «конъюгированными», и они представляют повышенную стабильность конформации, поэтому они энергетически предпочтительны в качестве реагентов во многих ситуациях и комбинациях.
| Алкан | C n H 2n + 2 | Это максимальное отношение H / C для данного числа атомов углерода. |
|---|---|---|
| Алкен | C n H 2n | Каждая двойная связь уменьшает количество атомов водорода на 2. |
Исходная структура — это самая длинная цепь, содержащая оба атома углерода двойной связи. Два атома углерода двойной связи и четыре присоединенных к ним атома лежат в плоскости с валентными углами приблизительно 120 °. Двойная связь состоит из одной сигма-связи, образованной перекрытием гибридных орбиталей sp 2 , и образованной одной пи-связи. перекрытием параллельных 2 p орбиталей
Рисунок 1: (а) С-связанная структура образована перекрытием двух наборов однократно занятых углеродных sp 2 гибридных орбиталей и четырех однократно занятых водородных 1 s орбиталей с образованием электронных парных связей.При этом используются 10 из 12 валентных электронов для образования пяти σ-связей (четыре связи C – H и одна связь C – C). (b) Одна однозонно занятая негибридизованная 2 p z орбиталь остается на каждом атоме углерода, образуя π-связь углерод-углерод. (Примечание: в плоских молекулах по соглашению ось, перпендикулярная плоскости молекулы, соответствует оси z ).Молекулярная формула углеводорода дает информацию о возможных структурных типах, которые он может представлять. Например, рассмотрим соединения формулы C 5 H 8 .Формула пятиуглеродного алканпентана: C 5 H 12 , поэтому разница в содержании водорода равна 4. Это различие предполагает, что такие соединения могут иметь тройную связь, две двойные связи, кольцо плюс двойную связь или два кольца. Здесь показаны некоторые примеры, а еще как минимум четырнадцать!
Правила ИЮПАК по номенклатуре алкенов и циклоалкенов
- Суффикс (окончание) ен указывает на алкен или циклоалкен.
- Самая длинная цепь, выбранная для корневого имени, должна включать обоих атомов углерода двойной связи .
- Корневая цепь должна быть пронумерована от конца, ближайшего к атому углерода с двойной связью . Если двойная связь находится в центре цепи, правило ближайшего заместителя используется для определения конца, с которого начинается нумерация.
- Меньшее из двух чисел, обозначающих атомы углерода двойной связи, используется в качестве локатора двойной связи.Если присутствует более одной двойной связи, соединение называется диеном, триеном или эквивалентным префиксом, указывающим количество двойных связей, и каждой двойной связи присваивается номер локатора.
- В циклоалкенах атомам углерода с двойной связью назначены положения кольца №1 и №2. Какой из двух является №1, может быть определено правилом ближайшего заместителя.
- Группы заместителей, содержащие двойные связи:
H 2 C = CH– Винильная группа
H 2 C = CH – CH 2 — Аллильная группа
Пример 1
На этой диаграмме это цис-конформация.У него оба заместителя идут вверх. Эта молекула будет называться (цис) 5-хлор-3-гептеном.)
Trans будет выглядеть так
v. С другой стороны, если к алкену присоединены 3 или 4 различных атома, не являющихся водородом, тогда используйте систему E, Z.
E (entgegen) означает, что группы с более высоким приоритетом расположены напротив друг друга относительно двойной связи.
Z (zusammen) означает, что группы с более высоким приоритетом находятся на одной стороне относительно двойной связи.
(Вы можете думать о Z как о Заме Зиде, чтобы запомнить его.)
Пример 2
Решение
В этом примере это Е-4-хлор-3-гептен. Это E, потому что хлор и CH 2 CH 3 являются двумя более высокими приоритетами, и они находятся на противоположных сторонах.
vi. Гидроксильная группа имеет приоритет над двойной связью. Поэтому алкены, содержащие алхольные группы, называются алкенолами. И префикс становится —enol.А это значит, что теперь спирт имеет самый низкий приоритет перед алкеном.
vii. Напоследок помните, что алкеновые заместители называются алкенилами. Суффикс —enyl.
Вот таблица, содержащая системные названия первых двадцати алкенов с прямой цепью.
| Имя | Молекулярная формула |
| Этен | С 2 В 4 |
| пропен | С 3 В 6 |
| бутен | С 4 В 8 |
| Pentene | С 5 В 10 |
| гексен | С 6 В 12 |
| Гептен | C 7 H 14 |
| октен | С 8 В 16 |
| Нонен | С 9 В 18 |
| Децен | С 10 В 20 |
| Undecene | С 11 В 22 |
| Додецен | C 12 H 24 |
| тридецен | C 13 H 26 |
| Тетрадецен | C 14 H 28 |
| Пентадецен | С 15 В 30 |
| гексадецен | С 16 В 32 |
| Гептадецен | C 17 H 34 |
| Октадецен | C 18 H 36 |
| Нонадецен | С 19 В 38 |
| Эйкосин | С 20 В 40 |
Вы заметили, что нет метена? Потому что углерод не может иметь двойную связь ни с чем.
Геометрические изомеры
Двойные связи могут существовать в виде геометрических изомеров, и эти изомеры обозначаются с использованием обозначения цис / транс или современного обозначения E / Z.
цис-изомеры
. Две самые большие группы находятся на одной стороне двойной связи.
транс-изомеры
… Две самые большие группы находятся по разные стороны двойной связи.
Номенклатура E / Z
E = entgegan («транс») Z = zusamen («cis»)
Приоритет групп основан на атомной массе присоединенных атомов (а не на размере группы).Атом, присоединенный кратной связью, учитывается один раз для каждой связи.
атом фтора> изопропильная группа> н-гексильная группа
атом дейтерия> атом водорода
-CH 2 -CH = CH 2 > -CH 2 CH 2 CH 3
Пример 3
Попробуйте назвать следующие соединения, используя оба обозначения …
Общие названия
Удалите суффикс -ane и добавьте -ylene.Есть несколько уникальных, таких как общее название этенила винил и общее название 2-пропенила аллил. Вам следует знать …
- виниловый заместитель H 2 C = CH-
- аллильный заместитель H 2 C = CH-CH 2 —
- молекула аллена H 2 C = C = CH 2
- изопрен
Эндоциклические алкены
Эндоциклические двойные связи содержат оба атома углерода в кольце, а экзоциклические двойные связи содержат только один углерод в составе кольца.
Циклопентен представляет собой пример эндоциклической двойной связи.
Метиленцилопентан является примером экзоциклической двойной связи.
Назовите следующие соединения …
1-метилциклобутен. Метильная группа размещает двойную связь. Правильно также называть это соединение 1-метилциклобут-1-еном.
1-этенилциклогексен, метильная группа размещает двойную связь.Правильно также называть это соединение 1-этенилциклогекс-1-еном. Обычное название — 1-винилциклогексен.
Попробуйте нарисовать структуры для следующих соединений …
- 2-винил-1,3-циклогексадиен
Список литературы
- Воллхардт, Питер и Нил Э. Шор. Органическая химия: структура и функции . 5-е издание. Нью-Йорк: W. H. Freeman & Company, 2007. .
Проблемы
Попробуйте назвать следующие соединения…
1-пентен или пент-1-ен
2-этил-1-гексен или 2-этилгекс-1-ен
Попробуйте нарисовать структуры для следующих соединений …
CH 3 –CH = CH – CH 2 –CH 3
CH 3 –CH 2 –CH = CH – CH 2 –CH 2 –CH 3
г. Дайте двойной связи наименьшее возможное число независимо от размещения заместителя.
• Попробуйте назвать следующее соединение…
Дж
• Попробуйте нарисовать структуру следующего соединения …
4-метил-2-пентен J
Назовите следующие структуры:
v. Нарисуйте (Z) -5-Хлор-3-этил-4-гексен-2-ол.
ответов
I. транс-8-этил-3-ундецен
II. E-5-бром-4-хлор-7,7-диметил-4-ундецен
III. Z-1,2-дифторциклогексен
IV. 4-этенилциклогексанол.
В.
Номенклатура алкенов — Chemistry LibreTexts
Молекулярная формула углеводорода дает информацию о возможных структурных типах, которые он может представлять.Например, рассмотрим соединения формулы \ (\ ce {C5H8} \). Формула пятиуглеродного алканпентана \ (\ ce {C5h22} \), поэтому разница в содержании водорода равна 4. Это различие предполагает, что такие соединения могут иметь тройную связь, две двойные связи, кольцо плюс двойную связь, или два кольца. Здесь показаны некоторые примеры, а еще как минимум четырнадцать!
Следовательно, как и в случае с алканами, необходимо принять согласованную систему номенклатуры, которая может разделить природу этих ненасыщенных химических веществ.Самыми простыми из них являются алкены, представляющие собой углеводороды с двойной связью углерод-углерод, функциональных групп и ненасыщенные углеводороды с молекулярной формулой \ (\ ce {Cnh3n} \), которая также имеет ту же молекулярную формулу, что и циклоалканы.
Правила ИЮПАК по номенклатуре алкенов
- Суффикс (окончание) ен указывает на алкен или циклоалкен.
- Самая длинная цепь, выбранная для корневого имени, должна включать обоих атомов углерода двойной связи .
- Корневая цепь должна быть пронумерована от конца, ближайшего к атому углерода с двойной связью . Если двойная связь находится в центре цепи, правило ближайшего заместителя используется для определения конца, с которого начинается нумерация.
- Меньшее из двух чисел, обозначающих атомы углерода двойной связи, используется в качестве локатора двойной связи.
- Если присутствует более одной двойной связи, соединение обозначается как диен, триен или эквивалентный префикс, указывающий количество двойных связей, и каждой двойной связи присваивается номер локатора.
- Группы заместителей, содержащие двойные связи:
- H 2 C = CH– Виниловая группа
- H 2 C = CH – CH 2 — Аллильная группа
Правило 1
Алкены названы с использованием тех же общих правил наименования для алканов, за исключением того, что теперь используется суффикс -ene. Вот диаграмма, содержащая системные названия первых двадцати алкенов с прямой цепью.
| Имя | Молекулярная формула | Имя | Молекулярная формула | |
|---|---|---|---|---|
| Этен | C 2 H 4 | Undecene | С 11 В 22 | |
| Пропен | С 3 В 6 | Додецен | С 12 В 24 | |
| Бутен | С 4 В 8 | Tridecene | С 13 В 26 | |
| Pentene | С 5 В 10 | Тетрадецен | C 14 H 28 | |
| гексен | С 6 В 12 | Пентадецен | С 15 В 30 | |
| Гептен | С 7 В 14 | гексадецен | С 16 В 32 | |
| октен | С 8 В 16 | Гептадецен | C 17 H 34 | |
| Нонен | С 9 В 18 | Октадецен | С 18 В 36 | |
| Decene | С 10 В 20 | Нонадецен | С 19 В 38 |
Вы заметили, что нет метена? Потому что углерод не может иметь двойную связь ни с чем.
Правило 2
Исходная структура — это самая длинная цепь, содержащая оба атома углерода двойной связи. Если алкен содержит только одну двойную связь и эта двойная связь является концевой (двойная связь находится на одном или другом конце молекулы), то нет необходимости помещать какое-либо число перед названием.
- бутан: C 4 H 10 (\ (\ ce {Ch4Ch3Ch3Ch4} \))
- бутен: C 4 H 8 (\ (\ ce {Ch3 = CHCh3Ch4} \))
Если двойная связь не является концевой (если она находится на атоме углерода где-то в центре цепи), тогда атомы углерода должны быть пронумерованы таким образом, чтобы дать первому из двух атомов углерода с двойной связью наименьшее возможное число. , и это число должно предшествовать суффиксу «ene» с тире, как показано ниже.
- правильно: пент-2-ен (\ (\ ce {Ch4CH = CHCh3Ch4} \))
- неверно: пент-3-ен (\ (\ ce {Ch4Ch3CH = CHCh4} \))
Второй вариант неверен, потому что переворот формулы по горизонтали приводит к меньшему количеству алкена.
Упражнение \ (\ PageIndex {1} \)
Назовите следующие соединения:
а:
г.
- Ответьте на
-
1-пентен или пент-1-ен
- Ответ б
-
2-этил-1-гексен или 2-этилгекс-1-ен
Упражнение \ (\ PageIndex {2} \)
a: Назовите следующее соединение (подсказка: дайте двойной связи наименьшее возможное число, независимо от размещения заместителя).
г. Изобразите структуру 4-метил-2-пентена.
- Ответьте на
-
4-метилпент-1-ен
- Ответ б
-
Правило 4
Если в алкене более одной двойной связи, все связи должны быть пронумерованы в названии молекулы — даже концевые двойные связи. Числа должны идти от наименьшего к наибольшему и отделяться друг от друга запятой.Цифровые префиксы IUPAC используются для обозначения количества двойных связей.
- окта-2,4-диен: \ (\ ce {Ch4CH = CHCH = CHCh3Ch3Ch4} \)
- дека-1,5-диен: \ (\ ce {Ch3 = CHCh3Ch3CH = CHCh3Ch3Ch3Ch4} \)
Обратите внимание, что нумерация «2-4» выше дает молекулу с двумя двойными связями, разделенными только одной одинарной связью. Двойные связи в таком состоянии называются «конъюгированными», и они представляют повышенную стабильность конформации, поэтому они энергетически предпочтительны в качестве реагентов во многих ситуациях и комбинациях.
Правило 4: Геометрические изомеры
Двойные связи могут существовать в виде геометрических изомеров, и эти изомеры обозначаются с использованием обозначения цис / транс или более гибкого обозначения E / Z.
цис Изомеры имеют две самые большие группы на одной стороне двойной связи (левая структура выше), а у транс-изомеров две самые большие группы находятся на противоположных сторонах двойной связи (правая структура наверху).
Если к алкену присоединены 3 или 4 различных атома, не являющихся водородом, тогда используйте систему E, Z.
- E (entgegen) означает, что группы с более высоким приоритетом находятся напротив друг друга относительно двойной связи.
- Z (zusammen) означает, что группы с более высоким приоритетом находятся на одной стороне относительно двойной связи.
E = entgegan («транс») Z = zusamen («cis»)
Приоритет групп основан на атомной массе присоединенных атомов (а не на размере группы). Атом, присоединенный кратной связью, учитывается один раз для каждой связи.
атом фтора> изопропильная группа> н-гексильная группа
атом дейтерия> атом водорода
-CH 2 -CH = CH 2 > -CH 2 CH 2 CH 3
Пример \ (\ PageIndex {5} \)
Попробуйте назвать следующие соединения, используя условные обозначения цис-транс и E / Z:
а:
б:
- Ответьте на
-
4-метилпент-1-ен
- Ответ б
-
Пример \ (\ PageIndex {3} \)
Как называется эта молекула?
Решение
На этой диаграмме это цис-конформация.У него оба заместителя идут вверх. Эта молекула будет называться (цис) 5-хлор-3-гептеном.)
Trans будет выглядеть так
Пример \ (\ PageIndex {4} \)
Как называется эта молекула?
Решение
В этом примере это Е-4-хлор-3-гептен. Это E, потому что хлор и CH 2 CH 3 являются двумя более высокими приоритетами, и они находятся на противоположных сторонах.
Общие названия
Удалите суффикс -ane и добавьте -ylene.Есть несколько уникальных, таких как общее название этенила винил и общее название 2-пропенила аллил. Вам следует знать …
- виниловый заместитель H 2 C = CH-
- аллильный заместитель H 2 C = CH-CH 2 —
- молекула аллена H 2 C = C = CH 2
- изопрен
Эндоциклические алкены
Эндоциклические двойные связи содержат оба атома углерода в кольце, а экзоциклические двойные связи содержат только один углерод в составе кольца.
Циклопентен представляет собой пример эндоциклической двойной связи.
Метиленцилопентан является примером экзоциклической двойной связи.
Упражнение \ (\ PageIndex {1} \)
Назовите следующие соединения:
а:
б:
- Ответьте на
-
1-метилциклобутен. Метильная группа размещает двойную связь. Правильно также называть это соединение 1-метилциклобут-1-еном.
- Ответ б
-
1-этенилциклогексен, метильная группа размещает двойную связь. Правильно также называть это соединение 1-этенилциклогекс-1-еном. Обычное название — 1-винилциклогексен.
Упражнение \ (\ PageIndex {1} \)
Назовите следующие соединения:
а:
б:
- Ответьте на
-
1-метилциклобутен.Метильная группа размещает двойную связь. Правильно также называть это соединение 1-метилциклобут-1-еном.
- Ответ б
-
1-этенилциклогексен, метильная группа размещает двойную связь. Правильно также называть это соединение 1-этенилциклогекс-1-еном. Обычное название — 1-винилциклогексен.
Упражнение \ (\ PageIndex {1} \)
Изобразите структуры следующего 2-винил-1,3-циклогексадиена
- Ответ
-
Список литературы
- Воллхардт, Питер и Нил Э.Шор. Органическая химия: структура и функции . 5-е издание. Нью-Йорк: W. H. Freeman & Company, 2007. .
Проблемы
Попробуйте назвать следующие соединения …
1-пентен или пент-1-ен
2-этил-1-гексен или 2-этилгекс-1-ен
Попробуйте нарисовать структуры для следующих соединений …
CH 3 –CH = CH – CH 2 –CH 3
CH 3 –CH 2 –CH = CH – CH 2 –CH 2 –CH 3
г.Дайте двойной связи наименьшее возможное число независимо от размещения заместителя.
• Попробуйте назвать следующее соединение …
Дж
• Попробуйте нарисовать структуру следующего соединения …
4-метил-2-пентен J
Назовите следующие структуры:
v. Нарисуйте (Z) -5-Хлор-3-этил-4-гексен-2-ол.
ответов
I. транс-8-этил-3-ундецен
II. E-5-бром-4-хлор-7,7-диметил-4-ундецен
III.Z-1,2-дифторциклогексен
IV. 4-этенилциклогексанол.
В.
Двойная связь: определение, формирование и пример — видео и стенограмма урока
Формирование двойных связей
Двойные связи образуются, когда два атома должны совместно использовать четыре электрона для выполнения правила октетов. Правило октетов гласит, что атомы будут терять, приобретать или делиться электронами, чтобы иметь восемь валентных электронов. Двойные связи образуются в природе довольно часто и обычно образуются неметаллами, такими как углерод, азот и кислород.Чтобы понять, как образуются двойные связи, давайте посмотрим, что происходит со строительными блоками связей — электронами.
Электроны беспорядочно и быстро перемещаются вокруг атома. Электроны будут оставаться в определенных формах в зависимости от их уровня энергии и близости к ядру. Конкретные формы, населенные электронами, называются электронными орбиталями . Есть четырех форм электронных орбиталей : s, p, d и f. В двойных связях участвуют s- и p-орбитали.
Некоторые атомы могут отдавать больше электронов двойной связи, а другие — меньше. Независимо от того, какой атом что принес, атомы должны перемещаться вокруг своих доступных электронов, чтобы обеспечить совместное использование четырех электронов.
Каждый атом должен сначала соединить свою крайнюю s-орбиталь с p-орбиталью, чтобы образовалась так называемая sp-орбиталь. Эта гибридизированная орбиталь будет содержать два электрона. Sp-орбиталь каждого атома будет перекрываться, так что каждый атом будет иметь доступ к этим двум электронам.Эта облигация известна как сигма-облигация . Затем каждый атом будет использовать одну из двух оставшихся p-орбиталей, чтобы разделить два электрона с другим атомом. Электроны, совместно используемые в перекрывающихся p-орбиталях, называются пи-связями . Двойная связь состоит из одной сигма-связи и одной пи-связи. На рисунке показано, как они расположены между двумя атомами кислорода (см. Видео).
Примеры
Двойные связи довольно часто встречаются в соединениях. Вдохните. Вы только что вдохнули столько двойных связей! Газообразный кислород, одна из важнейших молекул для жизни, составляет 20% воздуха вокруг нас и 20% каждого вдоха, который мы делаем.Когда кислород связывается сам с собой, он должен разделять в общей сложности четыре электрона, чтобы каждый атом соответствовал правилу октетов.
Выдохните. Когда мы выдыхаем, мы выделяем углекислый газ, молекулу, содержащую две двойные связи. Двуокись углерода образуется при сгорании углеводородов, таких как бензин или природный газ. Интересно, что растениям нужен этот бесцветный газ без запаха для фотосинтеза.
Ацетон — это простое углеродное соединение, которое содержит одну двойную связь между углеродом и кислородом.Если вы когда-нибудь были в маникюрном салоне или даже проходили мимо него, вы, вероятно, чувствовали запах ацетона. Этот состав можно использовать для удаления жестких лаков, таких как лак для ногтей, или в качестве чистящего растворителя в лабораториях.
Нам всем пришлось бы использовать намного больше солнцезащитного крема, если бы не молекула озона. Озон — это соединение трех атомов кислорода, связанных вместе. Это соединение имеет одну двойную связь, которая перемещается из стороны в сторону. Двойная связь возникает с левой стороны молекулы в 50% случаев, и она встречается с правой стороны молекулы в 50% случаев.Озон поглощает вредное излучение солнца, защищая нас, землян от опасной энергии.
Резюме урока
Двойная связь образуется, когда два атома разделяют две пары электронов. Совместное использование двух электронов известно как ковалентная связь . Двойные связи и прочнее, и короче одинарных.
Двойные связи включают обмен электронами между одной p-орбиталью связывающих атомов, а также обмен электронами между sp-орбиталью каждого атома.Когда р-орбитали участвуют в связывании, это называется связью пи . Когда две sp-орбитали участвуют в связывании, это называется сигма-связью . Двойные связи состоят из одной пи-связи и одной сигма-связи. Примеры соединений с двойными связями включают газообразный кислород, диоксид углерода, ацетон и озон.
Определение двойной связи в химии.
Примеры двойной связи в следующих темах:
-
Стереоселективность в дополнительных реакциях на двойные связи
- Как показано на рисунке ниже, связь pi- фиксирует двойную связь углерод-углерод в плоской конфигурации и не допускает свободного вращения вокруг самой связи двойной .
- Таким образом, мы видим, что реакции присоединения к этой функции могут происходить тремя разными способами, в зависимости от относительной ориентации атомов или групп, которые присоединяются к атомам углерода двойной связи : (i) они могут связывать из с одной стороны, (ii) они могут связывать с противоположных сторон, или (iii) они могут связывать случайным образом с обеих сторон.
- Поскольку начальная электрофильная атака на двойную связь может происходить одинаково хорошо с любой стороны, именно на второй стадии (или стадии) реакции ( связывание нуклеофила) может быть наложена стереоселективность.
- Если двухступенчатый механизм, описанный выше, верен, и если промежуточный карбокатион является достаточно долгоживущим, чтобы свободно вращаться вокруг компонента связи сигма- исходной двойной связи , мы ожидаем найти случайную или нестереоселективное добавление в продукты.
-
Циклизация реакциями внутримолекулярного присоединения
- Если радикал соединен с двойной связью цепью из трех или более атомов углерода, внутримолекулярное присоединение образует кольцо.
- Региоселективность таких добавок определяется больше стереоэлектронными факторами, чем заместителями на двойной связи .
- Как показано на следующей диаграмме, он находится под углом почти 20º от перпендикуляра к плоскости двойной связи .
- Из-за этого требования многие циклизации до колец среднего размера протекают путем радикальной атаки на ближайший атом углерода двойной связи , независимо от замещения.
- Конечно, если углеродная цепь, связывающая радикальный сайт с двойной связью , достаточно длинная, , связывающая с любой из двойной связи атомов углерода, учитывает стереоэлектронный фактор, и продукт снова определяется подмена.
-
Конфигурационные стереоизомеры алкенов
- Двойная связь углерод-углерод образуется между двумя sp2-гибридизированными атомами углерода и состоит из двух занятых молекулярных орбиталей, сигма-орбитали и пи-орбитали.
- Вращение концевых групп двойной связи относительно друг друга разрушает перекрытие p-орбиталей, которое создает пи-орбиталь или связь .
- Существенным требованием для этой стереоизомерии является то, что каждый углерод двойной связи должен иметь две разные группы заместителей (одна может быть водородом).
- В первом примере левая двойная связь углерода имеет два идентичных заместителя (A), поэтому стереоизомерия по двойной связи невозможна (замена заместителей на правом атоме углерода дает ту же конфигурацию ).
- В следующих двух примерах каждый атом углерода с двойной связью имеет две разные группы заместителей, и существует стереоизомерия, независимо от того, являются ли два заместителя на одном атоме углерода такими же, как и на другом.
-
Двойные и тройные ковалентные связи
- Двойная связь между двумя атомами углерода состоит из сигма-связи и связи π .
- Тройные связи сильнее, чем двойные связи из-за наличия двух облигаций $ \ pi $ , а не одной.
- Подобно двойной связи , вращение вокруг оси тройной связи невозможно.
- Эксперименты показали, что двойные связи прочнее одинарных связи , а тройные связи сильнее, чем двойные связи .
- Двойные связи имеют более короткие расстояния, чем одинарные связи , а тройные связи короче, чем двойные связи .
-
Свойства алкенов
- Из-за наличия двойной связи в углеродном скелете алкены более реакционноспособны, чем родственные им алканы.
- Алкены содержат двойную связь , которая состоит из одной сигма-связи и одной пи- связи между двумя атомами углерода.
- Атомы углерода в двойной связи гибридизуются sp2, образуя плоскую структуру.
- Вращение вокруг двойной связи нежелательно, поэтому алкены образуют довольно стабильные изомеры в зависимости от расположения заместителей на одной (цис) или противоположных (транс) сторонах двойной связи .
- Алкены более реакционноспособны, чем родственные им алканы из-за относительной нестабильности двойной связи .
-
Обозначение алкенов и алкинов
- Алкены и алкины названы так же, как алканы, на основе самой длинной цепи, которая содержит двойную или тройную связь .
- Алкены — это углеводороды, которые содержат одну или несколько двойных связей , в то время как алкины содержат одну или несколько тройных связей .
- Вращение ограничено вокруг двойной связи , поэтому для дифференциации стереоизомеров можно добавлять префиксы.
- Для циклоалкенов атомы углерода в двойной связи пронумерованы как позиции 1 и 2.
- Для соединений, содержащих как двойные , так и тройные связи , суффикс «-ene» предшествует «-yne», и соединение пронумеровано так, чтобы свести к минимуму положений связи .
-
Гибридизация в молекулах, содержащих двойные и тройные связи
- sp2, sp-гибридизации и связывание pi- можно использовать для описания химической связи в молекулах с двойными и тройными связями .
- Этен (C2h5) имеет двойную связь между атомами углерода.
- В этом случае sp-гибридизация приводит к двум двойным связям .
- Оставшиеся негибридизированные p-орбитали перекрываются для двойных и тройных пи связей .
- Опишите роль гибридизации в образовании двойных и тройных связей .
-
Физические свойства ковалентных молекул
- Теория связывания Льюиса может объяснить многие свойства соединений.
- Теория Льюиса также учитывает длины связи ; чем прочнее связь и чем больше электронов разделено, тем короче связь , длина .
- Согласно теории, тройные связи сильнее, чем двойные связи и двойные связи прочнее одинарных связей .
- Однако теория предполагает, что прочность связи у двойных связей в два раза выше, чем у одинарных связей , что неверно.
- Обсудите качественные предсказания теории ковалентной связи относительно точек кипения и плавления, длины и прочности связи и проводимости молекул
-
Bond Energy
- Поскольку реакции органических соединений включают образование и разрыв связей , прочность связей или их устойчивость к разрыву становится важным фактором.
- Связь энергия — это энергия, необходимая для гомолитического разрыва ковалентной связи (на нейтральные фрагменты).
- Энергия связи обычно дается в единицах ккал / моль или кДж / моль и обычно называется энергией диссоциации связи , если дана для конкретных связей , или средней энергией связи при суммировании для данного типа связь на многие виды соединений.
- В следующей таблице собраны средние энергии связи для множества обычных связей .
- Во-первых, одинарная связь между двумя данными атомами слабее, чем двойная связь , которая, в свою очередь, слабее тройной связи .
-
Ковалентные облигации
- Ковалентное связывание взаимодействия включают связывание сигма- (σ) и связывание pi- (π).
- Одиночные связи возникают, когда два электрона являются общими и состоят из одной сигма-связи между двумя атомами.
- Двойные связи возникают, когда четыре электрона разделяются между двумя атомами и состоят из одной сигма-связи и одной пи связи .
- Тройные связи возникают, когда шесть электронов разделяются между двумя атомами и состоят из одной сигма-связи и двух пи--связей (дополнительную информацию о пи- и сигма-связях см. В более поздней концепции).
- В отличие от ионной связи , ковалентная связь сильнее между двумя атомами с аналогичной электроотрицательностью.
Инфракрасная спектроскопия алкенов
Например, ароматические кольца имеют порядок связи углерод-углерод около 1,5 (3), а прототип ароматического соединения бензол с химической формулой C 6 H 6 может иметь атомы водорода. добавляли к нему с образованием насыщенного соединения циклогексана, C 6 H 12 (3). Этот пример показывает, что бензол и другие ароматические кольца содержат ненасыщенные атомы углерода.
Другое семейство непредельных углеводородов содержит двойные углерод-углеродные связи, C = C, и называется алкенами.В этой колонке основное внимание уделяется использованию инфракрасной (ИК) спектроскопии, чтобы отличить разные типы алкенов друг от друга.
Кроме того, начиная с этой части колонки, я перестану использовать см -1 после каждой позиции пика. Забегая вперед, вы можете просто предположить, что единицы положения пика будут в волновых числах (см -1 ), хотя в тексте этого не говорится.
Химическая структура алкенов
Алкены содержат ненасыщенные атомы углерода, потому что связи C = C могут иметь атомы водорода, добавленные к ним посредством реакции, известной как гидрирование с образованием насыщенных атомов углерода (3).Гидрогенизированное растительное масло содержит ненасыщенные жиры, двойные связи которых C = C гидрогенизированы с образованием насыщенных жиров.
Структурные изомеры — это молекулы, которые имеют одинаковую химическую формулу, но разные химические структуры, такие как орто-, мета- и пара-изомеры дизамещенных бензольных колец, обсуждавшиеся ранее (4). ИК-спектроскопия позволяет различать структурные изомеры, поскольку эти молекулы имеют разную силу связи, уменьшенную массу и, следовательно, разные положения пиков (5).Алкены состоят из шести различных разновидностей, некоторые из которых проявляют структурную изомерию. Схема различных типов алкенов показана на рисунке 1.
Винильные группы состоят из двойной связи с тремя атомами водорода и одним неводородным атомом, которые в дальнейшем будут называться «R-группами». Виниловые группы важны в промышленности, поскольку они реагируют с образованием обычных полимеров, таких как полипропилен, полистирол и поливинилхлорид.
Существует три различных структурных изомера алкена, которые состоят из связи C = C с двумя присоединенными атомами водорода и двумя R-группами.В молекуле винилидина два атома водорода присоединены к одному атому углерода, а R-группы — к другому атому углерода. Молекулы винилидена не используются в промышленности и не будут обсуждаться далее. Два других типа связей C = C с двумя атомами водорода называются цис и транс . Как показано на рисунке 1, цис-изомеры имеют свои водороды на одной стороне двойной связи, в то время как транс-изомеры имеют свои атомы водорода по диагонали друг от друга. Один из способов запомнить эти термины состоит в том, что латинское слово «trans» означает «через», а английский глагол «транспортировать» означает переносить что-либо из одного места в другое.Приставка cis также образована от латинского слова и означает «на ближней стороне». Цис- и транс-изомеры жиров были в новостях из-за их влияния на здоровье человека. Сегодня на многих пищевых этикетках содержится информация о том, сколько цис- и транс-жиров содержится в продукте. Как мы увидим ниже, цис- и транс-изомеры имеют разные ИК-спектры, поэтому ИК-спектроскопию можно использовать для различения и количественного определения этих жиров в образцах.
Когда алкен содержит три R-группы и одну водород, он называется трехзамещенным алкеном .У них нет структурных изомеров. Наконец, связь C = C с четырьмя R-группами называется тетразамещенным алкеном и снова не имеет структурных изомеров. На мой взгляд, наиболее промышленно важными алкенами являются виниловые, цис-, транс- и тризамещенные разновидности. В результате наше обсуждение ниже сосредоточено на этих типах молекул. Мы обнаружим, что можем отличить все шесть типов алкенов друг от друга с помощью ИК-спектроскопии.
ИК-спектроскопия насыщенных и ненасыщенных углеродов
В предыдущем столбце (6) мы видели, что метил (CH 3 ) и метилен (CH 2 ), содержащие функциональные группы, имеют CH простирается ниже 3000.Другой тип насыщенного углерода, метиновая группа, которая состоит из атома углерода с тремя связями C-C и одной связью C-H, также имеет пик растяжения C-H ниже 3000 (метиновые группы будут обсуждаться в следующей колонке по разветвленным алканам). В общем, насыщенные атомы углерода имеют пики удлинения C-H ниже 3000.
Из нашего обсуждения ароматических колец мы обнаружили, что эти ненасыщенные молекулы имеют удлинения C-H выше 3000 (2). Алкены и алкины , ненасыщенные молекулы с тройными углерод-углеродными связями, также имеют удлинения C-H выше 3000.Итак, в целом, мы можем сказать, что молекулы с насыщенным углеродом имеют протяженность СН ниже 3000, в то время как молекулы с ненасыщенным углеродом имеют протяженность СН более 3000. Эти идеи суммированы в Таблице I.
В предыдущих столбцах я утверждал, что все из представленных мною диапазонов пиков есть исключения, и что нет никаких абсолютных правил, когда дело доходит до интерпретации ИК-спектров. Хотя правила в Таблице I имеют известные исключения, их немного, и Таблица I — отличный инструмент для использования при интерпретации ИК-спектров.Если образец имеет только C-H удлинения выше 3000, то, скорее всего, все атомы углерода ненасыщены, и я называю образец «только ненасыщенным». Если образец имеет только C-H удлинения ниже 3000, скорее всего, все атомы углерода насыщены, и я называю образец «только насыщенным». Если образец имеет удлинения C-H выше и ниже 3000, он, скорее всего, содержит насыщенные и ненасыщенные атомы углерода, и я называю его «смешанным» образцом. Определение того, находятся ли участки C-H в спектре выше или ниже 3000, быстро и легко, и это должно быть одним из первых фрагментов информации, которые вы извлекаете из спектра.
Напомним, что метильная и метиленовая группы имеют определенные пики удлинения C-H, которые можно использовать, чтобы отличить их друг от друга (6). К сожалению, в случае ненасыщенных углеродов такая ситуация, как правило, не выполняется. И ароматические кольца, и алкены обычно имеют протяженность С-Н от 3100 до 3000. Из-за этого перекрытия присутствие пиков в этом диапазоне является диагностическим признаком ненасыщенности, но не типа ненасыщенности. Чтобы определить тип ненасыщенности, потребуется использование других пиков в спектре, как обсуждается ниже.
ИК-спектроскопия алкенов
ИК-спектр винилсодержащей молекулы, 1-октена, показан на рисунке 2.
Рисунок 2: ИК-спектр 1-октена.
Обратите внимание, что в структуре молекулы, показанной на рисунке 2, есть метильные группы, метиленовые группы и связь C = C. Эта структура является примером смешанной молекулы, и, следовательно, она должна иметь удлинения CH выше и ниже 3000. Это действительно так, поскольку пик растяжения винила CH обозначен буквой A и падает на 3077, а CH 3 и CH 2 пика растяжения образуют конверт ниже 3000.
В дополнение к связям C-H, алкены, конечно, имеют связи C = C. Растяжение этой двойной связи приводит к возникновению пика в спектрах алкенов между 1680 и 1630. В 1-октене этот пик приходится на 1641 и обозначен буквой B на рисунке 2. Как я писал ранее (5), один из Фактором, определяющим высоту пика ИК-излучения, является изменение дипольного момента по отношению к длине связи, dµ / d x , во время вибрации. Этот факт хорошо иллюстрируют интенсивности пиков валентных колебаний C = C алкенов.Если связь C = C имеет сильно электроотрицательный заместитель, такой как атом кислорода, связь C = C будет сильно поляризованной, dµ / d x будет большим, а пик растяжения C = C будет интенсивным. Если алкен имеет только атомы углерода и атомы водорода, расположенные вокруг двойной связи, и если он асимметрично замещен, dµ / d x будет меньше, а пик растяжения C = C будет менее интенсивным. Если алкен симметрично замещен, такой как этилен (C 2 H 4 ), участок C = C представляет собой симметричный участок симметричной молекулы, подобный симметричному участку CO 2 .В обоих случаях dµ / d x равно нулю, а пиковая интенсивность равна нулю (5). Таким образом, пик валентного сжатия C = C алкенов может быть интенсивным, слабым или отсутствовать в зависимости от заместителей и их расположения вокруг двойной связи. Следовательно, это не совсем надежное групповое волновое число.
Напомним, что бензольные кольца имеют «кольцевые моды» из-за растяжения углерод-углеродных связей в кольце, и они находятся между 1630 и 1400. Как обсуждалось выше, алкеновые удлинения C = C находятся между 1680 и 1630.Это означает, что точка 1630 в спектре является полезной разделительной линией, если есть удлинения C-H между 3100 и 3000 и пик между 1680 и 1630, ненасыщенность, вероятно, является алкеном. Если есть пики удлинения C-H между 3100 и 3000, нет пика между 1680 и 1630, но есть один или несколько острых пиков между 1630 и 1400, ненасыщенность, скорее всего, представляет собой ароматическое кольцо. Если есть удлинения C-H выше 3000, пики от 1680 до 1630 и пики от 1630 до 1460, то могут присутствовать как ароматическое кольцо, так и алкен.
В спектре 1-октена с низкими волновыми числами есть два интенсивных пика, вместе обозначенных буквой C на рисунке 2. Эти два пика происходят от изгибных колебаний C-H вне плоскости, или качелей , как я их называю. Как и ароматические кольца, связи C = C плоские, а связи C-H лежат в плоскости, определяемой двойной связью. Таким образом, связи C-H могут изгибаться выше и ниже плоскости молекулы так же, как собака виляет хвостом. Напомним, что для бензольных колец эти пики упали с 1000 до 700 (7).Изменения СН алкенов попадают в аналогичный диапазон, от 1000 до 600.
Подводя итог, можно сказать, что ИК-спектры алкенов характеризуются одним или несколькими пиками растяжения СН между 3100 и 3000, возможное удлинение С = С от 1680 до 1630, и один или несколько пиков колебания СН от 1000 до 600. В следующем разделе мы узнаем, как использовать удлинение двойной связи и пики колебания СН вместе, чтобы отличить разные типы алкенов друг от друга.
Различение типов алкенов
Мы использовали рисунок 2 как общий пример спектра двойной связи, но это также спектр винильной группы.Растяжение C = C приходится на 1641, а для виниловых групп этот пик обычно падает с 1660 до 1630. Пара резких, интенсивных колебаний C-H на 993 и 910 также указывает на винил. Эти пики обычно приходятся на 990 ± 5 и 910 ± 5. Оба этих пика должны появляться в спектре, чтобы присутствовала винильная группа. Эти два пика появляются в одном из самых узких видимых диапазонов и являются четкими и совершенными примерами групповых волновых чисел.
ИК-спектр цис-содержащей молекулы синтетического каучука показан на рисунке 3.
Рисунок 3: Инфракрасный спектр синтетического каучука.
Обратите внимание, что синтетический каучук содержит цис-двойную связь и метиленовые группы, представляет собой смешанную молекулу и имеет удлинения C-H выше и ниже 3000. Однако удлинение C-H на уровне 3006 также может быть связано с ароматическим кольцом. Тем не менее, пик на 1654 происходит от участка C = C. Для цис-двойных связей, как правило, этот пик падает с 1660 до 1630. Наконец, пик колебания цис-C-H наблюдается на 736. Этот пик обычно наблюдается при 690 ± 50 для цис-двойных связей.Многие каучукоподобные полимеры содержат связи C = C, поэтому их обнаружение с помощью ИК-спектроскопии важно в резиновой промышленности.
ЩЕЛКНИТЕ ИЗОБРАЖЕНИЕ ДЛЯ УВЕЛИЧЕНИЯ
ИК-спектр транс- -бутадиенового каучука показан на рисунке 4. Как можно догадаться из его названия, он содержит преимущественно транс двойные связи.
Рис. 4: Инфракрасный спектр транс -бутадиенового каучука.
Поскольку этот материал представляет собой смешанную молекулу, он имеет удлинения C-H выше и ниже 3000.Пик, обозначенный B при 1638, относится к присутствующим двойным транс-связям, а острый интенсивный пик при 966 — от колебания C-H транс-связей. Для транс-алкенов, как правило, удлинение C = C падает с 1680 до 1660, а колебание CH появляется на уровне 965 ± 5. Подобно колебаниям CH винильных групп, колебания CH двойной транс-связи резкие, интенсивные, узкий диапазон, и его очень легко обнаружить. Пик, обозначенный A на рис. 4 под номером 2217, представляет собой участок C≡N нитрила, спектр которого будет обсуждаться в следующей статье.
Наконец, ИК-спектр образца, содержащего тризамещенную двойную связь, натуральный каучук, показан на рисунке 5.
Рисунок 5: ИК-спектр натурального каучука.
Опять же, натуральный каучук представляет собой смешанную молекулу и имеет удлинение СН выше и ниже 3000. Растяжение С = С находится на уровне 1664, а колебание СН — на уровне 830. Для тризамещенных алкенов, как правило, эти пики падают с 1680 до 1660 и 815 ± 25.
Тетразамещенные алкены не имеют атомов водорода, присоединенных к фрагменту C = C, и, следовательно, не имеют пиков растяжения или колебания CH алкена.У них действительно есть пик растяжения C = C, который появляется от 1680 до 1660. Этот пик также появляется для других типов алкена, поэтому он не является диагностическим. Как обсуждалось выше, если тетразамещенный алкен имеет четыре идентичных заместителя, интенсивность пика участка C = C может быть равна нулю, и в этом случае не будет пиков, идентифицирующих присутствие тетразамещенного алкена в образце. Таблица II суммирует положения пиков для шести различных типов алкенов.
Обратите внимание на то, что из Таблицы II следует, что отрезки винилового, винилидинового и цис-C = C падают с 1660 до 1630, в то время как отрезки C = C транс-, тризамещенного и тетразамещенного алкена появляются с 1680 до 1660.Таким образом, мы можем использовать положение пика растяжения C = C, чтобы разбить алкены на две отдельные группы. Однако этого недостаточно для того, чтобы однозначно различать их всех, и именно здесь вступают в силу пометки C-H. Положение и количество колебаний C-H различны для каждого из типов алкенов. Следовательно, положение пика растяжения C = C и количество и положение колебаний C-H вместе можно использовать для различения этих алкенов друг от друга.
Список литературы
- до н.э. Smith, Spectroscopy 31 (9), 30–33 (2016).
- до н.э. Smith, Spectroscopy 31 (3), 34–37 (2016).
- Р. Моррисон и Р. Бойд, Organic Chemistry , 6-е издание (Prentice Hall, Englewood Cliffs, New Jersey, 1992).
- до н.э. Smith, Spectroscopy 31 (5), 36–39 (2016).
- до н.э. Smith, Spectroscopy 30 (1), 16–23 (2015).
- до н.э. Smith, Spectroscopy 30 (4), 18–23 (2015).
- до н.э. Smith, Spectroscopy 31 (7), 30–34 (2016).
Брайан С. Смит, доктор философии, , старший специалист по инфракрасным изделиям в компании PerkinElmer, базирующейся в Сан-Хосе, Калифорния.


