Электреты в медицине: Использование Электретов в медицине — Арго
Ортопедические электреты — реальная альтернатива эндопротезированию сустава у детей и подростков
ФГБУ «Национальный медицинский исследовательский центр детской травматологии и ортопедии имени Г. И. Турнера» Министерства здравоохранения Российской Федерации начинает проведение комплекса научных исследований в области применения имплантируемых ортопедических электретов ИМПЛЭСО® для лечения дегенеративно-дистрофических заболеваний суставов у детей.
В декабре 2020 года руководители и врачи института встретились со специалистами компании «Медэл» — производителя инновационных имплантируемых ортопедических электретов ИМПЛЭСО®, применяемых в комплексной стратегии лечения дегенеративно-дистрофических заболеваний суставов, для обсуждения программы сотрудничества.
Первый продукт в линейке медицинских электретов компании – имплантируемый ортопедический электрет ИМПЛЭСО® ориентирован на борьбу с дегенеративно-дистрофическими заболеваниями суставов, в частности, для комплексного лечения ювенильного идиопатического аваскулярного некроза головки бедренной кости или, иначе, болезни Легга-Кальве-Пертеса.
Ортопедический электрет – это биосовместимый электростатический эквивалент постоянного магнита, вводимый в субхондральную кость сустава непосредственно к очагу поражения. Имплантируемые электреты обеспечивают правильные режимы электростимуляции, формируя в тканях, повреждённых дегенеративно-дистрофическими изменениями, здоровый электрофизиологический фон и активизируя в них восстановительные процессы остео- и хондрогенеза. В результате возвращается возможность безболезненного движения в полном объеме, а пациент получает шанс вернуться к обычной активной жизни здорового человека. Такая возможность важна для любого человека, но, в особенности — для детей и подростков, проходящих лечение в Национальном медицинском исследовательском центре имени Г. И. Турнера.
До сих пор «золотым стандартом» в лечении артроза считалось эндопротезирование. Например, одним из основных методов лечения подростков с коксартрозом тазобедренного сустава III стадии, который развивается после острого гематогенного остеомиелита, выступает тотальное эндопротезирование сустава.
Ортопедический электрет ИМПЛЭСО® дает возможность врачам побороться за сохранение собственного сустава пациента, пока не пришло время на применение радикальных необратимых мер, и полностью меняет подход к лечению артроза и других дегенеративно-дистрофических заболеваний костно-суставной системы. У пациента появляется выбор, которого раньше просто не было. Иметь такое решение особенно важно, когда речь идет о спасении растущего сустава ребенка.
Стандартная операция по имплантированию ортопедического электрета в сустав является малоинвазивной, ее длительность составляет в среднем 40 минут. Как правило, пациенту разрешается полная нагрузка на прооперированный сустав уже через 24 часа после операции, а специальная реабилитация после проведения простой имплантации ортопедического электрета не требуется. Период восстановления полной двигательной активности сустава будет зависеть от его исходного состояния до операции, объема проведенного хирургического вмешательства, а также смелости и физической подготовки самого пациента.
Программа научных исследований, запланированная Национальным медицинским исследовательским центром имени Г.И. Турнера совместно с компанией «Медэл», является очень важным шагом в создании нового эффективного подхода к лечению не только болезни Пертеса, но и других патологических заболеваний костно-мышечной системы у детей. При этом, не стоит забывать, что дети, находящиеся на лечении в НМИЦ имени Турнера, как правило, имеют заболевания, требующие продолжительного и сложного восстановительного лечения, что создает особую ситуацию в их жизни: детям и подросткам крайне сложно справиться с эмоциональным дискомфортом, связанным с нарушением их привычных моделей поведения и множеством ограничений, которые накладывает болезнь.
Комментарий Алексея Георгиевича Баиндурашвили, президента ФГБУ «Национальный медицинский исследовательский центр детской травматологии и ортопедии имени Г. И. Турнера»:
Баиндурашвили Алексей Георгиевич Президент центра«Мы надеемся, что наше сотрудничество — это начало большого совместного исследования и перспектива развития травматологии и ортопедии детского возраста.
Мы рассчитываем, что применение электретных имплантатов в комплексном лечении детей с патологией тазобедренного сустава позволит в кратчайшие сроки добиться восстановления анатомических соотношений и функции сустава, а также значительно сократить период восстановительного лечения. Достигнутые результаты лечения пациентов с патологией тазобедренного сустава могут служить основой дальнейшего использования и развития технологий применения электретных имплантатов, направленных на восстановление и ремоделирование костной ткани, при различных патологических процессах».
Комментарий Анны Владимировны Гарбузовой, Заместителя генерального директора компании «Медэл»:
«Мы активно внедряем ортопедические электреты в клиническую практику лечения дегенеративно-дистрофических заболеваний суставов в различных регионах России. Врачи травматологи-ортопеды около 160-ти лечебных учреждений в 30 городах нашей страны от Ленинградской до Читинской области прошли обучение новой медицинской технологии.
Более 50 лечебных учреждений уже приступили к самостоятельным операциям.
Мы знаем, какую огромную научную и медицинскую работу проводит Национальный медицинский исследовательский центр имени Г.И. Турнера не только самостоятельно, но так-же в сотрудничестве с разработчиками и производителями инновационных продуктов для детской травматологии и ортопедии. И целью такой работы является необходимость сделать жизнь болеющего ребенка максимально здоровой и полноценной во всех смыслах, а значит — счастливой. Мы будем рады, если с помощью нашего продукта, эта благородная цель станет достижимой».
Компания «Медэл», участник инновационного центра «Сколково», основана в 2013 году для реализации инвестиционного проекта по созданию серийного производства инновационных медицинских изделий. «Медэл» является российским разработчиком и производителем медицинских электретов — нового семейства умных имплантатов, пришедших на замену классическим приборам инвазивной электростимуляции, при-менявшимся ранее в лечении повреждений различных биологических тканей.
Публикации в СМИ здесь.
В газете Вестник здесь.
|
Главная>> Научные статьи>> Электретные покрытия Автор: Олейник П.М. врач-стоматолог ортопед В течение последних 5-7 лет сформировалась и интенсивно развивается новая отрасль медицины, основанная на использовании близкодействующих статических электрических полей для стимулирования позитивных биологических процессов в организме человека. Главной отличительной особенностью практических методов, основанных на этой концепции, является то, что электрические поля создаются не традиционными электротехническими источниками энергии с сетевым или аккумуляторным электропитанием, а функционирующими автономно электретными пленками, нанесенными на имплантаты различного назначения, широко применяемые в медицине. Электрет — это диэлектрик, на поверхности или в объеме которого продолжительное время сохраняются нескомпенсированные электрические заряды, создающие в окружающем электрет пространстве квазистатическое (медленно меняющееся во времени) электрическое поле. Попадая вместе с имплантатом в организм человека, электретная пленка своим полем оказывает дозированное локальное воздействие на поврежденный орган, способствуя его лечению в оптимальных биофизических условиях. В основе этого процесса лежит природный эффект, состоящий в том, что внешнее близкодействующее электрическое поле определенной величины и знака, действуя на клеточном уровне, является катализатором появления здоровых новообразований в живых тканях. Результатом проведенных исследований стал комплекс принципиальных технологий нанесения в вакууме био- и химически инертных, обладающих заданными электретными свойствами, высокой адгезией и чистотой, равномерными свойствами на протяженных подложках сложной пространственной конфигурации пленок пятиокиси тантала на поверхности медицинских имплантатов различного назначения. Выбор электретных покрытий стехиометрического состава Та2О5 объясняется их уникальными свойствами. Так, тантал, уступая по температуре плавления только вольфраму, имеет рекордную химическую стойкость, значительно превосходя по этому параметру такой металл, как золото. Тантал является хорошим проводником и единственным металлом, который не отторгается живой человеческой тканью. Высший окисел тантала Та2О5, является отличным диэлектриком (( ~ 28 … 32), имеет высокие механические свойства, био- и химически инертен. После специальной обработки он приобретает электретные свойства, т.е. способность создавать в течение длительного времени в непосредственной близости от своей поверхности квазистатическое электрическое поле. Изоляция протезов, изготовленных из акриловых пластмасс, тонкими вакуумными пленками пятиокиси тантала позволяет полностью устранить все патологические проявления, обусловленные непереносимостью акрилатов: химико- токсические, аллергические, электрогальванические. Причиной перечисленных патологических проявлений является действие на организм человека продуктов поверхностной эрозии и элиминации компонентов акриловых пластмасс, в состав которых входит метилметакрилат, соединения метакриловой и акриловой кислот, различного рода пластификаторы, замутнители, красители и катализаторы. Попытки устранения явлений непереносимости акриловых пластмасс в стоматологии, связаны с созданием на их поверхности изолирующих барьерных слоев, препятствующих выделению в полость рта продуктов эрозии. Радикальным решением проблемы является нанесение на поверхность протезов покрытий различных материалов. Чаще всего для этой цели используются гальванические покрытия благородных металлов (золото, платина, палладий, серебро) толщиной до 50 мкм. Серьезным недостатком этих покрытий является то, что перечисленные металлы не всегда отвечают требованиям биосовместимости. Кроме того, металлизированная пластмасса приводит к появлению гальванических пар в полости рта. Гальванические покрытия толщиной несколько десятков микрометров изменяют микрорельеф поверхности протезов и нарушают их фиксацию. В идеальном варианте материал покрытия, препятствующего эрозии пластмассы, должен обладать следующими свойствами: — биоинертностью к тканям организма; — высокой прочностью, обеспечивающей целостность покрытия при механических нагрузках, возникающих в процессе эксплуатации; — химической инертностью к агрессивной среде в полости рта и применяемым стоматологическим материалам; — материал покрытия должен обладать диэлектрическими свойствами для исключения возможности образования гальванических пар в полости рта. Этим требованиям в полной мере удовлетворяет пятиокись тантала (Та2О5). Еще одной важной проблемой, которая успешно решается при использовании диэлектрических покрытий пятиокиси тантала, является проблема гальванизма в полости рта. В настоящее время для терапевтического и ортопедического лечения в стоматологии применяется большое количество электропроводящих элементов — изделий из металлов и их сплавов. При наличии во рту металлических включений возможны три вида патологического воздействия на организм человека: химико-токсическое, электрогальваническое (повреждающее действие гальванического тока) и аллергическое. Разработана оригинальная технология нанесения высококачественных диэлектрических пленок пятиокиси тантала, которые полностью изолируют поверхности проводящих изделий от электролита, сводя к нулю опасность возникновения гальванизма в полости рта. Использование имплантатов с электретным покрытием пятиокиси тантала исключает местные воспалительные осложнения, сокращает сроки приживления имплантатов и ускоряет применение дозированных функциональных нагрузок. Одним из наиболее перспективных способов использования электретных покрытий в челюстно-лицевой хирургии является применение дентальных имплантатов с нанесенной на их поверхность электретной пленкой пятиокиси тантала (Ta2O5) с целью оптимизации процессов остеоинтеграции при возмещении дефектов зубных рядов. Таким образом, полученные результаты экспериментального исследования открывают большие перспективы для специалистов в области дентальной имплантологии. Нанесение на поверхность имлантатов электретного пленочного покрытия из пятиокиси тантала способствует наиболее оптимальному протеканию процессов остеоинтеграции, сводит к минимуму риск развития ближайших и отдаленных воспалительных осложнений, позволяет надеяться на благоприятный исход имплантации даже у прогностически пациентов неблагоприятной категории. Литература: 1.Ефашкин Г., Электреты – диэлектрические аналоги магнитов 2.Гороховатский Ю.А., Электретный эффект и его применение 3.Гриднев С.А., Диэлектрики с метастабильной электрической поляризацией Главная>> Научные статьи>> Электретные покрытия |
Биологическое и медицинское применение электретов
-
А. Сассон, Биотехнологии: вызовы и перспективы, 2-е изд., ЮНЕСКО, 1985.
Google Scholar
-
Поддержание культур для биотехнологии и промышленности, Под ред. Дж. К. Хантер-Севера и А. Белт, Academic Press, Нью-Йорк, 1996.
Google Scholar
-
С. Такашима, Электрические свойства биополимеров и мембран, Адам Хиглер, Бристоль и Филадельфия, 1989.

Google Scholar
-
J.C. Fonticella-Camps, A. Volbeda, M. Frey, Trends in Biotechnology , 1996, Vol. 14, нет. 11, с. 417.
Перекрестная ссылка Google Scholar
-
Р. Браун, Тенденции в биотехнологии , 1996, Vol. 14, нет. 9, с. 333.
Перекрестная ссылка КАС Google Scholar
-
J. Berenstein, Electrobiologie, Braunschweig, 1912.
Google Scholar
-
A.L. Hodgkin, B. Katz, J. Physiol. , 1949, Том. 108, с. 37.
КАС Google Scholar
-
A.L. Hodgkin, A.F. Huxley, J. Physiol. , 1952, Том. 117, с. 5.
Google Scholar
-
Инопланетянин Кулин, Биоэлектрический эффект, Минск, Наука и техника, 1980.

Google Scholar
-
В.С. Андреев, В.Г. Попов, Н.В. Дронова, Биотехнология , Москва, 1988, т. 1, с. 4, нет. 1 р. 32.
КАС Google Scholar
-
В.С. Андреев, А.А. Галицин, В.Г. Попов, Биотехнология , Москва, 1990, вып. 1, с. 39.
Google Scholar
-
В.И. Карамушка, З.Р. Ульберг, Т.Г. Грузина, Биотехнология , Москва, 1991, вып. 2, стр. 65.
Google Scholar
-
С. Фогель, Дж.В. Welch, DH Maloney, J. Basic Microbiol. , 1988, Том. 28, нет. 3, с. 147.
Перекрестная ссылка КАС Google Scholar
-
К.М. Ханенбергер, С.Э. Курц, Тенденции в области биотехнологии , 1997, Том.
 15, нет. 1, с. 1.
15, нет. 1, с. 1. Перекрестная ссылка КАС Google Scholar
-
J.C. Fonticella-Camps, A. Volbeda, M. Frey, Trends in Biotechnology , 1996, Vol. 14, нет. 11, с. 409.
Перекрестная ссылка Google Scholar
-
Д. Нери, С. Монтиджани, П.М. Kirkham, Тенденции в биотехнологии , 1996, Vol. 14, нет. 12, с. 465.
Перекрестная ссылка КАС Google Scholar
-
С. Прентис, New Scientist , 1981, Vol. 92, нет. 1275, с.159.
КАС Google Scholar
-
Р.К. Хэддон, А.А. Ламола, Proc. Натл. акад. науч. США , 1985, Том. 82, с. 1874.
Перекрёстная ссылка КАС Google Scholar
-
М.
 Суги, Дж. Мол. Электроника , 1985, Вып. 1, с. 3.
Суги, Дж. Мол. Электроника , 1985, Вып. 1, с. 3. КАС Google Scholar
-
C. Nylander, J. Phys. Э: наук. Иструм. , 1985, Том. 18, с. 736.
Перекрестная ссылка КАС Google Scholar
-
Биосенсоры в аналитической биотехнологии / Под ред. Р. Фрайтаг, Academic Press, Лондон, 1996.
Google Scholar
-
Т.А. Сергеева, Е.А. Рачков, М.И. Терещенко, А.В. Ельская, Абстр. 8 европ. конгр. по биотехнологии , Будапешт, 1997, с. 415.
Google Scholar
-
С. Судзуки, И. Карубе, Заяв. Биохим. биоинж. , 1981, Том. 3, с. 145.
КАС Google Scholar
-
J. Rischpon, D.
 Ivnitski, Enzyme Engineering XIII, Annals of the New York Ac. науч. , 1996, Том. 799, с. 508.
Ivnitski, Enzyme Engineering XIII, Annals of the New York Ac. науч. , 1996, Том. 799, с. 508. Перекрестная ссылка Google Scholar
-
М. Карп, С. Тауриайнен, М. Вирта, Abstr. 8 европ. конгр. по биотехнологии , Будапешт, 1997, с. 416.
Google Scholar
-
А.Ф. Лоуренс, Р.Р. Бирдж, в кн.: Нелинейная электродинамика в биологических системах, под ред. В. Р. Адей и А. Ф. Лоуренс, Plenum Press, Нью-Йорк и Лондон, 1984, с. 207.
Перекрёстная ссылка Google Scholar
-
Д. Де Во, Квантово-механическое туннелирование в биологических системах, 2-е изд., University Press, Cambridge, 1984.
Google Scholar
-
Ю. Мацура, Т. Такано, Р.Э. Дикерсон, J. Mol.
 биои. , 1982, Том. 156, с. 384.
биои. , 1982, Том. 156, с. 384. Перекрестная ссылка Google Scholar
-
Карпов, В.А. Лялин, А.А. Свицов, Биотехнология , Москва, 1989, т. 1, с. 5, нет. 3, с. 260.
Google Scholar
-
В.М. Коликов, А.Б. Орешков, Н.В. Катушкина и др., Биотехнология , Москва,1990, вып. 6, с. 47.
Google Scholar
-
С.А. Щукин, А.В. Гаврюшкин, Ю.Н. Брезгунов и др., Электрофорез , 1986, т. 1, с. 7, с. 572.
Перекрестная ссылка Google Scholar
-
Панасюк Т., Пилацкий С., Нигматуллин Р., Ельская А., Абстр. 8 европ. конгр. по биотехнологии , Будапешт, 1997, с. 414.
Google Scholar
-
К.
 Мацумото, В. Асад, Abstr. 8 европ. конгр. по биотехнологии , Будапешт, 1997, с. 417.
Мацумото, В. Асад, Abstr. 8 европ. конгр. по биотехнологии , Будапешт, 1997, с. 417. Google Scholar
-
X. Wang, HG Spencer, Trends in Polymer Science , 1997, Том. 5, нет. 2, с. 38.
КАС Google Scholar
-
Б.И. Ческис, Г.Б. Шебека, А.Б. Паулуконис, Д.А. Казлаускас, Биотехнология , Москва, 1990, №1, с. 33.
Google Scholar
-
E. Kokufuta, W. Matsumoto, I. Nakamura, J. Appl. Полим. науч. , 1982, Том. 27, с. 2503.
Перекрестная ссылка КАС Google Scholar
-
Л.В. Дмитренко, Г.А. Яскович, Г.Е. Елкин и др., Биотехнология , Москва, 1990, вып. 2, с. 26.
Google Scholar
-
Л.
 В. Карпунина, В.Е. Никитина, Н.А. Воротилова и др., Биотехнология , Москва, 1989, т. 1, с. 5, нет. 2, с. 208.
В. Карпунина, В.Е. Никитина, Н.А. Воротилова и др., Биотехнология , Москва, 1989, т. 1, с. 5, нет. 2, с. 208. КАС Google Scholar
-
Г.Н. Нировская, П.И. Гвоздяк, И.И. Шамолина и др., Биотехнология , Москва, 1990, вып. 2, с. 53.
Google Scholar
-
Ю.Е. Кирш, И.Ю. Галаев, Т.М. Карапутадзе и др., Биотехнология , Москва, 1987, т. 1, с. 3, нет. 2, с. 184.
КАС Google Scholar
-
Л.В. Свердлов, А.И. Курмаева, В.П. Барабанов, Д.Г. Победимский, Биотехнология , Москва, 1989, т. 1, с. 5, нет. 1, с. 21.
КАС Google Scholar
-
M. Kumakura, I. Kaetsu, Biomass , 1983, Vol. 3, нет. 2, с. 199.
Перекрестная ссылка КАС Google Scholar
-
Н.
 В. Иванова, А.А. Шишко, В.Г. Горохова и др., ДАН , Москва, 1995, т. 1, с. 343, нет. 4, с. 486.
В. Иванова, А.А. Шишко, В.Г. Горохова и др., ДАН , Москва, 1995, т. 1, с. 343, нет. 4, с. 486. КАС Google Scholar
-
С.Д. Варфоломеев, Е.П. Калязин, С.В. Калюжный и др., Биотехнология , Москва, 1989, т. 1, с. 5, №1, с. 54.
КАС Google Scholar
-
П. Кристон, Дж. Э. Мерфи, В.Ф. Суэйн, Proc. Натл. акад. науч. США , 1987, Том. 84, нет. 12, с. 3962.
Перекрестная ссылка Google Scholar
-
И.Ю. Галаев, Russian Chemical Reviews , 1995, Том. 65, нет. 5, с. 505.
Google Scholar
-
Т. Танака, И. Нисио, С.-Т. Sun, S. Ueno-Nishio, Science , 1982, Vol. 218, с. 467.
Перекрестная ссылка КАС Google Scholar
-
С.
 Маскареньяс, Анн. Нью-Йоркская академия. науч. , 1974, Том. 238, с. 36.
Маскареньяс, Анн. Нью-Йоркская академия. науч. , 1974, Том. 238, с. 36. Перекрёстная ссылка КАС Google Scholar
-
З.Б. Фриденберг, К.Т. Bringhton, J. Хирург суставов костей. [Am] , 1966, Vol. 48, с. 915.
КАС Google Scholar
-
З.Б. Friedenberg, HG Smith, Clin. Ортоп. , 1969, Том. 63, с. 222.
КАС Google Scholar
-
М.Х. Шамос, Л.С. Лавин, М.И. Шараос, Nature , 1963, Vol. 197, с. 81.
перекрестная ссылка КАС Google Scholar
-
E. Fukada, I. Yasuda, J. Phys. соц. Япония. , 1957, вып. 10, с. 1158.
Google Scholar
-
С.
 Р. Поллак, Ортоп. клин. Север. Являюсь. , 1984, Том. 15, с. 3.
Р. Поллак, Ортоп. клин. Север. Являюсь. , 1984, Том. 15, с. 3. КАС Google Scholar
-
П.А. Reveil, Патология кости, Springer-Verlag, Берлин, 1986.
Перекрестная ссылка Google Scholar
-
J. Черный, Ортоп. клин. Север. Являюсь. , 1984, Том. 15, с. 15.
КАС Google Scholar
-
Н.В. Корнилов, А.И. Анисимов, А.Ю. Каныкин, Абстр. Ист междунар. Конг. «Слабые и сверхслабые поля и излучения в биологии и медицине» , Санкт-Петербург, 1997, с. 72.
Google Scholar
-
М.С. Моргунов, В.П. Хомутов, И.М. Соколова, , учеб. 8-й междунар. Симп. на Электретах , Париж, 1994, с. 863.
Google Scholar
-
Патент СССР, 1454482, A61N, 1989 г.
 Стимулятор остеорепарации.
Стимулятор остеорепарации. Google Scholar
-
Патент СССР, 1122328, А61Н, 1984 г. Устройство для остеосинтеза.
Google Scholar
-
Г.В. Гастингс, Proc. 6-й междунар. конф. Полим. Мед. и сург. , 1989, с. 1/1.
Google Scholar
-
Д.Ф. Уильямс, Определения в биоматериалах, Progress in Biomedical Engineering , Vol. 4, Эльзевир, 1987.
Google Scholar
-
E.W. Morscher, Endoprothetik, Springer-Verlag, Berlin, 1995.
CrossRef Google Scholar
-
Б.Д. Ratner, Trends in Polymer Science , 1994, Vol. 2, нет. 12, с. 402.
КАС Google Scholar
-
F.
 Simon, G. Hermel, D. Lunkwitz et al., Proc. 5-й Дрезденский Полим. Обсуждать. Полим. мед. , Кенигштайн, Макромоль. Симп. , 1996, Том. 103, с. 243.
Simon, G. Hermel, D. Lunkwitz et al., Proc. 5-й Дрезденский Полим. Обсуждать. Полим. мед. , Кенигштайн, Макромоль. Симп. , 1996, Том. 103, с. 243. КАС Google Scholar
-
Электреты, изд. Г.М. Сесслер, 2-е изд., Springer-Verlag, Берлин, Гейдельберг, Нью-Йорк, 1987 ( Top. Appl. Phys. , Vol. 33).
Google Scholar
-
K. James, J. Kohn, Trends in Polymer Science , 1996, Vol. 4, нет. 12, с. 394.
КАС Google Scholar
-
М. Дж. Фист, С. Манро, Р. В. Ричардс, Полимерные поверхности и интерфейсы, John Wiley & Sons, Нью-Йорк, 1993.
Google Scholar
-
HJ Taunton, C. Toprakocioglu, LJ Fettersh, J. Klein, Nature , 1988, Vol. 332, с.
 712.
712. Перекрёстная ссылка КАС Google Scholar
-
М. Амиджи, К. Парк, Дж. Биоматер. наук, полим. Эд. , 1993, Том. 4, с. 217.
Перекрёстная ссылка КАС Google Scholar
-
Ю. Нагасаки, К. Катаока, Тенденции в науке о полимерах , 1996, Том. 4, нет. 2, с. 59.
КАС Google Scholar
-
Специальные полимеры для электроники и оптоэлектроники / Под ред. Дж.А. Чилтон и М.Т. Гуси, Шэпман и Хилл, 1995.
Google Scholar
-
Дж. Р. Купер, Д. Доусон, Дж. Фишер, Wear , 1993, Vol. 162-164, с. 378.
Перекрестная ссылка КАС Google Scholar
-
Л.С. Пинчур, Э.
 А. Цветкова, В.И. Николаев, Журнал трения и износа , 1995, Вып. 16, нет. 3, с. 79.
А. Цветкова, В.И. Николаев, Журнал трения и износа , 1995, Вып. 16, нет. 3, с. 79. Google Scholar
-
Д. Панцера, Т.Б. Кирк, Р.В. Анамалая, проц. Междунар. конгр. трибологии AUSTRIB’94 , Перт, Австралия, 1994, с. 407.
Google Scholar
-
Н. Дан, Р. Йерушалми-Розен, Тенденции в науке о полимерах , 1997, Том. 5, нет. 2, с. 46.
КАС Google Scholar
-
П.А. Revell, Патология костей, Springer-Verlag, Berlin, 1986.
CrossRef Google Scholar
-
С.Р. Ермаков, Механика композиционных материалов , Латв. акад. наук, 1992, вып. 4, с. 539.
Google Scholar
-
A.
 Zaffaroni, in: Biomedical anddental Applications of Polymer, Plenum Press, New York — London, 1981, p. 293.
Zaffaroni, in: Biomedical anddental Applications of Polymer, Plenum Press, New York — London, 1981, p. 293. Google Scholar
-
П. Артурсон, Т. Лааксо, П. Эдман, J. Pharm. наук , 1983, Вып. 72, с. 1415.
Перекрестная ссылка КАС Google Scholar
-
H. Struyker, Trends Pharm. науч. , 1982, Том. 3, с. 162.
Перекрестная ссылка Google Scholar
-
M. Brownlee, A. Cerami, Science , 1979, Vol. 206, с. 1190.
Перекрестная ссылка КАС Google Scholar
-
С. Сато, С.Ю. Чжон, Дж. К. МакРи, С.В. Ким, Контролируемый выпуск , 1984, Vol. 1, с. 67.
Перекрёстная ссылка КАС Google Scholar
-
К.
 Э. Гонсалвес, П.М. Мунгара, Тенденции в науке о полимерах , 1996, Том. 4, нет. 1, с. 25.
Э. Гонсалвес, П.М. Мунгара, Тенденции в науке о полимерах , 1996, Том. 4, нет. 1, с. 25. КАС Google Scholar
-
Плате Н.А., Васильев А.Е. Физиология активных полимеров, Москва, Химия, 1986.
Google Scholar
-
Патент США, 5336505, A61K, 1994, Биодеструктивные полимеры для контролируемого высвобождения терапевтических средств.
Google Scholar
-
Дж. Л. Вест, Тенденции в науке о полимерах , 1996, Vol. 4, нет. 7, с. 206.
КАС Google Scholar
-
J.F. Künzler, Trends in Polymer Science , 1996, Vol. 4, нет. 2, с. 52.
Google Scholar
-
Т.Г. Лазарева, И.А.
 Ильющенко, И.Ф. Алимов, High-Molec. Комп. , Москва, 1994, вып. 36А, нет. 9, с. 1481.
Ильющенко, И.Ф. Алимов, High-Molec. Комп. , Москва, 1994, вып. 36А, нет. 9, с. 1481. Google Scholar
-
З.Е. Браун, Дж.В. Сатклифф, П.Д. Pulsinelli, Биохимия , 1983, Vol. 22, с. 2914.
Перекрестная ссылка КАС Google Scholar
-
М.Ф. Коломбо, Р. Санчес, Биофизическая химия , 1990, Vol. 36, с. 33.
Перекрёстная ссылка КАС Google Scholar
-
М.Г. Brudelli, R. Capeletti, Losi S. et al., Proc. 8-й междунар. Симп. на Электретах, Париж , 1994, с. 869.
Google Scholar
-
Патент СССР, 1834655, 61, 1993 г. Устройство для сегментарно-рефлекторной терапии.
Google Scholar
-
J.
 L. West, Trends in Polymer Science , 1996, Vol. 4, нет. 7, с. 206.
L. West, Trends in Polymer Science , 1996, Vol. 4, нет. 7, с. 206. КАС Google Scholar
Скачать ссылки
Влияние технологии электретного покрытия на тромбогенность коронарного стента
. 2022 17 февраля; 33 (2): 312-319.
дои: 10.1080/09537104.2021.1912313. Epub 2021 15 апр.
М Урой Зафар 1 , Хосе Хавьер Браво-Кордеро 2 , Сержи Торрамаде-Мойкс 3 , Хинес Эсколар 1 3 , Дидак Херес-Дольц 3 , Эли I Лев 4 , Хуан Хосе Бадимон 1
Принадлежности
- 1 Медицинский факультет, Отдел исследования атеротромбоза (ATRU), Институт сердечно-сосудистых заболеваний, Медицинская школа Икана на горе Синай, Нью-Йорк, США.

- 2 Отделение гематологии и онкологии, медицинский факультет, Институт рака Тиша, Медицинская школа Икана на горе Синай, Нью-Йорк, США.
- 3 Отделение гемостаза и коагуляции, отделение патологии, больница Clinic De Barcelona, Барселона, Испания.
- 4 Университетская больница Ассута Ашдод, Ашдод, и факультет медицинских наук Университета Бен-Гуриона, Израиль.
- PMID: 33856288
- PMCID: PMC8759110
- DOI: 10.1080/09537104.2021.1912313
Бесплатная статья ЧВК
М. Урой Зафар и др.
Тромбоциты.
.
Урой Зафар и др.
Тромбоциты.
.
Бесплатная статья ЧВК
. 2022 17 февраля; 33 (2): 312-319.
дои: 10.1080/09537104.2021.1912313. Epub 2021 15 апр.
Авторы
М Урой Зафар 1 , Хосе Хавьер Браво-Кордеро 2 , Сержи Торрамаде-Мойкс 3 , Хинес Эсколар 1 3 , Дидак Херес-Дольц 3 , Эли I Лев 4 , Хуан Хосе Бадимон 1
Принадлежности
- 1 Медицинский факультет, Отдел исследования атеротромбоза (ATRU), Институт сердечно-сосудистых заболеваний, Медицинская школа Икана на горе Синай, Нью-Йорк, США.

- 2 Отделение гематологии и онкологии, медицинский факультет, Институт рака Тиша, Медицинская школа Икана на горе Синай, Нью-Йорк, США.
- 3 Отделение гемостаза и коагуляции, отделение патологии, больница Clinic De Barcelona, Барселона, Испания.
- 4 Университетская больница Ассута Ашдод, Ашдод, и факультет медицинских наук Университета Бен-Гуриона, Израиль.
- PMID: 33856288
- PMCID: PMC8759110
- DOI: 10.1080/09537104.2021.1912313
Абстрактный
Тромбоз стента (ST) является катастрофическим событием, и усилия по снижению его частоты путем изменения взаимодействия кровь-стент предпринимаются давно. Новая технология электретного покрытия, создающая долговременный отрицательный заряд на поверхности стента, может сделать их внутренне устойчивыми к тромбообразованию. Мы оценили тромбогенность стентов, используя модель кольцевой перфузии с помощью конфокальной микроскопии, и определили эффективность технологии электретного покрытия для придания тромборезистентных свойств стандартным стентам. Используя кольцевую перфузионную камеру, незащищенный металлический стент (BMS), стандартный непокрытый DES (DES) и DES с электретным покрытием (e-DES) подвергали воздействию крови человека в условиях артериального кровотока. Отложения фибриногена и тромбоцитов на поверхности стента анализировали с помощью иммунофлуоресцентного окрашивания и конфокальной микроскопии. Покрытие поверхности фибриногеном и тромбоцитами, а также размер отложений/агрегатов количественно определяли с помощью компьютерного морфометрического анализа. Экспериментальная методология дала последовательные, поддающиеся количественной оценке результаты.
Новая технология электретного покрытия, создающая долговременный отрицательный заряд на поверхности стента, может сделать их внутренне устойчивыми к тромбообразованию. Мы оценили тромбогенность стентов, используя модель кольцевой перфузии с помощью конфокальной микроскопии, и определили эффективность технологии электретного покрытия для придания тромборезистентных свойств стандартным стентам. Используя кольцевую перфузионную камеру, незащищенный металлический стент (BMS), стандартный непокрытый DES (DES) и DES с электретным покрытием (e-DES) подвергали воздействию крови человека в условиях артериального кровотока. Отложения фибриногена и тромбоцитов на поверхности стента анализировали с помощью иммунофлуоресцентного окрашивания и конфокальной микроскопии. Покрытие поверхности фибриногеном и тромбоцитами, а также размер отложений/агрегатов количественно определяли с помощью компьютерного морфометрического анализа. Экспериментальная методология дала последовательные, поддающиеся количественной оценке результаты. Площадь поверхности стента, покрытая фибриногеном и тромбоцитами, и средний размер отложений/агрегатов были самыми низкими для e-DES и самыми высокими для BMS, с DES в середине. Размер отложений фибриногена не отличался между стентами. Методология испытаний, использованная в нашем исследовании, успешно продемонстрировала, что электретное покрытие придает стентам для СЛП значительные антитромботические свойства. Эти результаты требуют подтверждения в более крупном исследовании.
Площадь поверхности стента, покрытая фибриногеном и тромбоцитами, и средний размер отложений/агрегатов были самыми низкими для e-DES и самыми высокими для BMS, с DES в середине. Размер отложений фибриногена не отличался между стентами. Методология испытаний, использованная в нашем исследовании, успешно продемонстрировала, что электретное покрытие придает стентам для СЛП значительные антитромботические свойства. Эти результаты требуют подтверждения в более крупном исследовании.
Ключевые слова: Электрет; тромбоцит; стент; стентовое покрытие; тромбоз.
Заявление о конфликте интересов
Цифры
Рисунок 1:
Система кольцевой перфузионной камеры…
Рисунок 1:
Система кольцевой перфузионной камеры. Фотография кольцевой камеры со стентом…
Фотография кольцевой камеры со стентом…
Система кольцевой перфузионной камеры. Фотография кольцевой камеры со стентом, размещенным на внутренней стержневой конструкции (А). Графическая иллюстрация модели перфузии (B).
Рисунок 2.
Репрезентативные изображения конфокальной микроскопии…
Рисунок 2.
Конфокальные микроскопические репрезентативные изображения исследуемого стента. Панели слева показывают фибриноген…
Фигура 2. Конфокальные микроскопические репрезентативные изображения исследуемого стента. На панелях слева показано отложение фибриногена, а справа показано отложение тромбоцитов на голом металлическом стенте (A), стандартном/непокрытом стенте с лекарственным покрытием (B) и стенте с электретным покрытием (C).
Рисунок 3.
Блок-схема фибриногена и…
Рисунок 3.
Коробчатая диаграмма отложений фибриногена и тромбоцитов. Коробчатые диаграммы, суммирующие покрытие поверхности…
Рисунок 3. Коробчатая диаграмма отложений фибриногена и тромбоцитов. Коробчатые диаграммы, суммирующие покрытие поверхности каждого типа стента фибриногеном и тромбоцитами. Отложение фибриногена (левая панель) на стандартном/непокрытом стенте с лекарственным покрытием (СЛП) было значительно ниже, чем на непокрытом металлическом стенте (СМС), а на покрытом электретом стенте с лекарственным покрытием (e-DES) было значительно ниже, чем как на СЛП, так и на BMS. . Аналогичные результаты были отмечены для отложения тромбоцитов (правая панель), но различия были статистически значимыми только между e-DES и BMS.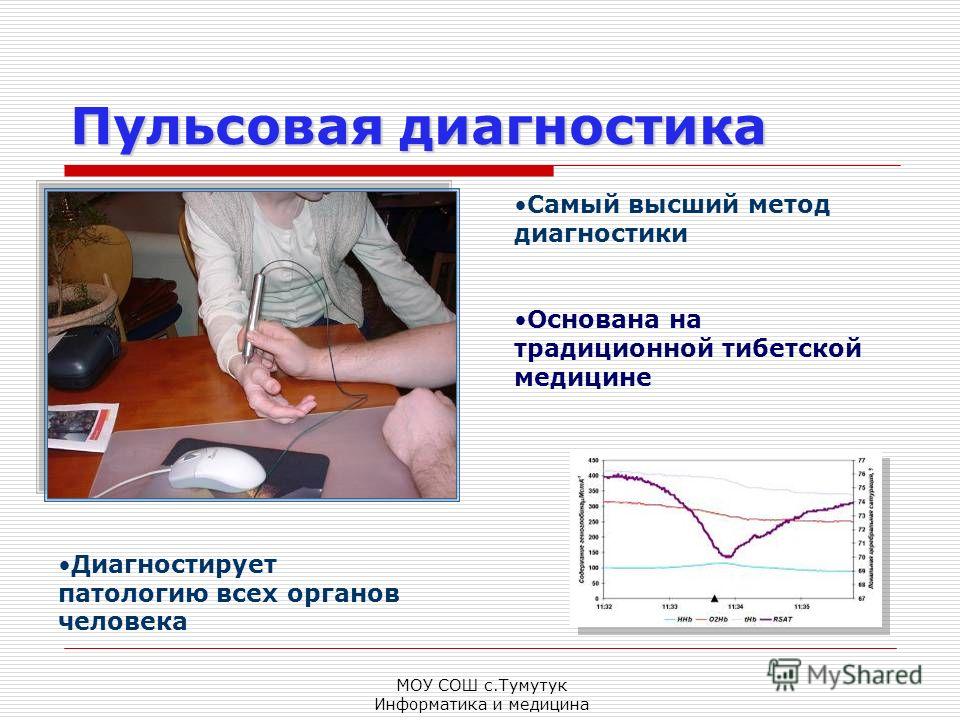
Рисунок 4.
Блок-схема фибриногена и…
Рисунок 4.
Коробчатая диаграмма размеров фибриногена и тромбоцитов. Коробчатые участки размером…
Рисунок 4. Коробчатая диаграмма размера фибриногена и тромбоцитарного агрегата. Коробчатые диаграммы размера агрегатов фибриногена и тромбоцитов, сформированных на трех типах исследуемых стентов. Никаких различий в размере агрегатов фибриногена не наблюдалось (левая панель). Средний размер агрегатов тромбоцитов (правая панель) на стенте с лекарственным покрытием (DES) был меньше, чем на стенте из чистого металла (BMS), а на стенте с электретным покрытием (e-DES) меньше, чем на DES и BMS. Однако эти различия достигли статистической значимости только между e-DES и BMS.
См. это изображение и информацию об авторских правах в PMC
Похожие статьи
-
Сравнение нового поколения стентов с лекарственным покрытием с голыми металлическими стентами у пациентов с острым инфарктом миокарда с подъемом сегмента ST: объединенный анализ ОБСЛЕДОВАНИЯ (клиническая оценка стента Xience-V при остром инфаркте миокарда) и COMFORTABLE-AMI (сравнение биолимуса, элюируемого из эродируемого покрытия стентов голыми металлическими стентами при остром инфаркте миокарда с подъемом сегмента ST).
Сабате М., Рабер Л., Хег Д., Бругалетта С., Келбек Х., Секье А., Остойич М., Иньигес А., Тюллер Д., Серра А., Баумбах А., фон Биргелен С., Эрнандес-Антолин Р., Роффи М., Майнар В., Валгимигли М., Серруйс П.В., Юни П., Виндекер С. Сабате М. и др. JACC Cardiovasc Interv. 2014 Январь;7(1):55-63. doi: 10.1016/j.jcin.2013.07.
 012. Epub 2013 11 декабря.
JACC Cardiovasc Interv. 2014.
PMID: 24332419
012. Epub 2013 11 декабря.
JACC Cardiovasc Interv. 2014.
PMID: 24332419 -
Внутрисосудистое ультразвуковое исследование оценивало неполное прилегание стента и его разрушение при тромбозе стента после лечения голым металлом по сравнению со стентом с лекарственным покрытием в Северном внутрисосудистом ультразвуковом исследовании (NIVUS).
Косонен П., Викман С., Дженсен Л.О., Лассен Дж.Ф., Харнек Дж., Оливекрона Г.К., Эрглис А., Фоссум Э., Ниемела М., Кервинен К., Юлитало А., Пиетила М., Аароэ Дж., Келлерт Т., Саунамяки К., Тайссен П., Хеллстен Л., Туесен Л., Ниемела К. Косонен П. и др. Int J Кардиол. 2013 г., 30 сентября; 168(2):1010-6. doi: 10.1016/j.ijcard.2012.10.033. Epub 2012 17 ноября. Int J Кардиол. 2013. PMID: 23164593 Клиническое испытание.
-
Риск тромбоза стента среди голых металлических стентов, стентов с лекарственным покрытием первого поколения и стентов с лекарственным покрытием второго поколения: результаты регистра 18 334 пациентов.

Тада Т., Бирн Р.А., Симунович И., Кинг Л.А., Кассезе С., Йонер М., Фузаро М., Шнайдер С., Шульц С., Ибрагим Т., Отт И., Массберг С., Лаугвиц К.Л., Кастрати А. Тада Т. и др. JACC Cardiovasc Interv. 2013 Декабрь; 6 (12): 1267-74. doi: 10.1016/j.jcin.2013.06.015. JACC Cardiovasc Interv. 2013. PMID: 24355117
-
Роль сосудистой визуализации в проведении рутинных чрескожных коронарных вмешательств: метаанализ испытаний стентов из чистого металла и стентов с лекарственным покрытием.
Алсидави С., Эффат М., Рахман С., Абдалла М., Лисар М. Альсидави С. и др. Кардиоваск Ther. 2015 дек;33(6):360-6. дои: 10.1111/1755-5922.12160. Кардиоваск Ther. 2015. PMID: 26363283 Обзор.
-
Ангиопластика.
Чабра Л.





 При наличии непереносимости акриловых протезов больные предъявляют жалобы на жжение слизистой оболочки полости рта, жжение и пощипывание языка, отечность слизистой, сухость во рту. Объективно явления непереносимости могут сопровождаться гиперемией (ограниченной пределами протезного ложа или разлитой), отеком слизистой оболочки губ, щек, языка, петехиальными кровоизлияниями, наличием папул и эрозий. Наряду с местными реакциями, возможны общие проявления непереносимости в виде ринита, крапивницы, дерматита, конъюнктивита, реакции со стороны центральной нервной системы (бессонница, головокружение), обострение хронических заболеваний. Общие проявления могут сочетаться с местными симптомами или реализовываться изолированно. Постоянное выделение из протезов малых доз токсических веществ приводит к хронической интоксикации организма.
При наличии непереносимости акриловых протезов больные предъявляют жалобы на жжение слизистой оболочки полости рта, жжение и пощипывание языка, отечность слизистой, сухость во рту. Объективно явления непереносимости могут сопровождаться гиперемией (ограниченной пределами протезного ложа или разлитой), отеком слизистой оболочки губ, щек, языка, петехиальными кровоизлияниями, наличием папул и эрозий. Наряду с местными реакциями, возможны общие проявления непереносимости в виде ринита, крапивницы, дерматита, конъюнктивита, реакции со стороны центральной нервной системы (бессонница, головокружение), обострение хронических заболеваний. Общие проявления могут сочетаться с местными симптомами или реализовываться изолированно. Постоянное выделение из протезов малых доз токсических веществ приводит к хронической интоксикации организма. Эрозия пластмассы происходит под действием ряда причин, в числе которых — неполное связывание мономера в процессе полимеризации, селективная экстракция компонентов, химические и механические нагрузки, возникающие в процессе эксплуатации протеза.
Эрозия пластмассы происходит под действием ряда причин, в числе которых — неполное связывание мономера в процессе полимеризации, селективная экстракция компонентов, химические и механические нагрузки, возникающие в процессе эксплуатации протеза.
 Всегда, когда проводник и электролит находятся в контакте, возникает электрический эффект, который заключается в стремлении металла отдать положительно заряженные ионы в раствор, сохранив принадлежащие ему электроны. Вследствие этого на проводнике, погруженном в электролит (слюну), возникает электрический заряд, а между разнородными проводниками — разность электрохимических потенциалов, т.е. образуется гальванический элемент. Возникающие при этом токи электронов и ионов приводят к серьезным заболеваниям.
Всегда, когда проводник и электролит находятся в контакте, возникает электрический эффект, который заключается в стремлении металла отдать положительно заряженные ионы в раствор, сохранив принадлежащие ему электроны. Вследствие этого на проводнике, погруженном в электролит (слюну), возникает электрический заряд, а между разнородными проводниками — разность электрохимических потенциалов, т.е. образуется гальванический элемент. Возникающие при этом токи электронов и ионов приводят к серьезным заболеваниям. В настоящее время предпринимаются попытки изучения биоэлектрических процессов в костной ткани и ее электретных свойств. Это позволяет использовать различные материалы с электретными свойствами для направленного влияния на процессы репаративного остеогенеза, что является актуальным как при лечении больных с травматическими повреждениями костей лицевого черепа, так и при дентальной имплантации.
В настоящее время предпринимаются попытки изучения биоэлектрических процессов в костной ткани и ее электретных свойств. Это позволяет использовать различные материалы с электретными свойствами для направленного влияния на процессы репаративного остеогенеза, что является актуальным как при лечении больных с травматическими повреждениями костей лицевого черепа, так и при дентальной имплантации.