Камптокормия: Камптокормия при болезни Паркинсона
Камптокормия при болезни Паркинсона
Одной из наиболее трудных проблем, с которой сталкивается врач-невролог при лечении пациентов с болезнью Паркинсона (БП), являются нарушения позы. Среди них можно выделить такие проявления, как антероколлис (синдром «свисающей головы»), наклон туловища в сторону (синдром «пизанской башни») и камптокормия (синдром «согнутой спины»), которые приводят к инвалидности пациентов и плохо поддаются противопаркинсонической терапии. Две первые формы чаще встречаются при мультисистемной атрофии, в то время как камптокормия (КК) более типична для БП [6].
КК представляет собой непроизвольный наклон туловища вперед (сгибание в грудопоясничном отделе позвоночника), усиливающийся при длительном стоянии и ходьбе, но исчезающий или резко уменьшающийся в положении лежа [27]. Термин «камптокормия» впервые ввел в медицинскую литературу В. Brodiе в 1837 г. Это название произошло от греческих слов «согнуть» и «ствол» [13]. В 1817 г. Дж. Паркинсон в своей книге «Эссе о дрожательном параличе» отметил склонность к наклону туловища вперед как один из признаков БП [22].
В современной литературе связь КК с БП описал R. Djaldetti [13]. Первоначально КК считалась редким феноменом, но в последнее время сообщения о данном феномене стали встречаться значительно чаще [27]. Результаты современных исследований [3, 39] определяют распространенность КК среди пациентов с БП показателем от 3 до 17%.
Причины развития КК у пациентов с БП недостаточно изучены [5, 12, 15, 23, 24]. Тот факт, что проявления КК уменьшаются в горизонтальном положении, исключает дегенеративный спондилоартроз как возможную причину данного феномена [27]. Изначально КК считали крайним вариантом характерной для БП сгорбленной позы, возникающей вследствие ригидности мышц туловища [13].
Частое сочетание КК с мышечными изменениями послужило основанием к появлению гипотезы о периферическом механизме ее формирования. При этом КК, ассоциированная с БП, объясняется специфической миопатией антигравитационных мышц, выпрямляющих туловище, с субклиническим вовлечением мышц тазового и плечевого пояса [17]. Эту концепцию подтверждают клинические наблюдения (слабость паравертебральных мышц) и электрофизиологические исследования (выявление полифазных потенциалов, позитивных острых волн при ЭМГ) [26, 35].
При этом КК, ассоциированная с БП, объясняется специфической миопатией антигравитационных мышц, выпрямляющих туловище, с субклиническим вовлечением мышц тазового и плечевого пояса [17]. Эту концепцию подтверждают клинические наблюдения (слабость паравертебральных мышц) и электрофизиологические исследования (выявление полифазных потенциалов, позитивных острых волн при ЭМГ) [26, 35].
В случаях длительного течения БП с КК при морфологическом исследовании биоптата мышц обнаруживают воспалительные или другие неспецифические миопатические изменения [15, 33]. Магнитно-резонансная томография (МРТ) паравертебральных мышц также может выявлять признаки миопатии [26]. Кроме того, описаны случаи снижения тяжести КК на фоне системной терапии стероидами [43].
В ряде исследований [2, 10, 13, 36] описано возникновение или усиление КК на фоне терапии леводопой или агонистами дофаминовых рецепторов.
КК при БП обычно появляется по мере прогрессирования заболевания. По данным некоторых авторов, пациенты с КК характеризуются более старшим возрастом, большей длительностью заболевания, более выраженной степенью тяжести БП, большей продолжительностью терапии препаратами леводопы, большей суточной дозой леводопы, ранним присоединением аксиальных симптомов и более частой сопутствующей деменцией [3, 13]. Другие авторы [39], напротив, не находят корреляции между степенью сгибания туловища и возрастом, длительностью БП, стадией заболевания, а также продолжительностью лечения и дозами леводопы. В некоторых исследованиях [39] у пациентов с КК выявлены более частые случаи предшествующих хирургических вмешательств на позвоночнике (ламинэктомии по поводу грыж пояснично-крестцового отдела позвоночника и др.).
Другие авторы [39], напротив, не находят корреляции между степенью сгибания туловища и возрастом, длительностью БП, стадией заболевания, а также продолжительностью лечения и дозами леводопы. В некоторых исследованиях [39] у пациентов с КК выявлены более частые случаи предшествующих хирургических вмешательств на позвоночнике (ламинэктомии по поводу грыж пояснично-крестцового отдела позвоночника и др.).
Для клинической оценки степени выраженности КК используют гониометрическое измерение степени тораколюмбальной флексии, рассчитываемой как угол между вертикальной плоскостью и плоскостью, проходящей через край акромиона. Как правило, КК считают переднюю флексию с углом наклона более 45° [24, 39].
N. Margraf и соавт. [26] разработали шкалу, которая состоит из 5 разделов, позволяющих оценить в баллах величину угла наклона, условия возникновения, время в течение дня, когда у пациента присутствует КК, выраженность боли в спине и степень инвалидизации. В ней учитываются также длительность и течение заболевания, методы коррекции КК, наличие зависимости от приема дофаминергических средств.
Диагноз КК ставят на основании клинических данных. МРТ головного мозга и позвоночника, электронейромиографию (ЭНМГ) и мышечную биопсию используют для исключения вторичной КК при других заболеваниях [9, 15, 26]. Для дифференциальной диагностики КК важны также определение СОЭ, С-реактивного белка, электролитов (кальций), креатинфосфокиназы (КФК), пирувата и лактата (для исключения миозитов и митохондриальной патологии) [35]. По данным ЭМГ поясничных и грудных паравертебральных мышц могут отмечаться фибрилляции, положительные острые волны и патологические разряды высокой частоты [33]. При гистологическом исследовании паравертебральных мышц при КК выявляются фиброз и наличие жировой ткани с дегенеративными волокнами [24].
Цель настоящего исследования — изучение клинических особенностей КК при БП.
Материал и методы
Исследовали 70 пациентов с БП, имевших КК. Средний возраст пациентов был 68,9±7,8 года. Стадия по Хену и Яру составила 3,4±0,7 балла; средняя продолжительность заболевания — 9,9±5,6 года.
Контрольную группу составили 20 пациентов с БП без КК. Она соответствовала основной по возрасту, полу, продолжительности заболевания и степени тяжести.
Для оценки степени тяжести БП использовалась шкала Хена и Яра в модификации Линдвалла [20]; для оценки выраженности основных симптомов БП — унифицированная шкала БП (Unifed Parkinsons Disease Rating Scale — UPDRS) [14]; для оценки постуральной неустойчивости — шкала Берга [7], шкала нарушений ходьбы и равновесия (Gait and Balance Scale) [37]; для оценки повседневной активности больных — шкала Schwab et England [31]; для оценки качества жизни больных БП — шкала PDQ-39 [29]; для оценки степени выраженности КК и степени выраженности болевого синдрома — шкала КК [26]; для оценки влияния дофаминергических препаратов на выраженность КК использовался дневник пациента [18].
Результаты и обсуждение
У пациентов с КК отмечена достоверно более низкая оценка по шкале повседневной активности Schwab and England (68,3±19,5 балла в основной группе и 72,0±15,8 балла в контрольной группе) и более низкое качество жизни (оценка по PDQ-39 — 106,0±21,3 балла в основной группе и 100,1±25,3 балла в контрольной, p<0,05). У пациентов с КК была также более выражена постуральная неустойчивость. Падения наблюдались у 29 (41,4%) пациентов. Только у 18 (25,7%) больных выявлена четкая связь появления КК с началом дофаминергической терапии. У 27 (38,6%) больных отмечалось ухудшение позы в периоде «выключения», у 8 (11,4%) пациентов — в утренние часы после ночного перерыва в приеме препаратов.
У пациентов с КК была также более выражена постуральная неустойчивость. Падения наблюдались у 29 (41,4%) пациентов. Только у 18 (25,7%) больных выявлена четкая связь появления КК с началом дофаминергической терапии. У 27 (38,6%) больных отмечалось ухудшение позы в периоде «выключения», у 8 (11,4%) пациентов — в утренние часы после ночного перерыва в приеме препаратов.
Средняя длительность КК составила 3,6±3,0 года. КК возникала преимущественно в возрасте от 61 года до 70 лет. У 55 (78,6%) больных отмечался наклон вперед, у 15 (21,4%) — сочетание наклона туловища вперед с наклоном в стороны. Тораколюмбальный угол составил в среднем 63,5±17,2°, цервико-краниальный угол — 43,2±22,5°. Болевой синдром наблюдался у 62 (88,6%) больных. У 53 (75,7%) больных отмечалась четкая связь между появлением болевого синдрома в позвоночнике и началом развития КК.
У 44 (62,9%) больных КК возникала уже в положении сидя, у 21 (30%) — сразу при приеме вертикального положения, у 2 (2,9%) — после прохождения 50 м, у 3 (4,3%) — только после значительной нагрузки в вертикальном положении. У 54 (77,1%) пациентов КК наблюдалась в течение всего дня, у 4 (5,7%) — в течение нескольких часов в дневное время, у 12 (17,1%) — только вечером. Факторами, усиливающими проявления КК, в 10% случаев были стрессовые ситуации, в 57% случаев физические нагрузки провоцировали развитие КК.
У 54 (77,1%) пациентов КК наблюдалась в течение всего дня, у 4 (5,7%) — в течение нескольких часов в дневное время, у 12 (17,1%) — только вечером. Факторами, усиливающими проявления КК, в 10% случаев были стрессовые ситуации, в 57% случаев физические нагрузки провоцировали развитие КК.
Для коррекции КК 10 (14,3%) пациентов использовали корсет; 1 (1,4%) пациенту помогало ношение заплечного рюкзака, комбинированное применение рюкзака и корсета было эффективно в 1 (1,4%) случае. Использовали при ходьбе трость 36 (37,1%) пациентов, 8 (11,4%) — были вынуждены использовать ходунки.
Были выделены 3 варианта течения КК при БП: 1. Быстропрогрессирующий тип течения — подострое начало в течение 1-4 нед и быстрое нарастание нарушения позы на протяжении нескольких месяцев (18,6%). 2. Медленно прогрессирующий тип течения — постепенное начало в течение 1-6 мес и нарастание КК на протяжении нескольких лет (65,7%). 3. Ступенчатое — медленно прогрессирующее течение с периодами ухудшения и улучшения позы (15,7%).
Таким образом, по нашим наблюдениям, большинство пациентов страдали от КК даже в положении сидя, КК наблюдалась в течение всего дня, ухудшение КК отмечалось после физической нагрузки или стресса. В большинстве случаев КК была более инвалидизирующим фактором для пациентов, чем классические двигательные симптомы БП.
Обобщая имеющийся материал, целесообразно отметить, что различные концепции патогенеза КК при БП по своему содержанию не противоречат друг другу, а скорее отражают его отдельные звенья [25]. В качестве причин развития КК при БП предполагают аксиальную дистонию или фокальную миопатию паравертебральных мышц, однако точные механизмы патогенеза изучены недостаточно. Миопатия паравертебральных мышц может формироваться вторично на фоне первичной туловищной дистонии и ригидности, отражая хроническое напряжение мышц, участвующих в компенсаторном выпрямлении туловища. Отсутствие достоверной корреляции между степенью выраженности КК и клиническими вариантами БП, эффективностью дофаминергической терапии может свидетельствовать о том, что в ее патогенезе задействованы недофаминергические механизмы [6, 16]. Косвенно о роли центральных недофаминергических путей свидетельствует уменьшение у пациентов с КК объема моста и среднего мозга по данным МРТ головного мозга [8]. Наблюдения пациентов с КК создают предпосылки рассматривать БП в качестве генетически гетерогенного заболевания.
Косвенно о роли центральных недофаминергических путей свидетельствует уменьшение у пациентов с КК объема моста и среднего мозга по данным МРТ головного мозга [8]. Наблюдения пациентов с КК создают предпосылки рассматривать БП в качестве генетически гетерогенного заболевания.
Возможности терапии КК при БП достаточно ограничены. Как правило, при ведении таких пациентов неврологам приходится сталкиваться с многочисленными трудностями, а результаты лечения часто не оправдывают ожидания [11, 39]. Лечение должно включать коррекцию противопаркинсонической терапии, отмену медикаментов, способных вызвать КК, а также хирургическую коррекцию или глубокую стимуляцию мозга [15]. В большинстве наблюдений КК при БП оказывается нечувствительной к стандартной противопаркинсонической терапии. При возникновении КК, связанной с изменениями дофаминергической терапии, целесообразна попытка коррекции медикаментозного лечения и прежде всего исключения или замены одного препарата — агониста дофаминовых рецепторов на другой. Стероиды, по данным различных авторов [26], являются эффективными лишь в редких случаях. Умеренный эффект иногда приносит клоназепам [39]. Локальные инъекции ботулинистического токсина (БТ) в подвздошную мышцу и/или прямую мышцу живота дают неоднозначные результаты [5, 40]. Чаще отмечается полное отсутствие эффекта [4, 22, 40].
Стероиды, по данным различных авторов [26], являются эффективными лишь в редких случаях. Умеренный эффект иногда приносит клоназепам [39]. Локальные инъекции ботулинистического токсина (БТ) в подвздошную мышцу и/или прямую мышцу живота дают неоднозначные результаты [5, 40]. Чаще отмечается полное отсутствие эффекта [4, 22, 40].
В отдельных случаях аномальное положение туловища улучшается при использовании заплечного рюкзака [22]. Некоторые авторы [32] предлагают использовать для облегчения КК поясничные корсеты, кожаные ортезы. В настоящее время все больше находят применение новые специальные ортезы, изготовленные по принципу торакально-тазовой передней фиксации.
Хирургическое лечение КК складывается из стабилизирующих вертебральных вмешательств, а также хронической стимуляции глубоких структур мозга [28, 33]. При операциях на позвоночнике лечение сопряжено с необходимостью длительной иммобилизации, повторными хирургическими вмешательствами, высоким риском осложнений [41, 42].
В современной литературе постепенно накапливаются данные об использовании стимуляции глубоких структур мозга, однако результаты остаются противоречивыми. Кроме того, среди исследователей пока не сложилось единого мнения относительно выбора оптимальной мишени [1, 11].
Болезнь Паркинсона и расстройства движений
Под ред. Иллариошкина С.Н., Левина О.С.
М.: ЗАО «РКИ Соверо пресс», 2014. 405 с.
Настоящее руководство, подготовленное по материалам III Национального конгресса по болезни Паркинсона и расстройствам движений, представляет новейшие данные в области изучения этиологии, патогенеза, разработки методов диагностики и лечения экстрапирамидных заболеваний и других форм двигательных расстройств. В этом году в программе Конгресса и в материалах руководства особое внимание уделено анализу немоторных симптомов болезни Паркинсона, поиску ранних биомаркеров нейродегенеративного процесса, достижениям отечественных ученых в разработке и внедрении наиболее передовых высокотехнологичных методов лечения (в том числе хирургического) и реабилитации пациентов с двигательными расстройствами. Руководство рассчитано на неврологов, нейрореабилитоголов, нейрохирургов, нейрофизиологов, специалистов в области лучевой диагностики, а также практических врачей других специальностей и студентов медицинских вузов, интересующихся данной проблемой клинической неврологии.
Руководство рассчитано на неврологов, нейрореабилитоголов, нейрохирургов, нейрофизиологов, специалистов в области лучевой диагностики, а также практических врачей других специальностей и студентов медицинских вузов, интересующихся данной проблемой клинической неврологии.
СОДЕРЖАНИЕ
Часть I. АННОТИРОВАННЫЕ ДОКЛАДЫ
Раздел 1. Болезнь Паркинсона и другие формы паркинсонизма
1.1. Этиология и молекулярные основы болезни Паркинсона.
Экспериментальные аспекты изучения паркинсонизма.
Этиология болезни Паркинсона: новые представления и новые вызовы
С.Н. Иллариошкин
Трансляционная и профилактическая медицина как основа для борьбы с болезнью Паркинсона
М.В. Угрюмов
Полноэкзомное секвенирование в изучении генетических основ болезни Паркинсона
М.В. Шульская, В.А. Зырин, М.И. Шадрина, С.Н. Пчелина, С.Н. Иллариошкин, П. А. Сломинский
А. Сломинский
Агрегация альфа-синуклеина как возможный молекулярный механизм связи болезни Паркинсона и лизосомных болезней накопления
С.Н.Пчелина, А.К.Емельянов, Е.П.Нужный, Т.С.Усенко, А.Ф.Якимовский, Е.Ю.Захаров.
Оценка ассоциации полиморфной микросателлитной области SNCA-Rep1 с развитием болезни Паркинсона в российской популяции
М.С.Степанова, Е.Ю.Федотова, Н.Ю.Абрамычева, С.Н.Иллариошкин
Ассоциация «промежуточной» полиглутаминовой экспансии гена ATXN2 (атаксин-2) с риском развития нейродегенеративных заболеваний в российской популяции
А.А.Мороз, М.С.Степанова, Е.В.Лысогорская, Е.Ю.Федотова, Н.Ю.Абрамычева,С.А.Клюшников, И.А. Иванова-Смоленская, С.Н.Иллариошкин
Транскриптомные маркеры ранней стадии болезни Паркинсона
М.И. Шадрина, А.Х. Алиева, Е.В. Филатова, А.В. Карабанов, А.А. Колачева, С.Н. Иллариошкин, М.В. Угрюмов, П.А. Сломинский
Мутационный скрининг гена GBAс анализом клинических фенотипов болезни Паркинсона, ассоциированных с мутациями
Н. Ю. Абрамычева, Е.Ю. Федотова, М.С. Степанова, С.Н. Иллариошкин
Ю. Абрамычева, Е.Ю. Федотова, М.С. Степанова, С.Н. Иллариошкин
Ген C9ORF72 в развитии нейродегенеративных заболеваний, сопровождающихся расстройствами движений
Е.Ю. Федотова, Н.Ю. Абрамычева, М.С. Степанова,Е.В. Лысогорская, С.Н. Иллариошкин
Экспериментальные аспекты изучения дофаминергических нейронов, полученных из фибробластов кожи человека на основе технологии индуцированных плюрипотентных стволовых клеток
Л.Г. Хаспеков, А.В. Ставровская, Р.М. Худоерков, Д.Н. Воронков, М.А. Лагарькова, С.Л. Киселев, Е.Ю. Федотова, И.А. Гривенников, И.В. Мухина, С.Н. Иллариошкин.
1.2. Моторные симптомы болезни Паркинсона.
Диагностика и лечение ранней стадии болезни Паркинсона
О.С. Левин, А.В. Росинская
Дрожательные фенотипы болезни Паркинсона
З.А. Залялова.
Нарушение позы у больных с болезнью Паркинсона
Н.В. Федорова, О.А. Орехова.
Феномен застывания при ходьбе у пациентов болезнью Паркинсона
Н. А. Скрипкина, О.С.Левин
А. Скрипкина, О.С.Левин
Клинические особенности нарушений вертикального взора у пациентов с болезнью Паркинсона
С.А. Лихачев, О.А. Аленикова.
1.3. Немоторные симптомы болезни Паркинсона.
Немоторные проявления продромальной стадии болезни Паркинсона
В. Пёве, Ф. Малкнехт (Werner Poewe, Philipp Mahlknecht).
Гетерогенность нервно-психических нарушений при болезни Паркинсона
М.Р. Нодель, Н.Н. Яхно
Некогнитивные предикторы деменции при болезни Паркинсона
И.В. Литвиненко.
Депрессия при болезни Паркинсона
З.А. Залялова, Д.М. Хасанова.
Психотические нарушения при болезни Паркинсона
М.А. Аникина, Е.Е. Васенина, О.С. Левин
Импульсивно-компульсивные нарушения при болезни Паркинсона
Н.В. Федорова, А.В.Никитина
Зрительные нарушения при болезни Паркинсона
О.А. Аленикова, С.А. Лихачев
Нарушение зрительно-пространственного восприятия и изменения сетчатки глаза при болезни Паркинсона
И. В. Литвиненко, П.С. Дынин, Э.В. Бойко, Р.Ф. Гимадутдинов, Г.Е. Исаева
В. Литвиненко, П.С. Дынин, Э.В. Бойко, Р.Ф. Гимадутдинов, Г.Е. Исаева
Вегетативные нарушения в дифференциальной диагностике болезни Паркинсона и мультисистемной атрофии
С.Ю. Киртаев, И.В.Литвиненко
Нарушения поведения во сне с быстрыми движениями глаз у пациентов с болезнью Паркинсона
Е.А. Ляшенко, М.Г. Полуэктов, О.С. Левин
Расстройства фазы быстрого сна при болезни Паркинсона – диагностика и способы терапии
И.В. Красаков, И.В. Литвиненко
Метаболические нарушения при болезни Паркинсона
Р.Р. Богданов, А.Р. Богданов, С.В. Котов
Особенности когнитивных нарушений и дифференциальный диагноз заболеваний с клиникой паркинсонизма
В.В. Захаров.
1.4. Нейровизуализационные и нейрофизиологические бомаркеры болезни Паркинсона.
Возможности МРТ в диагностике и оценке прогрессирования болезни Паркинсона
А.Г. Труфанов, И.В. Литвиненко
Новые возможности структурных методов нейровизуализации в диагностике немоторных симптомов болезни Паркинсона
Е. В. Мазуренко, В.В. Пономарев, Р.А. Сакович
В. Мазуренко, В.В. Пономарев, Р.А. Сакович
Функциональная магнитно-резонансная томография покоя и её роль в изучении экстрапирамидных заболеваний
Ю.А. Селивёрстов, Е.В. Селивёрстова, Р.Н. Коновалов, С.А. Клюшников, М.В. Кротенкова, С.Н. Иллариошкин
Особенности функционирования безусловной нейрональной сети в состоянии покоя и церебрального метаболизма у пациентов с болезнью Паркинсона и различным когнитивным статусом по данным фМРТ и in vivo 1H MRC
З.З. Рожкова, Н.В. Карасевич, А.Н. Омельченко, И.Н. Карабань
МРС черной субстанции у первичных пациентов с болезнью Паркинсона, ранее не получавших леводопатерапию
А.Г. Труфанов, И.В. Литвиненко.
Электрофизиологические особенности треморной активности мышц при эссенциальном треморе и болезни Паркинсона
Е.О.Иванова, А.П.Федин, И.А.Иванова-Смоленская, С.Н. Иллариошкин
Изменения источников когнитивных вызванных потенциалов Р300 у больных болезнью Паркинсона
С. А. Крижановский, А.А. Чернинский, О.В. Иваненко, И.Г. Зима, И.Н. Карабань
А. Крижановский, А.А. Чернинский, О.В. Иваненко, И.Г. Зима, И.Н. Карабань
1.5. Лечение и реабилитация пациентов с болезнью Паркинсона.
Современные подходы к лечению болезни Паркинсона
А. Антонини (Angelo Antonini)
Неотложные состояния при болезни Паркинсона
О.С. Левин.
Двигательные осложнения длительной леводопа-терапиии подходы к их коррекции
Е.А. Катунина, Н.В. Титова
Взгляд клинического фармаколога на возможности фармакотерапии болезни Паркинсона с использованием ротиготина – трансдермального пластыря
С.К. Зырянов.
Роль ингибитора МАО-В разагилина в лечении болезни Паркинсона
О.С. Левин.
Оценка эффективности терапии пирибедилом пациентов с болезнью Паркинсона при моторных флуктуациях и лекарственных дискинезиях
Ю.А. Князькина
Использование ботулинотерапии для лечения камптокормии у пациентов с болезнью Паркинсона (клинический случай)
А. П. Коваленко.
П. Коваленко.
Роль медицинской реабилитации в лечении болезни Паркинсона
Н.А. Амосова, И.Г. Смоленцева.
Мультидисциплинарный подход к ведению больных на поздней стадии болезни Паркинсона
И.Г. Смоленцева, О.В. Кривонос, Н.А. Амосова.
Возможный нейропротективный эффект метода темпоритмовой коррекции ходьбы при болезни Паркинсона
Д.В. Похабов, В.Г. Абрамов, Ю.В. Нестерова.
Послеоперационное ведение больных с болезнью Паркинсона на фоне глубокой стимуляции головного мозга
Е.В. Бриль, А.А. Томский, А.А. Гамалея , В.А. Шабалов, Н.В. Федорова, Н.А. Губарева.
1.6. Вопросы организации специализированной помощи и ведения пациентов с болезнью Паркинсона. Эпидемиология. Качество жизни.
Организация медицинской помощи больным болезнью Паркинсона в современных социально-экономических условиях
О.В. Кривонос.
Медицинские и социальные аспекты болезни Паркинсона
А.Б. Гехт, Г. Р. Попов.
Р. Попов.
Регистр болезни Паркинсона Национального общества болезни Паркинсона и расстройств движений
С.Н. Иллариошкин, А.Н. Бойко, О.С. Левин, С.В. Петров, А. Б. Ямпольский, П.У. Гойтемирова, Е.М. Ким, Н.А. Орышич, О.Л. Табакова, А.К. Файзулаева, И.Л. Иванова, Е.В. Сизова, Л.В. Чепкасова, И.С. Чупина
Инновационные возможности объективизации качества жизни пациентов с болезнью Паркинсона
И.Н. Карабань, Н.В. Карасевич, О.В. Крицкая.
Можно ли предупредить болезнь Паркинсона?
О.С. Левин.
Идентификация лиц в латентной стадии болезни Паркинсона: первые результаты российского обсервационного исследования ПАРКИНЛАР
Е.Ю. Федотова, А.О. Чечеткин, Н.Ю. Абрамычева, Л.А. Чигалейчик, Б.Х. Базиян, Т.А. Пономарева, Н.С. Алексеева, П.А. Федин, М.А. Кравченко, С.Н. Иллариошкин.
Раздел 2. Экстрапирамидные гиперкинезы
2.1. Дистония.
Молекулярная генетика фокальной дистонии в российской популяции
М. Ю. Краснов, С.Л. Тимербаева, Н.Ю. Абрамычева, М.С. Степанова, Ю.А. Шпилюкова, О.Ю. Реброва, С.Н. Иллариошкин.
Ю. Краснов, С.Л. Тимербаева, Н.Ю. Абрамычева, М.С. Степанова, Ю.А. Шпилюкова, О.Ю. Реброва, С.Н. Иллариошкин.
Краниальные дистонии: клинические проявления, дифференциальная диагностика, методы лечения
З.А. Залялова
Писчий спазм: современное состояние проблемы, опыт лечения инъекциями ботулотоксина типа А
С.А. Лихачев, Т.Н. Чернуха, Н.И. Черненко.
Интенционная судорога Рюльфа и другие пароксизмальные дискинезии
М.В. Селихова.
2.2. Тремор, хорея и тики.
Тремор: дифференциальная диагностика и выбор терапии
Е. Ружичка (Evzen Růžička).
Нейрофизиологические маркеры преклинической стадии болезни Гентингтона и их зависимость от тяжести мутаций в гене гентингтина
Н.В. Пономарева, С.А. Клюшников, Н.Ю. Абрамычева, Д.Д. Малина, Н.С. Щеглова, В.Ф. Фокин, И.А. Иванова-Смоленская, С.Н. Иллариошкин
Морфофункциональные изменения головного мозга при болезни Гентингтона
Е. Н. Юдина, С.Н. Иллариошкин, Р.Н. Коновалов, В.В. Гнездицкий
Н. Юдина, С.Н. Иллариошкин, Р.Н. Коновалов, В.В. Гнездицкий
Синдром Туретта у детей и подростков
В.П. Зыков, Е.Б. Новикова, Э.С.Каширина
Глубокая стимуляция мозга при синдроме Туретта с выраженными инвалидизирующими тиками и генерализованной дистонии
В.М. Тюрников, И.И. Федоренко, С.Н. Иллариошкин, Е.Ю. Федотова, Л.П. Метелкина, А.О. Гуща.
Раздел 3. Другие двигательные расстройства
Расстройства движений при нейродегенеративных деменциях
Е.Е. Васенина, О.А. Ганькина, О.С. Левин.
Токсическое поражение базальных ядер: диагностика и лечение
П. Таба (Pille Taba)
Нейродегенерации с накоплением железа в мозге: юношеские и взрослые формы
Г.Е. Руденская, Е.Ю. Захарова
Аутосомно-рецессивные мозжечковые атаксии
С.В. Копишинская, А.В. Густов, М.А. Радюк, С.Н. Светозарский.
Болезнь Ниманна-Пика типа C — молекулярная генетика и патогенез, клиническиефенотипы, возможности диагностики и терапии
С. А. Клюшников.
А. Клюшников.
Эффективность ботулинотерапии при спастичности
Д.В. Похабов, В.Г. Абрамов, Ю.В. Нестерова.
Двигательные расстройства в психиатрии
В.Л. Голубев.
Часть II. ТЕЗИСЫ
ГЕН FMR1 И ДВИГАТЕЛЬНЫЕ РАССТРОЙСТВА У ПАЦИЕНТОВ В РОССИЙСКОЙ ПОПУЛЯЦИИ
Н.Ю. Абрамычева, М.С. Степанова, Е.Ю. Федотова, С.Л. Тимербаева, С.Н. Иллариошкин.
УРОВЕНЬ АЛЬФА-СИНУКЛЕИНА В ПЛАЗМЕ КРОВИ У ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА И ПАЦИЕНТОВ С ЛИЗОСОМНЫМИ БОЛЕЗНЯМИ НАКОПЛЕНИЯ
П.А. Андоскин, Е.П. Нужный, А.К. Емельянов, М.А. Николаев, А.Ф. Якимовский, Е.Ю. Захарова, С.Н. Пчелина.
КОРРЕКЦИЯ ДВИГАТЕЛЬНЫХ РАССТРОЙСТВ У ВЗРОСЛЫХ ПАЦИЕНТОВ, СТРАДАЮЩИХ ДЕТСКИМ ЦЕРЕБРАЛЬНЫМ ПАРАЛИЧОМ
Е.А. Антипенко, А.В. Густов
ОПЫТ ПРИМЕНЕНИЯ АНВИФЕНАョ В ЛЕЧЕНИИ ГИПЕРКИНЕТИЧЕСКОГО СИНДРОМА
Г.Н. Бельская, И.Г. Лукашевич, Л.В. Тряпицына, Е.А. Политицкая, Е.И. Лузанова.
ВЛИЯНИЕ ДРОЖАТЕЛЬНОГО ГИПЕРКИНЕЗА НА КАЧЕСТВО ЖИЗНИ ПАЦИЕНТОВ, СТРАДАЮЩИХ БОЛЕЗНЬЮ ПАРКИНСОНА
В. А. Богачева, Д.В. Захаров, В.А. Михайлов
А. Богачева, Д.В. Захаров, В.А. Михайлов
ЛИПИДНЫЕ ПАРАМЕТРЫ КРОВИ У ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА
Е.В.Борисова, М.А.Фоминцева, С.А.Свиридова, Н.Г.Никульчева, Л.А.Шатилина
СНИЖЕНИЕ ЧАСТОТЫ КОРОТКИХ АЛЛЕЛЕЙ B2-VNTR ГЕНА РЕЦЕПТОРА В2 БРАДИКИНИНА У ЖЕНЩИН С ДЕБЮТОМ ЗАБОЛЕВАНИЯ БОЛЕЗНИ ПАРКИНСОНА ДО 50 ЛЕТ
Н.К. Боровкова, И.О. Сучкова, Е.В. Борисова, Е.Л. Паткин
ТРЕХЛЕТНЕЕ СРАВНИТЕЛЬНОЕ ИССЛЕДОВАНИЕ ЭФФЕКТИВНОСТИ ЭЛЕКТРОСТИМУЛЯЦИИ СУБТАЛАМИЧЕСКОГО ЯДРА И КОНСЕРВАТИВНОЙ ТЕРАПИИ У БОЛЬНЫХ С РАЗВЕРНУТОЙ СТАДИЕЙ БОЛЕЗНИ ПАРКИНСОНА
Е.В.Бриль, А.А.Томский, А.А.Гамалея, В.А.Шабалов, Н.В.Федорова, А.А.Бондаренко, С.Б.Буклина, А.В. Декопов, Е.М. Салова, Н.Н.Губарева
УРОВЕНЬ АЛЬФА-СИНУКЛЕИНА В CD45+ КЛЕТКАХ ПЕРИФЕРИЧЕСКОЙ КРОВИ ПРИ БОЛЕЗНИ ПАРКИНСОНА
А.К. Емельянов, П.А. Андоскин, А.Ф. Якимовский, А.А. Тимофеева, М.А. Николаев, С.Н. Пчелина.
КЛИНИКО-МР-ТОМОГРАФИЧЕСКАЯ ХАРАКТЕРИСТИКА ЛЕКАРСТВЕННОГО ПАРКИНСОНИЗМА
З. А. Залялова, Г.Р. Латыпова, С.Э. Мунасипова
А. Залялова, Г.Р. Латыпова, С.Э. Мунасипова
СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ЭССЕНЦИАЛЬНОГО ТРЕМОРА И БОЛЕЗНИ ПАРКИНСОНА ПО ЭЛЕКТРОФИЗИОЛОГИЧЕСКИМ ПАРАМЕТРАМ ПОСТУРАЛЬНОГО ТРЕМОРА РУК
Е.О. Иванова, П.А. Федин, А.Г. Брутян, И.А. Иванова-Смоленская, С.Н. Иллариошкин.
КОМОРБИДНЫЕ СОСТОЯНИЯ И КАЧЕСТВО ЖИЗНИ У ПАЦИЕНТОВ С ФОКАЛЬНЫМИ ДИСТОНИЯМИ
И.Г. Измайлова, И.В. Кравцова, А.Ф. Старостюк, Т.И. Бодрова, Ю.В. Цымбал, Е.Н. Журавлева.
ОПЫТ ЛЕЧЕНИЯ РАЗЛИЧНЫХ ФОРМ ИДИОПАТИЧЕСКОЙ ДИСТОНИИ БИПЕРИДЕНА ГИДРОХЛОРИДОМ (АКИНЕТОНОМ)
А.В. Карабанов, М.Ю. Краснов, Н.Ю. Абрамычева, С.Н. Иллариошкин
ДИАГНОСТИКА ДРОЖАТЕЛЬНОГО ГИПЕРКИНЕЗА С ИСПОЛЬЗОВАНИЕМ ОРИГИНАЛЬНОГО АППАРАТНО-ПРОГРАММНОГО КОМПЛЕКСА
А.В. Карабанов, С.Н. Иллариошкин, В.В. Шведков, В.В Полещук, И.А. Иванова-Смоленская, С.В. Пушилин, В.Б. Чемоданов
ЗАПОРЫ ПРИ БОЛЕЗНИ ПАРКИНСОНА И ВОЗМОЖНЫЕ ПУТИ ИХ КОРРЕКЦИИ
С.Ю. Киртаев, И.В. Литвиненко.
СИНДРОМ SANDO — НОВАЯ ФОРМА АУТОСОМНО-РЕЦЕССИВНЫХ АТАКСИЙ
С. А. Клюшников, Т.Д. Крылова, П.Г. Цыганкова, Ю.А. Селивёрстов, Е.В. Коновалова, Е.Ю. Захарова.
А. Клюшников, Т.Д. Крылова, П.Г. Цыганкова, Ю.А. Селивёрстов, Е.В. Коновалова, Е.Ю. Захарова.
ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ ФАРМАКОЛОГИЧЕСКОГО ДЕЙСТВИЯ ЛЕВОДОПЫ В СОСТАВЕ ПОЛИМЕРНЫХ КАПСУЛ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ПАРКИНСОНА
И.Г. Кондрашева, П.Е. Гамбарян, И.А. Тубашева, Е.С. Северин, А.А. Каменский.
МУТАЦИИ В ГЕНЕ TOR1A (DYT1) ПРИ ГЕНЕРАЛИЗОВАННОЙ ДИСТОНИИ В РОССИЙСКОЙ И БЕЛОРУССКОЙ ПОПУЛЯЦИЯХ
М.Ю. Краснов, С.А. Лихачев, Н.Ю. Абрамычева, Т.Н. Чернуха, И.В. Плешко, С.Л. Тимербаева, С.Н. Иллариошкин.
ОСОБЕННОСТИ ПАТОГЕНЕТИЧЕСКОГО ЛЕЧЕНИЯ РАЗЛИЧНЫХ КЛИНИЧЕСКИХ ФОРМ ЭССЕНЦИАЛЬНОГО ТРЕМОРА
Г.Р. Латыпова, З.А. Залялова.
ОСОБЕННОСТИ МЕДИКАМЕНТОЗНОЙ ТЕРАПИИ ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА В ПЕРИОД ГЛУБОКОЙ СТИМУЛЯЦИИ ГОЛОВНОГО МОЗГА
А.С. Лихачев, М.Н. Ган
КЛИНИЧЕСКОЕ ЗНАЧЕНИЕ НАРУШЕНИЙ ВЕРТИКАЛЬНОГО ВЗОРА У ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА
С.А. Лихачев, О.А. Аленикова
ВИДЕОАНАЛИЗ ДВИЖЕНИЙ В ДИАГНОСТИКЕ БОЛЕЗНИ ПАРКИНСОНА
С. А. Лихачев, В.В. Ващилин, И.С. Гурский
А. Лихачев, В.В. Ващилин, И.С. Гурский
ДИСТОНИЧЕСКИЕ РЕАКЦИИ, ОБУСЛОВЛЕННЫЕ ПРИЕМОМ ЛЕКАРСТВЕННЫХ СРЕДСТВ
С.А. Лихачев, Т.Н. Чернуха, Е.А. Королевич
ОПЫТ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭКСТРАПИРАМИДНОЙ ПАТОЛОГИИ МЕТОДОМ ХРОНИЧЕСКОЙ СТИМУЛЯЦИИ ГЛУБИННЫХ СТРУКТУР ГОЛОВНОГО МОЗГА (DBS)
В.В. Алексеевец, С.А. Лихачев, Т.Н. Чернуха, С.В. Терехов, Г.В. Забродец, М.Н. Ган.
ОЦЕНКА НАРУШЕНИЙ СНА ПРИ БОЛЕЗНИ ПАРКИНСОНА ПО ДАННЫМ ПОЛИСОМНОГРАФИИ
С.А.Лихачев, И.С. Савицкий
КАРНОЗИН ПРЕДОТВРАЩАЕТ РОСТ СОДЕРЖАНИЯ МЕТГЕМОГЛОБИНА, ВЫЗВАННОГО ВВЕДЕНИЕМ АКРОЛЕИНА, В ЭРИТРОЦИТАХ ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА
М.Г. Маклецова, Г.Т. Рихирева, В.В. Полещук, А.А. Логвиненко, Л.М. Байдер, М.Ю. Вакуленко, Т.Н. Федорова, С.Л. Тимербаева
КЛИНИКО-БИОХИМИЧЕСКАЯ ГЕТЕРОГЕННОСТЬ БОЛЕЗНИ ПАРКИНСОНА
И.В. Милюхина, М.Н. Карпенко
ВЕРОЯТНЫЙ СЛУЧАЙ СПОРАДИЧЕСКОЙ МУЛЬТИСИСТЕМНОЙ АТРОФИИ В МОЛОДОМ ВОЗРАСТЕ
Е.С. Мищенко.
СИНДРОМ «ЧУЖОЙ» РУКИ (ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ)
С. Э.Мунасипова, З.А.Залялова.
Э.Мунасипова, З.А.Залялова.
РАСПРОСТРАНЕННОСТЬ БОЛЕЗНИ ПАРКИНСОНА В РЕСПУБЛИКЕ БАШКОРТОСТАН
Л.Б. Новикова, А.П. Акопян, Э.Р. Галимуллина.
ИНСОМНИЯ ПРИ БОЛЕЗНИ ПАРКИНСОНА И ЕЕ ВЛИЯНИЕ НА КАЧЕСТВО ЖИЗНИ ПАЦИЕНТОВ
М.Р. Нодель, Н.Н. Яхно, Ю.В. Украинцева, В.Б. Дорохов
ГЕТЕРОГЕННОСТЬ ГИПЕРСОМНИЧЕСКОГО СИНДРОМА ПРИ БОЛЕЗНИ ПАРКИНСОНА
М.Р. Нодель, Н.Н. Яхно, Ю.В. Украинцева.
РОЛЬ МУТАЦИЙ В ГЕНАХ ЛИЗОСОМНЫХ БОЛЕЗНЕЙ НАКОПЛЕНИЯ В ВОЗНИКНОВЕНИИ НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ
Е.П. Нужный, А.Ф. Якимовский, А.А. Тимофеева, А.М. Букина, Е.Ю. Захарова, С.Н. Пчелина.
АНАЛИЗ ТОНКОЙ СТРУКТУРЫ ТАНДЕМНЫХ CAG- И CCG-ПОВТОРОВ В ГЕНЕ НТТ ПРИ БОЛЕЗНИ ГЕНТИНГТОНА
Д.А. Приходько, Н.Ю. Абрамычева, М.С. Степанова, С.А. Клюшников.
ИНТРАЭПИДЕРМАЛЬНЫЕ НЕРВНЫЕ ВОЛОКНА В ДИАГНОСТИКЕ СЕНСОРНЫХ НАРУШЕНИЙ ПРИ БОЛЕЗНИ ПАРКИНСОНА
М.А. Радюк, О.В. Курушина, С.В. Копишинская, А.В. Густов
ВОЗМОЖНОСТЬ ОЦЕНКИ СКОРОСТИ ПРОГРЕССИРОВАНИЯ БОЛЕЗНИ ПАРКИНСОНА В ОТСУТСТВИЕ ДИНАМИЧЕСКОГО НАБЛЮДЕНИЯ ЗА БОЛЬНЫМ
В. В. Раздорская, О.Н. Воскресенская, Г.К. Юдина
В. Раздорская, О.Н. Воскресенская, Г.К. Юдина
ЗАБОЛЕВАЕМОСТЬ БОЛЕЗНЬЮ ПАРКИНСОНА В САРАТОВЕ
В.В. Раздорская, О.Н. Воскресенская, Г.К. Юдина.
НАСЛЕДСТВЕННАЯ СПАСТИЧЕСКАЯ ПАРАПЛЕГИЯ 3-ГО ТИПА (SPG3): ПЕРВЫЕ РОССИЙСКИЕ НАБЛЮДЕНИЯ
Г.Е.Руденская, К.Биц (С.Beetz), В.А.Кадникова, А.А.Степанова, Т.Н.Проскокова, В.П.Федотов, А.В. Поляков
КЛИНИЧЕСКИЙ СЛУЧАЙ БЛЕФАРОСПАЗМА, АССОЦИИРОВАННОГО СО ВТОРИЧНЫМ ДИСМЕТАБОЛИЧЕСКИМ МИОПАТИЧЕСКИМ СИНДРОМОМ
Д.К. Сичинава, Л.А. Цукурова, М.А. Барабанова, Е.Н. Головко, П.В. Катаев
ОТРАБОТКА ЭКСПЕРИМЕНТАЛЬНОЙ МОДЕЛИ БОЛЕЗНИ ГЕНТИНГТОНА ДЛЯ РЕШЕНИЯ ФУНДАМЕНТАЛЬНЫХ ЗАДАЧ НЕЙРОБИОЛОГИИ
А.В. Ставровская, Н.Г. Ямщикова, А.С. Ольшанский, Д.Н. Воронков, С.Н. Иллариошкин.
КОМБИНИРОВАННОЕ НЕЙРОХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ БОЛЬНЫХ С БОЛЕЗНЬЮ ПАРКИНСОНА С ИСПОЛЬЗОВАНИЕМ МЕТОДА СТЕРЕОТАКСИЧЕСКОЙ ВЫСОКОЧАСТОТНОЙ ДЕСТРУКЦИИ С ОДНОЙ СТОРОНЫ И ГЛУБОКОЙ СТИМУЛЯЦИИ ПОДКОРКОВЫХ СТРУКТУР ГОЛОВНОГО МОЗГА С ДРУГОЙ СТОРОНЫ
В. М.Тюрников, И.И. Федоренко, Л.П. Метелкина , Е.Ю. Федотова,В.В. Полещук, С.Н. Иллариошкин, А.О. Гуща.
М.Тюрников, И.И. Федоренко, Л.П. Метелкина , Е.Ю. Федотова,В.В. Полещук, С.Н. Иллариошкин, А.О. Гуща.
ПЕРСПЕКТИВЫ ПРОФИЛАКТИКИ ТОКСИЧЕСКОГО ПАРКИНСОНИЗМА: ИНТЕГРАЦИЯ ДОСТИЖЕНИЙ НЕЙРОХИМИИ В ОБРАЗОВАТЕЛЬНЫЕ ПРОГРАММЫ ТЕХНИЧЕСКИХ И
ТЕХНОЛОГИЧЕСКИХ ВУЗОВ
А.Т. Файзутдинова, Р.С. Заббарова.
МИКРОЭЛЕКТРОДНАЯ РЕГИСТРАЦИЯ ВО ВРЕМЯ ИМПЛАНТАЦИИ ЭЛЕКТРОДОВ ДЛЯ ГЛУБОКОЙ СТИМУЛЯЦИИ МОЗГА ПРИ БОЛЕЗНИ ПАРКИНСОНА
И.И. Федоренко, В.М. Тюрников, Л.П. Метелкина, С.Н. Иллариошкин, А.О. Гуща.
«НОРМОТИМИЧЕСКОЕ» ДЕЙСТВИЕ БОТУЛИНОТЕРАПИИ В РЕАБИЛИТАЦИИ ПАЦИЕНТОВ С КРАНИАЛЬНОЙ И ЦЕРВИКАЛЬНОЙ ДИСТОНИЕЙ
З.Г.Хаятова, Г.Н.Гарипова, З.А.Залялова.
ОСОБЕННОСТИ НЕЙРОННОЙ ОРГАНИЗАЦИИ КОМПАКТНОЙ ЧАСТИ ЧЕРНОЙ СУБСТАНЦИИ МОЗГА ЧЕЛОВЕКА И КРЫСЫ
Д.Н.Воронков, Р.М.Худоерков, В.Н.Сальков, Ю.В.Дикалова, Н.С.Носс.
РОЛЬ ИССЛЕДОВАНИЯ ЗРИТЕЛЬНО-МОТОРНОЙ КООРДИНАЦИИ У ПАЦИЕНТОВ С БОЛЕЗНЬЮ ПАРКИНСОНА И ИХ РОДСТВЕННИКОВ ПРИ РАННЕЙ И ДОКЛИНИЧЕСКОЙ ДИАГНОСТИКЕ ЗАБОЛЕВАНИЯ
Л. А. Чигалейчик, Е.Ю. Федотова, В.В. Полещук, Б.Х. Базиян, С.Н. Иллариошкин.
А. Чигалейчик, Е.Ю. Федотова, В.В. Полещук, Б.Х. Базиян, С.Н. Иллариошкин.
ОСОБЕННОСТИ ПСИХОСОЦИАЛЬНОГО ФУНКЦИОНИРОВАНИЯ БОЛЬНЫХ ЭССЕНЦИАЛЬНЫМ ТРЕМОРОМ
Ю.В. Шубина, Д.В. Захаров, В.А. Михайлов.
Участиники
Именной указатель
Противодействия болезни Паркинсона, комплексы упражнений. Научный раздел клиники ИАКИ
Глубокое дыхание
Цель: добиться упражнением более глубокого дыхания.
В положении сидя. Положите руки на живот. Сделайте медленный глубокий вдох через нос, почувствуйте как расширяется грудная клетка и как бы «надувается» живот. Затем медленно, считая до 5, выдыхайте воздух через рот, как при задувании свечи. Повторите 10 раз. В положении стоя. Подойдите к стенке. Встаньте так, чтобы всей спиной и поясницей Вы чувствовали бы стенку или другую вертикальную поверхность: шкаф, дверь и т.д. Поднимите руки вверх и, касаясь ими стены, сделайте глубокий вдох; при выдохе опускайте руки вниз и перекрещивайте их перед грудью и животом так, чтобы кисть правой руки взялась за локоть левой руки и наоборот. Повторите 10 раз.
Повторите 10 раз.
Упражнение для улучшения осанки
Цель: научиться регулировать напряжение мышц шеи, туловища, чтобы противодействовать формированию «согбенной позы».
Встаньте спиной к стене, так, чтобы затылок, лопатки, ягодицы, бедра и голени касались стены; руки располагаются вдоль тела, ладони упираются в стену. Постарайтесь с напряжением «вжаться» в стену (до счета 5), а потом следует расслабиться и отдохнуть, сколько Вам потребуется. Повторяйте упражнение несколько раз, старайтесь «не сбивать» дыхания. Исходное положение, как и в предыдущем упражнении. Оставаясь «прилипшим» к стене затылком, спиной, ягодицами и ладонями присядьте на корточки «скользя» спиною по стене. Если Вам трудно потом подняться, поставьте рядом стул или возьмите палку, на которую можно опереться. Встаньте лицом к стене так, чтобы одна щека, повернутая в сторону, грудная клетка и живот, бедра как бы «прилипли» к стене. Раскиньте руки на уровне плеч и расположите их так, чтобы ладони «прилипли» к стене. Поднимайте «прилипшие» к стене ладони кверху над головой. Когда ладони над головой — делайте выдох, когда они возвращаются на уровень плеч — делайте вдох. Упражнение делаете до ощущения приятной усталости.
Поднимайте «прилипшие» к стене ладони кверху над головой. Когда ладони над головой — делайте выдох, когда они возвращаются на уровень плеч — делайте вдох. Упражнение делаете до ощущения приятной усталости.
«Скручивание туловища»
Цель: улучшение подвижности мышц шеи, плеч, туловища. В положении сидя или стоя положите ладони на плечи или за шею. Поворачивайте голову, шею и туловище сначала в одну, а потом в другую сторону, как можно больше. Вы должны почувствовать легкое напряжение мышц туловища. Повторите 10 раз.
Прогибания туловища
Цель: улучшение осанки и улучшение подвижности в грудном и поясничном отделе позвоночника.
Сидя на стуле положите ладони на колени, наклонитесь вперед, после чего, выгните спину дугой, расправьте плечи. Затем сядьте прямо. Повторите 10 раз.
Сидя на стуле поместите кисти рук на область поясницы («возьмите себя за поясницу»). Прогнитесь в пояснице, выпятив грудь вперед и расправив плечи, считая до «20». Затем сядьте прямо. Повторите 10 раз.
Затем сядьте прямо. Повторите 10 раз.
Упражнение для мышц брюшного пресса
Цель: укрепление мышц брюшного пресса.
Лежа на спине (на полу, на кровати), согните ноги в коленях, поставив стопы на пол (кровать). Медленно вытяните руки вперед и садитесь, приподнимая плечи и голову (при этом поясница касается пола) столько раз, на сколько у Вас хватит сил, не ‘сбивая дыхания». Коснитесь руками коленей. Затем вернитесь в исходное положение. Повторите 10 раз.
«Мостик»
Цель: укрепление мышц туловища, бедер и тренировка поворотов в постели. Лежа на спине, согните ноги в коленях, поставив стопы на пол (кровать), поднимите таз, опираясь на стопы и на плечи, повернитесь налево и направо. Повторите 10 раз.
Отжимания
Цель: растяжение плечевых мышц и улучшение позы. Встаньте лицом в угол комнаты. Упритесь руками в обе стенки и наклонитесь к углу, согнув руки в локтях так, чтобы Вы почувствовали напряжение мышц. При выполнении наклона не отрывайте стопы от пола. Наклонившись и продолжая упираться руками в стены, посчитайте до 20. Затем вернитесь в исходное положение. Повторите 10 раз.
При выполнении наклона не отрывайте стопы от пола. Наклонившись и продолжая упираться руками в стены, посчитайте до 20. Затем вернитесь в исходное положение. Повторите 10 раз.
Круговые движения и наклоны туловища Цель: улучшение подвижности мышц туловища. Исходное положение стоя, ноги — на ширине плеч, руки — на талии. Выполняйте круговые движения туловищем (как будто вертите обруч), а также наклоны кпереди, кзади, в стороны. Повторите по 10 раз в каждую сторону. Упражнения для мышц шеи и надплечья Повороты головы в стороны Цель: улучшение подвижности в шейном отделе позвоночника. В положении сидя или стоя медленно поворачивайте голову из стороны в сторону, стараясь при поворотах смотреть за плечо. Повернув голову, удерживайте её в таком положении, считая до 5. Вы должны почувствовать легкое напряжение мышц шеи. Повторите 10 раз.
Наклоны головы в стороны
Цель: улучшение подвижности в шейном отделе позвоночника. В положении сидя. Медленно наклоняйте голову в стороны, поочередно к каждому плечу. Во время наклонов старайтесь не поворачивать голову, смотрите вперед. При каждом наклоне Вы должны почувствовать легкое напряжение («растяжение») мышц шеи. Выполняйте по 10 наклонов в каждую сторону.
Во время наклонов старайтесь не поворачивать голову, смотрите вперед. При каждом наклоне Вы должны почувствовать легкое напряжение («растяжение») мышц шеи. Выполняйте по 10 наклонов в каждую сторону.
Наклоны головы вперед и назад
Цель: улучшение осанки и уменьшение фиксированного сгибательного положения головы.
В положении сидя или стоя. Разогнуть шею и выдвинуть подбородок вперед.
Затем вернитесь в исходное положение. Повторите 10 раз. Опустить голову и коснуться подбородком груди, вернуть голову в исходное положение. Повторите 10 раз. После этого медленно откиньте голову назад (если Вы выполняете это движение стоя, лучше подстраховаться, удерживаясь за крепкий неподвижный предмет или скобу на стене). Откинув голову назад постарайтесь расслабить мышцы шеи и «почувствовать это положение». Оно должно противодействовать фиксированному положению шеи в позе сгибания.
Упражнения для мышц плечевого пояса
Упражнение для попеременного напряжения и расслабления мышц верхнего плечевого пояса («молитва»)
Цель: добиться тренировкой напряжения и расслабления мышц верхнего плечевого пояса.
В положении сидя или стоя соедините руки, сложив ладони друг с другом.
Напрягите руки, что есть мочи, чтобы ладони упирались друг в друга. Просчитайте до «20». Потом расслабьте руки, «бросьте» их вниз. Повторите 5-10 раз. Постарайтесь зафиксировать в памяти свои ощущения во время напряжения рук и во время их расслабления. Ощущение расслабления попробуйте воспроизвести при нарастании скованности. Разведение плеч («расправить плечи»)
Цель: увеличение объема движений в суставах верхнего плечевого пояса. В положении сидя или стоя согните руки в локтях и отведите локти назад, приблизив друг к другу лопатки. Удерживайте их в таком положении, считая до пяти. Затем расслабьтесь и верните руки в исходное положение. Повторите 10 раз.
Круговые движения в плечевых суставах
Цель: увеличение объема движений в плечевых суставах. В положении сидя или стоя производите круговые движения плечами (плечо движется вверх, назад, вниз и вперед). Выполняйте вместе или поочередно каждым плечом по 5 раз. Затем повторите круговые движения в противоположную сторону (вниз, вперед, вверх, назад).
Выполняйте вместе или поочередно каждым плечом по 5 раз. Затем повторите круговые движения в противоположную сторону (вниз, вперед, вверх, назад).
Упражнение с палкой
1) подъем и опускание
Цель: увеличение объема движений в плечевых суставах. В положении сидя или стоя возьмите обеими руками деревянную палку (трость) длиной около 1 метра и поднимите до уровня груди. Затем попробуйте поднять палку над головой. Далее опустите руки до уровня груди и затем опустите руки на колени.
Повторите 10 раз.
2) «круги»
Цель: увеличение объема движений в плечевых суставах. В положении сидя. Держа палку обеими руками на уровне груди, выполняйте круговые обороты («рисуя перед собой круг»), плавно сгибая и выпрямляя руки в локтях. Повторите 10 раз в каждую сторону.
«Вы на байдарке»
Цель: увеличение объема движений в плечевых и локтевых суставах.
В положении сидя, держа палку обеими руками на уровне груди, двигайте палкой то одной, то другой рукой, имитируя движения веслом байдарке. Повторите 10 раз.
Повторите 10 раз.
В положении сидя, держите палку руками горизонтально на уровне бедер. Поднимите правый конец палки вверх в направлении правого плеча, при этом лозая рука остается неподвижной, з палка располагает ся диагонально по отношению к телу. Опустите палку в исходное положение, теперь выполните упражнение, поднимая левый конец палки левой рукой. Повторите по 5 раз в каждую сторону.
Упражнение для рук
Цель: улучшение подвижности в локтевых и лучезапястных суставах. В положении сидя положите кисти на бедра, ладонями вниз. Затем поверните руки ладонями вверх. Начинайте эти попеременные движения в медленном темпе, затем постепенно увеличивайте темп движений. Повторите 10 раз. Можете при этом «прихлопывать» кистями, отбивая удобный для Вас ритм движений.
Круговые движения кисти
Цель: улучшение подвижности в лучезапястных суставах. В положении сидя, медленно выполняйте круговые вращения кисти одной руки в лучезапястном суставе. Выполняйте по пять оборотов в каждую сторону. Затем выполните круговые вращения кисти другой руки. При необходимости, для облегчения движений кисти одной руки можете фиксировать это предплечье другой рукой.
Выполняйте по пять оборотов в каждую сторону. Затем выполните круговые вращения кисти другой руки. При необходимости, для облегчения движений кисти одной руки можете фиксировать это предплечье другой рукой.
Упражнение для пальцев рук
Цель: улучшение подвижности пальцев.
В положении сидя или стоя, поочередно дотрагивайтесь большим пальцем до 2, 3, 4 и 5 пальцев. Продолжайте упражнение, стараясь увеличить темп движений. Повторите 10 раз.
Упражнения для мышц нижнего пояса конечностей Прогибания в поясничном отделе позвоночника Цель: улучшение подвижности мышц поясницы и бедер. Лягте на живот. Расслабьтесь на 3-5 минут. Затем попытайтесь приподнять верхнюю половину туловища, опираясь на локти и стараясь прогнуться в пояснице. Оставайтесь в таком положении, считая до «20». Затем вернитесь в исходное положение и расслабьтесь. Повторите 10 раз.
Упражнение для мышц бедер (разведение бедер)
Цель: укрепление мышц бедер
Лежа на спине, согните ноги в коленях, поставив стопы на пол (на кровать). Разведите бедра и колени в стороны, соединив подошвы. Удерживайте ноги в таком положении, считая до «20». Вы должны почувствовать легкое напряжение мышц внутренней поверхности бедер. Затем верните ноги в исходное положение. Повторите 10 раз.
Разведите бедра и колени в стороны, соединив подошвы. Удерживайте ноги в таком положении, считая до «20». Вы должны почувствовать легкое напряжение мышц внутренней поверхности бедер. Затем верните ноги в исходное положение. Повторите 10 раз.
Повороты бедер в положении лежа
Цель: развивает гибкость мышц туловища и бедер. Лежа на спине (на полу, на кровати), согните ноги в коленях, поставив стопы на пол (кровать). Наклоняйте колени обеих ног в стороны, стараясь коснуться ими пола (кровати). Наклонив колени, удерживайте их в таком положении, считая до 20. Повторите упражнение с наклоном 10 раз в каждую сторону.
Подъем прямой ноги
Цель: укрепление мышц бедер и голеней.
Лежа на спине (на полу), согните одну ногу в колене, другую — держите выпрямленной (обе ноги касаются пола). Поднимите выпрямленную ногу так высоко, как только можете, стараясь не сгибать её в колене. Затем медленно опустите ногу на пол. Повторите 10 раз (каждой ногой).
Повторите 10 раз (каждой ногой).
Полуприседания
Цель: укрепление икроножных мышц и мышц бедра.
Стойте прямо, опираясь одной рукой на спинку стула, ноги — вместе. Медленно приседайте, сгибая ноги в коленях, стараясь держать при этом спину прямой. Затем вернитесь в исходное положение. Повторите 10 раз.
Сгибание ног
Цель: укрепление мышц бедер и голеней.
Лежа на спине, согните правую ногу в колене, левую — держите выпрямленной. Возьмите левой рукой колено правой ноги и потяните согнутую ногу влево. Удерживайте ногу в таком положении, считая до «20». Повторите 10 раз в каждую сторону. Повторите упражнение с согнутой левой ногой.
Лягте на живот. Согните одну ногу в колене, пытаясь дотянуться пяткой до задней поверхности бедра. Вы должны почувствовать легкое напряжение мышц задней поверхности бедер. Затем верните ногу в исходное положение. Повторите 10 раз каждой ногой.
Упражнения для улучшения движений в коленных суставах
Цель: улучшение подвижности в коленных суставах и увеличение силы в ногах.
Сидя на стуле, разогните одну ногу в коленном суставе, затем верните в исходное положение. Повторите каждой ногой 10 раз. Сидя на стуле, поднимите одну ногу и положите её на маленький стульчик (табурет). Затем положите руки на колено выпрямленной ноги и потянитесь вперед. Вы должны почувствовать легкое напряжение мышц задней поверхности ноги. Оставайтесь в этом положении, считая до 20. Затем расслабьтесь. Повторите упражнение 5 раз.
Напряжение и расслабление мышц бедра и голени Цель: укрепление мышц бедра и икроножных мышц. Станьте боком к спинке стула и обопритесь на неё рукой. Поставьте одну ногу вперед на 50 см, а другую поставьте кзади. Теперь согните выдвинутую вперед ногу в колене и, постепенно опускайтесь, перенося тяжесть тела на выдвинутую и согнутую в колене ногу. Когда Вы полностью «присядете» на выставленную вперед ногу постарайтесь почувствовать напряжение её мышц и растяжение мышц «оставленной» сзади ноги. Оставайтесь в таком положении, считая до 20, затем расслабьтесь, и вернитесь в исходное положение. Повторите по 5 раз (каждой ногой).
Оставайтесь в таком положении, считая до 20, затем расслабьтесь, и вернитесь в исходное положение. Повторите по 5 раз (каждой ногой).
Подъем на носках
Цель: укрепление икроножных мышц.
Стойте прямо, опираясь руками на спинку стула. Приподнимайтесь на носках.
Повторите 10 раз.
Упражнения для мышц лица
Эти упражнения целесообразно выполнять перед зеркалом. Цель: увеличение объема движений мышц лица, улучшение мимики.
Попробуйте изобразить различные эмоции: радость, удивление, гнев и др. Сожмите губы, затем растяните их широко так, чтобы максимально разошлись углы рта, скажите с напряжением слово «сы-ы-ыр». Задерживайте каждое движение на несколько секунд.
Поднимайте и опускайте брови, нахмурьтесь как можно сильнее; поднимите брови и раскройте глаза и выразите крайнее удивление. Высуньте язык и медленно двигайте кончиком языка от одного угла рта до другого.
Откройте рот и кончиком языка проведите круговым движением по губам.
Некоторые дополнительные советы, которые помогут Вам преодолеть затруднения в повседневной двигательной активности Ходьба Здоровый человек не задумывается о том, как у него совершается ходьба. У больного с болезнью Паркинсона ходьба затруднена из-за скованности и замедления движений.
Когда Ваш врач и Вы программируете ЛФК-упражнения для улучшения ходьбы, Вы вместе должны подумать о следующем:
-
Вам следует определить («прочувствовать») удобный для Вас ритм и темп ходьбы. Не стесняйтесь командовать себе «левой-правой» или «раз-два-три-четыре».
-
Никто, кроме Вас, не знает, какой ритм и темп ходьбы является для Вас наиболее подходящим. Определяйте темп и ритм сами таким, чтобы это по возможности не отличалось от ходьбы здорового человека. А для этого не следует, во-первых, спешить, а во-вторых, не следует идти медленнее, чем Вы можете.

-
При выполнении любых упражнений ЛФК старайтесь «поймать и почувствовать» нужный и подходящий для Вас темп и ритм ходьбы.
-
Не щадите себя, заставляйте себя ходить как можно дальше и лучше.
-
Следите за своей ходьбой.Вы должны преодолеть «шаркающую» походку. Для этого достаточно выбрать нужный темп и ритм ходьбы. Пусть «шаркающие» звуки Вас самого раздражают. Добивайтесь бесшумной походки. Занимаясь упражнениями ЛФК, уделите этому вопросу особое внимание.
-
При ходьбе не забывайте о тех затруднениях, которые готовит Вам неровная дорога. Будьте внимательны. Замечайте все неровности и другие неудобные особенности дороги, по которой Вы держите свой путь.
-
Все это особенно важно, если Вы несете домой покупки — Вы можете при падении получить травмы и повредить то, что Вы несете.

Занимаясь ЛФК, посвятите должное внимание и время тренировке ходьбы.
Равновесие
Если у Вас затруднение движений сопровождается нарушением равновесия, то при выполнении программы ЛФК этому должно быть уделено специальное внимание. Такие тренировочные упражнения, конечно, лучше отработать дома — в комнатах и коридорах Вашей квартиры.
Выполнение движений, обеспечивающих хорошее равновесие, требует целого ряда условий:
-
Абсолютное внимание — Вы должны строго следить за дорогой, по которой Вам предстоит пройти. Если это в квартире — то перед Вами пол, покрытый лаком, или линолеум с нежелательной лужей от случайно пролитого Вами чая, или плиточное покрытие пола.
-
Во всех случаях все особенности Вашего передвижения -будь это дома или на улице, Вы — должны принимать во внимание и учитывать с целью своей безопасности.
-
Для отработки мер, обеспечивающих Ваше равновесие во время ходьбы, следует тренироваться в специальных устройствах, которые у спортсменов называются «параллельные брусья», или пользоваться Зх-4х-опорным «козелком», или — идеально — палкой.
 Все трудности, сопровождающие Вашу ходьбу, особенно на неровной дороге или на лестнице, должны быть преодолены путем многократных тренировок.
Все трудности, сопровождающие Вашу ходьбу, особенно на неровной дороге или на лестнице, должны быть преодолены путем многократных тренировок.
-
В домашней обстановке следует тренировать свое равновесие в условиях «выключения зрения» (зрительного контроля). Это следует делать только при наличии в Вашей квартире специально укрепленных на стене перил (деревянная или металлическая планка на стене).
-
Все упражнения по поддержанию хорошего качества ходьбы и равновесия должны осуществляться ежедневно.
Речевые упражнения
В связи с нарушением нормальной функции речедвигательной мускулатуры бывают затруднения речи. При этом Ваши родные и близкие иногда перестают Вас понимать. Это рождает взаимное раздражение, а иногда и ссоры. Первое, что следует сделать — Вы вместе со своим врачом должны объяснить своим близким Ваши трудности и, тем самым, снять взаимное раздражение и недопонимание.
В то же время, в программу ЛФК входят и упражнения по улучшению речи. Идеально, если Вы начнете заниматься со специалистом-логопедом. Но и в том случае, если нет такой возможности, Вы можете сами заниматься ЛФК для улучшения речи. Для этого есть несколько возможностей и вариантов. Самое главное — и это никто не сделает, кроме Вас — Вы должны определить оптимальный темп и ритм речи.
Это можно сделать с помощью разных упражнений. Первое — Вы берете свою любимую книгу и начинаете читать вслух. При этом Вы выбираете удобный для Вас ритм и темп речи. Второе — Вы пытаетесь повторить текст за диктором радио и телевидения. Конечно, в этом случае за образец Вы должны выбрать спокойного диктора, который говорит в нормальном темпе.
Третье — целый ряд текстов разговорного характера Вы должны отрепетировать заранее и при необходимости выговаривать их в удобном для Вас ритме. В любом случае, Вы никогда не должны стесняться, и предупредите своего собеседника, что Вы говорите очень медленно и, кстати говоря, пусть он приспосабливается к ритму и темпу разговора, который удобен Вам.
Письмо
В связи с особенностями двигательных нарушений при болезни Паркинсона может нарушаться и письмо. Слова и буквы могут стать неразборчивыми, и тогда написанное не удастся прочесть, в некоторых случаях даже самому больному.
Начиная писать строку, больной обычно пишет удовлетворительно. Но по мере продолжения написания этой строки почерк становится все более и более неразборчивым. И в этих случаях нужна «ЛФК почерка». Чему она должна быть подчинена? Опять-таки отработке индивидуального темпа и ритма письма. Напоминаем, что Вы в начале строки пишете удовлетворительно, и только потом буквы становятся неразборчивыми. Поэтому надо резко снизить темп написания письма, записок и других рукописных текстов. Однако, в этих условиях написание письма (или какого-то иного текста) может превратиться в тяжелую работу, когда текст рождается «через час по чайной ложке». В этом случае Вам следует воспользоваться пишущей машинкой, но еще лучше печатать текст на клавишах компьютера. Не такая уж это сложная наука, чтобы Вы не овладели печатанием текста на компьютере, ведь там достаточно легкого касания, а на «выходе» получается идеальный текст, напечатанный любым заданным шрифтом.
Не такая уж это сложная наука, чтобы Вы не овладели печатанием текста на компьютере, ведь там достаточно легкого касания, а на «выходе» получается идеальный текст, напечатанный любым заданным шрифтом.
В нашем центре есть возможность получить все необходимое лечение, проконсультироваться с врачом.
Камптокормия: синдром искривления позвоночника, обновление
Eur Spine J. 2010 Aug; 19(8): 1229–1237.
Опубликовано онлайн 2010 март 19. DOI: 10.1007/S00586-010-1370-5
, 1 , 2 , 3 , 1 и 4
. и Информация о лицензии Отказ от ответственности
Камптокормия, также называемая синдромом искривления позвоночника (BSS), определяется как ненормальное сгибание туловища, появляющееся в положении стоя, усиливающееся при ходьбе и уменьшающееся в положении лежа. Первоначально BSS рассматривался, особенно в военное время, как психогенное расстройство. В настоящее время признано, что в дополнение к психическим синдромам многие случаи редуцированного BSS имеют соматическое происхождение, связанное с рядом мышечно-скелетных или неврологических расстройств. Большинство BSS мышечного происхождения связано с первичной идиопатической аксиальной миопатией с поздним началом, прогрессирующей у пожилых пациентов. Диагноз аксиальной миопатии впервые описан Laroche et al. основан на КТ/МРТ исследовании, демонстрирующем массивную жировую инфильтрацию паравертебральных мышц. Неспецифический гистологический аспект включает обширный эндомизиальный фиброз и жировую ткань с неправильной дегенерацией волокон. Слабость паравертебральных мышц может быть вторичной по отношению к целому ряду заболеваний, вызывающих диффузные патологические изменения в мышечной ткани. BSS может быть преобладающим, а иногда и показательным симптомом более генерализованного мышечного расстройства. Причины вторичного BSS многочисленны. Их необходимо тщательно оценить и исключить, прежде чем рассматривать диагноз первичной аксиальной миопатии.
В настоящее время признано, что в дополнение к психическим синдромам многие случаи редуцированного BSS имеют соматическое происхождение, связанное с рядом мышечно-скелетных или неврологических расстройств. Большинство BSS мышечного происхождения связано с первичной идиопатической аксиальной миопатией с поздним началом, прогрессирующей у пожилых пациентов. Диагноз аксиальной миопатии впервые описан Laroche et al. основан на КТ/МРТ исследовании, демонстрирующем массивную жировую инфильтрацию паравертебральных мышц. Неспецифический гистологический аспект включает обширный эндомизиальный фиброз и жировую ткань с неправильной дегенерацией волокон. Слабость паравертебральных мышц может быть вторичной по отношению к целому ряду заболеваний, вызывающих диффузные патологические изменения в мышечной ткани. BSS может быть преобладающим, а иногда и показательным симптомом более генерализованного мышечного расстройства. Причины вторичного BSS многочисленны. Их необходимо тщательно оценить и исключить, прежде чем рассматривать диагноз первичной аксиальной миопатии. Основные этиологии включают, с одной стороны, воспалительные миопатии, мышечные дистрофии с поздним началом, миотонические миопатии, эндокринные и метаболические миопатии, а с другой стороны, неврологические расстройства, главным образом болезнь Паркинсона. Камптокормия при паркинсонизме вызывается аксиальной дистонией, которая является отличительной чертой болезни Паркинсона. Специфического фармакологического лечения первичной аксиальной миопатии не существует. Следует поощрять общую активность, ходьбу с тростью, лечебную физкультуру, гимнастику. Лечение вторичных форм BSS зависит от разновидности расстройства, вызывающего мышечную патологию. Фармакологическое и общее лечение камптокормии при болезни Паркинсона сочетается с таковой при паркинсонизме. Лечение леводопой, обычно воздействующее на ригидность опухоли и акинезию, оказывает слабое или отрицательное влияние на BSS.
Основные этиологии включают, с одной стороны, воспалительные миопатии, мышечные дистрофии с поздним началом, миотонические миопатии, эндокринные и метаболические миопатии, а с другой стороны, неврологические расстройства, главным образом болезнь Паркинсона. Камптокормия при паркинсонизме вызывается аксиальной дистонией, которая является отличительной чертой болезни Паркинсона. Специфического фармакологического лечения первичной аксиальной миопатии не существует. Следует поощрять общую активность, ходьбу с тростью, лечебную физкультуру, гимнастику. Лечение вторичных форм BSS зависит от разновидности расстройства, вызывающего мышечную патологию. Фармакологическое и общее лечение камптокормии при болезни Паркинсона сочетается с таковой при паркинсонизме. Лечение леводопой, обычно воздействующее на ригидность опухоли и акинезию, оказывает слабое или отрицательное влияние на BSS.
Ключевые слова: Камптокормия, Синдром искривления позвоночника, Аксиальная миопатия, Мышечные дистрофии, Болезнь Паркинсона
В течение многих лет камптокормия, обозначающая вынужденную позу с наклоненным вперед туловищем, считалась связанной с психическими проявлениями. Времена изменились, и теперь хорошо известно, что соматические факторы способны вызывать это хроническое аномальное искривление поясничного отдела позвоночника в положении стоя. Со времен ранней военной литературы [16, 40, 41] произошло много изменений, и теперь стало возможным установить более точный этиологический диагноз. Однако многие аспекты нозологии, классификации, патогенеза и терапии этого синдрома остаются неясными. Поэтому мы решили обновить текущие знания об этом редком, но недействительном симптоме.
Времена изменились, и теперь хорошо известно, что соматические факторы способны вызывать это хроническое аномальное искривление поясничного отдела позвоночника в положении стоя. Со времен ранней военной литературы [16, 40, 41] произошло много изменений, и теперь стало возможным установить более точный этиологический диагноз. Однако многие аспекты нозологии, классификации, патогенеза и терапии этого синдрома остаются неясными. Поэтому мы решили обновить текущие знания об этом редком, но недействительном симптоме.
Мы провели обзор литературы на английском и французском языках по «камптокормии» и «синдрому искривления позвоночника» с 1991 по 2009 год с использованием базы данных PubMed. Этот поиск выявил в общей сложности 121 статью, включая 12 обзоров. Метаанализа или систематического обзора обнаружено не было. Сорок шесть статей были посвящены болезни Паркинсона, связанной с камптокормией. Остальные статьи касались мышечной патологии. Мы критически проанализировали опубликованные материалы. Среди них мы отобрали наиболее подходящие статьи, также принимая во внимание личные сообщения и наш собственный опыт лечения этого заболевания, чтобы составить всесторонний описательный обзор малоизученной сущности.
Среди них мы отобрали наиболее подходящие статьи, также принимая во внимание личные сообщения и наш собственный опыт лечения этого заболевания, чтобы составить всесторонний описательный обзор малоизученной сущности.
Камптокормия характеризуется патологическим изгибом туловища, появляющимся в положении стоя, усиливающимся при ходьбе и уменьшающимся в положении лежа. Термин камптокормия иногда называют «синдромом искривления позвоночника» (BSS). Аномальное искривление должно быть поясничным кифозом. Переднее сгибание на 45° или более необходимо для того, чтобы дифференцировать BSS от кифоза, начинающегося с дорсального отдела позвоночника, часто наблюдаемого у пожилых людей (рис. ).
Открыть в отдельном окне
Клиническая фотография, показывающая согнутую позу ( a ), уменьшающуюся в положении лежа ( b )
История синдрома подробно рассмотрена Karkowski [18]. Слово камптокормия было впервые использовано Souques и Rosanoff в 1915 году на собрании «Societé de Neurologie de Paris». Предлагая это название, происходящее от греческих слов camptos (согнутый) и kormos (ствол), эти авторы стремились объединить в единое целое аномальное искривление туловища, которое ранее обозначалось различными терминами. В серии последовательных статей Souques и сотрудники [40, 41] прекрасно описали синдром в том виде, в каком он теперь признан и определен. В своем отчете о 16 пациентах они обратили внимание на то, что психогенное происхождение, как правило, можно было идентифицировать. Большинство их пациентов состояли из раненых солдат, которые не могли справиться с боевым стрессом. Их лечили психотерапией и электротерапией, некоторые из них с успехом.
Предлагая это название, происходящее от греческих слов camptos (согнутый) и kormos (ствол), эти авторы стремились объединить в единое целое аномальное искривление туловища, которое ранее обозначалось различными терминами. В серии последовательных статей Souques и сотрудники [40, 41] прекрасно описали синдром в том виде, в каком он теперь признан и определен. В своем отчете о 16 пациентах они обратили внимание на то, что психогенное происхождение, как правило, можно было идентифицировать. Большинство их пациентов состояли из раненых солдат, которые не могли справиться с боевым стрессом. Их лечили психотерапией и электротерапией, некоторые из них с успехом.
До недавнего времени камптокормию обычно рассматривали как конверсионную реакцию, наблюдаемую главным образом у солдат во время Первой и Второй мировых войн. Например, Sandler [34] в 1947 году сообщил о серии пациентов, в основном солдат, с острым наклоном вперед, который был диагностирован как истерическая контрактура. Как подчеркивает Карковски [18], очень мало статей было опубликовано после Второй мировой войны. В этот период камптокормия еще считалась психогенной. Постепенно в отчетах, опубликованных в 1990-х годов и позднее стало очевидным, что помимо психических синдромов, в основном наблюдавшихся в военное время, с этим аномальным сгибанием туловища связано множество других мышечно-скелетных или неврологических нарушений. Поскольку развитию этого синдрома могут способствовать различные механизмы, был предложен термин «синдром искривления позвоночника» [36] вместо камптокормии, сохранявшей в медицинском сообществе сильную психиатрическую коннотацию. Настоящие авторы согласны с тем, что термин «синдром искривления позвоночника» (BSS) предпочтительнее.
В этот период камптокормия еще считалась психогенной. Постепенно в отчетах, опубликованных в 1990-х годов и позднее стало очевидным, что помимо психических синдромов, в основном наблюдавшихся в военное время, с этим аномальным сгибанием туловища связано множество других мышечно-скелетных или неврологических нарушений. Поскольку развитию этого синдрома могут способствовать различные механизмы, был предложен термин «синдром искривления позвоночника» [36] вместо камптокормии, сохранявшей в медицинском сообществе сильную психиатрическую коннотацию. Настоящие авторы согласны с тем, что термин «синдром искривления позвоночника» (BSS) предпочтительнее.
Этиологию BSS можно разделить на два основных раздела: с одной стороны, мышечного происхождения; с другой стороны, связь с различными неврологическими расстройствами. Как подчеркивают Azher et al. [2] распределение этиологий варьируется в зависимости от схемы направления. Большинство пациентов с мышечными расстройствами, скорее всего, будут обследованы в ортопедической или ревматологической клинике. И наоборот, пациенты, имеющие ассоциацию с неврологическим заболеванием, будут лечиться в центре неврологических и двигательных расстройств. Мы обсудим по очереди эти две основные этиологии.
И наоборот, пациенты, имеющие ассоциацию с неврологическим заболеванием, будут лечиться в центре неврологических и двигательных расстройств. Мы обсудим по очереди эти две основные этиологии.
У этой категории больных СБШ обусловлен слабостью паравертебральных мышц, связанной с деградацией мышечных тканей, независимо от их иннервации. В положении стоя на двигательные сегменты действует изгибающий момент вперед, который должен уравновешиваться выпрямляющими мышцами позвоночника. Недостаточность этих мышц приводит к нарушению равновесия между постуральными мышцами спины и живота, что приводит к наклону туловища вперед. Гипотонус этих мышц объясняет полную вправимость искривления при пассивных движениях и в положении лежа.
Слабость мышц-разгибателей позвоночника может быть вторичной по отношению к различным заболеваниям, вызывающим патологические изменения в антигравитационных мышцах, участвующих в разгибании туловища, или первичной идиопатической.
Вторичный BSS
Вторичный BSS наблюдался при широком спектре генерализованных мышечных заболеваний (таблица). Его действительно можно встретить при полимиозите и дерматомиозите, где в ряде случаев BSS был показательным симптомом [8]. Диагноз ставится на основании характерной картины ЭМГ, повышения уровня креатинкиназы в сыворотке, кожных поражений, воспалительного синдрома и некроза мышечных волокон с массивными периваскулярными и эндомизиальными воспалительными инфильтратами при биопсии.
Его действительно можно встретить при полимиозите и дерматомиозите, где в ряде случаев BSS был показательным симптомом [8]. Диагноз ставится на основании характерной картины ЭМГ, повышения уровня креатинкиназы в сыворотке, кожных поражений, воспалительного синдрома и некроза мышечных волокон с массивными периваскулярными и эндомизиальными воспалительными инфильтратами при биопсии.
Таблица 1
Синдром вторичного изогнутого позвоночника, связанный с мышечными расстройствами
| Причины миопатии |
|---|
| Дистрофия | 63 | Дистрофия | 900363 | Дистрофия | 96363 | Dystrophy | 9.Dystrophy | 7707063. |
| Нервно-мышечные расстройства |
| Миотоническая мышечная дистрофия |
| Болезнь Штейнерта |
| Inflammatory |
| Focal myositis |
| Dermatomyositis |
| Polymyositis |
| Inclusion body myositis |
| Endocrine-metabolic |
| Hypothyroidism |
| Osteomalacia |
| Steroid induced |
| Амилоидоз |
| Митохондриальные миопатии |
| Дефицит карнитинпальмитилтрансферазы |
| Дефицит комплексов дыхательной цепи |
Открыто в отдельном окне
BSS также сообщалось при «миозите с тельцами включения», другом воспалительном заболевании мышц. Биопсия мышц может показать несколько общих результатов, включая эндомизиальные воспалительные клетки, цитоплазматическую вакуолярную дегенерацию, включения или бляшки аномальных белков [15].
Биопсия мышц может показать несколько общих результатов, включая эндомизиальные воспалительные клетки, цитоплазматическую вакуолярную дегенерацию, включения или бляшки аномальных белков [15].
BSS может быть частью симптоматики мышечных дистрофий с поздним началом, включая конечностно-поясные и фасциально-лопаточно-плечевые типы, дополнительно идентифицируемые по типу наследования, ответственному гену и дефицитному белку [12]. Аналогичным образом сообщалось о BSS при миотонических миопатиях, включая болезнь Штейнерта [32] и проксимальную миотоническую миопатию. Последнее расстройство было недавно идентифицировано Serratrice et al. как новая причина вторичного BSS. [37]. Впервые описан Ricker et al. [30], проксимальная миотоническая миопатия передается по аутосомно-доминантному типу наследования. Диагноз этого состояния основывается на диффузных болях и миалгиях, нарушениях походки, слабости проксимальных мышц, катаракте и электрической миотонии.
Приобретенная миопатия классической этиологии может вызывать аномальные позы и вторичный BSS. Это случай миопатий, выявленных при метаболических или эндокринных нарушениях, таких как гипотиреоз, остеомаляция или мышечная дистрофия, вызванная терапией стероидами [8, 14, 38]. Следовательно, при вправимом искривлении позвоночника обязательными являются исследование костного метаболизма и визуализация скелета, а также оценка уровня гормонов щитовидной железы. Наконец, сообщалось о двух исключительных случаях вторичного BSS [8]. Первый касался амилоидной миопатии, распознаваемой по выявлению в биоптатах амилоидных отложений, содержащих легкие цепи лямбда-иммуноглобулина, подобные тем, которые выявляются при иммуноэлектрофорезе крови. Вторым был случай митохондриальной миопатии, обнаруженной по наличию «красных рваных волокон» в биопсии мышц и по потере ферментативной активности митохондриальных дыхательных цепей.
Это случай миопатий, выявленных при метаболических или эндокринных нарушениях, таких как гипотиреоз, остеомаляция или мышечная дистрофия, вызванная терапией стероидами [8, 14, 38]. Следовательно, при вправимом искривлении позвоночника обязательными являются исследование костного метаболизма и визуализация скелета, а также оценка уровня гормонов щитовидной железы. Наконец, сообщалось о двух исключительных случаях вторичного BSS [8]. Первый касался амилоидной миопатии, распознаваемой по выявлению в биоптатах амилоидных отложений, содержащих легкие цепи лямбда-иммуноглобулина, подобные тем, которые выявляются при иммуноэлектрофорезе крови. Вторым был случай митохондриальной миопатии, обнаруженной по наличию «красных рваных волокон» в биопсии мышц и по потере ферментативной активности митохондриальных дыхательных цепей.
При наличии аксиальной миопатии необходимо систематически искать эти различные причины вторичного BSS. Их специфические клинико-лабораторные признаки позволяют проводить дифференциальную диагностику. Точно так же фиксированные невправимые искривления позвоночника, связанные с переломами позвонков, последствиями спондилита и анкилозирующего спондилита, исключаются клиническим обследованием и обычной рентгенограммой дорсолюмбального отдела позвоночника. Поскольку некоторые из этих заболеваний имеют специфические гистологические особенности, биопсия иногда обязательна для точного установления диагноза.
Точно так же фиксированные невправимые искривления позвоночника, связанные с переломами позвонков, последствиями спондилита и анкилозирующего спондилита, исключаются клиническим обследованием и обычной рентгенограммой дорсолюмбального отдела позвоночника. Поскольку некоторые из этих заболеваний имеют специфические гистологические особенности, биопсия иногда обязательна для точного установления диагноза.
Первичный BSS
Анализ литературы и наших собственных случаев показывает, что идиопатический первичный BSS миопатического происхождения наиболее часто встречается в клинической практике. Первичный BSS в настоящее время, по-видимому, представляет собой отдельную клиническую единицу, наблюдаемую у пожилых людей, которые имеют поразительно идентичную клиническую картину с общей картиной визуализации паравертебральных мышц и сходными гистологическими данными [20–22, 26, 36].
В 1991 г. Laroche et al. [22] впервые описали миопатию с поздним началом, ограниченную мышцами позвоночника, у 14 пациентов со средним возрастом 66 лет. Все пациенты имели общее переднее сгибание туловища, вправимое в горизонтальном положении, жировую инфильтрацию паравертебральных мышц на КТ, общий рисунок при биопсии мышц и наличие отягощенного анамнеза. Эти авторы постулировали, что этот приобретенный поясничный кифоз был первичной миопатией с поздним началом, локализованной в паравертебральных мышцах-разгибателях. После этой первой публикации первоначальная гипотеза была подтверждена другими исследователями [11, 14, 26, 28, 36] и дальнейшими исследованиями той же группы [19]., 23].
Все пациенты имели общее переднее сгибание туловища, вправимое в горизонтальном положении, жировую инфильтрацию паравертебральных мышц на КТ, общий рисунок при биопсии мышц и наличие отягощенного анамнеза. Эти авторы постулировали, что этот приобретенный поясничный кифоз был первичной миопатией с поздним началом, локализованной в паравертебральных мышцах-разгибателях. После этой первой публикации первоначальная гипотеза была подтверждена другими исследователями [11, 14, 26, 28, 36] и дальнейшими исследованиями той же группы [19]., 23].
Постепенно подтверждалось, что идиопатический первичный BSS характеризуется прогрессирующей слабостью паравертебральных мышц у пожилых пациентов с преобладанием женского пола. Также был подтвержден частый семейный анамнез. Например, в одном отчете [36] было 2 наследственных случая из 8, в другом — 12 из 23 случаев [31]. Пять из шести пациентов вспомнили аналогичные семейные случаи в серии Mahjneh [26]. Сопутствующие признаки не обнаружены. Неврологическое обследование в норме, особенно тонус, рефлексы и сенсорные функции. Мышечная слабость строго локализована в мышцах-разгибателях позвоночника, и никакой другой мышечный дефицит клинически не обнаруживается. BSS ответственен за серьезную функциональную инвалидность и боль, которые со временем усиливаются [31] и плохо поддаются медикаментозной терапии и реабилитации.
Мышечная слабость строго локализована в мышцах-разгибателях позвоночника, и никакой другой мышечный дефицит клинически не обнаруживается. BSS ответственен за серьезную функциональную инвалидность и боль, которые со временем усиливаются [31] и плохо поддаются медикаментозной терапии и реабилитации.
Изокинетическая оценка была выполнена Laroche et al. [23] с использованием устройства Cibex у 23 пациентов с BSS и 15 контрольных пациентов, сопоставимых по возрасту, полу и телосложению. В позвоночнике пиковые значения крутящего момента и мощности у пациентов были значительно ниже, чем в контрольной группе. Интересно, что работа во время повторяющихся движений с низким сопротивлением и высокой скоростью была наиболее нарушена в группе пациентов, что свидетельствует об утомляемости в дополнение к потере силы и мощности выпрямляющих мышц. Это согласуется с клиническими наблюдениями за пациентами, у которых невозможность стоять прямо появляется постепенно по мере утомления в течение дня или после прохождения определенного расстояния ходьбы. Также оценивались ротаторы плеча и отводящие мышцы бедра. Работа, выполненная после серии из 20 быстрых движений, показала снижение силы в средней ягодичной и лопаточной мышцах. Значение этих последних результатов будет рассмотрено при обсуждении нозологии BSS.
Также оценивались ротаторы плеча и отводящие мышцы бедра. Работа, выполненная после серии из 20 быстрых движений, показала снижение силы в средней ягодичной и лопаточной мышцах. Значение этих последних результатов будет рассмотрено при обсуждении нозологии BSS.
КТ, включающая дорсальные и поясничные отделы паравертебральных мышц, является наиболее информативным диагностическим инструментом [5, 19, 24, 26, 28]. Сходные и характерные аномалии наблюдаются у пациентов с первичным BSS [23, 36]. Типичные, хотя и неспецифические картины включают нормальный параспинальный контур и нормальный объем мышц, которые кажутся гиподенсивными, с потерей вещества, связанной с массивной жировой инфильтрацией (рис. ). Это отличается от нейрогенной атрофии, при которой объем мышц уменьшается, но плотность ткани остается нормальной [5, 24]. Ларош и др. [23] сравнили КТ пациентов с BSS с КТ контрольных субъектов без BSS и с болью в пояснице, вызванной остеоартритом фасеточных суставов или поясничным стенозом. У их 43 пациентов при КТ была выявлена жировая инфильтрация паравертебральной мышцы с преобладанием дистальной головки мышцы и распространением от Т4 до L5, тогда как в контроле атрофия и жировая инфильтрация были центробежными, преобладающими кзади вокруг задней дуги и не столь обширными. как пациенты с BSS. КТ была повторена у 23 пациентов после 3,5-летнего наблюдения [31]. Средняя потеря мышечной плотности составила 6,9.± 16 HU у пациентов. В контрольной группе различий в плотности мышц не наблюдалось. Плотность мышц также измеряли у 43 пациентов и контрольной группы в надостной и средней ягодичных мышцах. Внешний вид надостных мышц у пациентов на КТ был аналогичен таковому в контрольной группе, но со значительно меньшей плотностью. У трех из 43 пациентов были выявлены миопатические изменения средней ягодичной мышцы, сходные с наблюдаемыми в мышцах позвоночника. Кроме того, у 40% этих пациентов было легкое жировое поражение задних мышц бедер и икр. Эти изменения не сопровождались клиническими симптомами или физикальными признаками.
У их 43 пациентов при КТ была выявлена жировая инфильтрация паравертебральной мышцы с преобладанием дистальной головки мышцы и распространением от Т4 до L5, тогда как в контроле атрофия и жировая инфильтрация были центробежными, преобладающими кзади вокруг задней дуги и не столь обширными. как пациенты с BSS. КТ была повторена у 23 пациентов после 3,5-летнего наблюдения [31]. Средняя потеря мышечной плотности составила 6,9.± 16 HU у пациентов. В контрольной группе различий в плотности мышц не наблюдалось. Плотность мышц также измеряли у 43 пациентов и контрольной группы в надостной и средней ягодичных мышцах. Внешний вид надостных мышц у пациентов на КТ был аналогичен таковому в контрольной группе, но со значительно меньшей плотностью. У трех из 43 пациентов были выявлены миопатические изменения средней ягодичной мышцы, сходные с наблюдаемыми в мышцах позвоночника. Кроме того, у 40% этих пациентов было легкое жировое поражение задних мышц бедер и икр. Эти изменения не сопровождались клиническими симптомами или физикальными признаками. Эти данные подчеркивают прогрессирующее ухудшение аксиального мышечного расстройства. Они также указывают на наличие мышечных визуализирующих изменений в других мышцах без мышечной слабости при клиническом обследовании. МРТ-обследование, проведенное другими исследователями [26, 36], выявило аналогичное избирательное и выраженное жировое поражение паравертебральных мышц. Интерес МРТ заключается в получении корональных срезов, показывающих совокупность мышц-разгибателей и разрежение мышечных пучков [36].
Эти данные подчеркивают прогрессирующее ухудшение аксиального мышечного расстройства. Они также указывают на наличие мышечных визуализирующих изменений в других мышцах без мышечной слабости при клиническом обследовании. МРТ-обследование, проведенное другими исследователями [26, 36], выявило аналогичное избирательное и выраженное жировое поражение паравертебральных мышц. Интерес МРТ заключается в получении корональных срезов, показывающих совокупность мышц-разгибателей и разрежение мышечных пучков [36].
Открыть в отдельном окне
КТ идиопатического искривления позвоночника (уровень L5): жировая инфильтрация спинных мышц с постоянным мышечным объемом
Лабораторные исследования обычно в норме. Концентрация креатинкиназы в сыворотке повышена в некоторых случаях: от 2 до 5 раз выше верхней границы нормы в одном исследовании [26] и в 1,5-2 раза выше патологического уровня у 42% в другом исследовании [31]. Иммунологических отклонений не обнаружено. Электромиография спинных мышц иногда затруднена, так как добиться полного расслабления спинных мышц непросто. В одном из исследований у 80% пациентов были обнаружены преобладающие признаки, состоящие из паттерна низкой амплитуды во время произвольного усилия [19].]. В других отчетах результаты не были однородными: в большинстве случаев миопатические, в других — нейропатические или нормальные [26, 36]. ЭМГ нижних конечностей, а также скорость проведения обычно в норме. Однако в одном исследовании миопатические паттерны наблюдались в средней ягодичной и дельтовидной мышцах у шести пациентов без каких-либо клинических симптомов [21].
В одном из исследований у 80% пациентов были обнаружены преобладающие признаки, состоящие из паттерна низкой амплитуды во время произвольного усилия [19].]. В других отчетах результаты не были однородными: в большинстве случаев миопатические, в других — нейропатические или нормальные [26, 36]. ЭМГ нижних конечностей, а также скорость проведения обычно в норме. Однако в одном исследовании миопатические паттерны наблюдались в средней ягодичной и дельтовидной мышцах у шести пациентов без каких-либо клинических симптомов [21].
Во всех исследованиях биопсия мышц выявляет миопатическую картину [20, 26, 36]. Наиболее яркими признаками являются дезорганизация нормальной архитектуры с заменой переменной интенсивности мышечной ткани фиброзом и жировой инфильтрацией. Наблюдается заметное уменьшение количества волокон с изменением их размера (рис. ). Laroche и Delisle [21] сравнили биоптаты параспинальных мышц BSS с образцами мышц пациентов с другими известными заболеваниями позвоночника (поясничный стеноз, грыжа диска). Они наблюдали значительное увеличение эндомизиального фиброза и жировой инфильтрации у пациентов с BSS по сравнению с контрольной группой. Другие аномалии, такие как митохондриальные изменения, обнаруженные в обеих группах, считаются связанными со старостью.
Они наблюдали значительное увеличение эндомизиального фиброза и жировой инфильтрации у пациентов с BSS по сравнению с контрольной группой. Другие аномалии, такие как митохондриальные изменения, обнаруженные в обеих группах, считаются связанными со старостью.
Открыть в отдельном окне
Биопсия мышц позвоночника, показывающая интенсивное эндомизиальное отложение фиброза ( зеленый ) и жировую инфильтрацию. Мы также можем наблюдать неравномерное распределение инволютивных мышечных волокон. (Трихром, оригинальное увеличение ×100)
Нозологию первичного СБШ можно рассматривать двояко: во-первых, можно ли рассматривать первичный СБШ как прогрессирующую мышечную дистрофию? Во-вторых, можно ли связать первичный BSS с одним из признанных типов гетерогенной группы мышечных дистрофий? По определению Эмери [12] «мышечные дистрофии представляют собой группу наследственных заболеваний, характеризующихся прогрессирующей мышечной атрофией и слабостью. Объединяющей чертой является гистологический анализ образцов мышц, который в конечном итоге показывает повышенное количество жира и соединительной ткани с выраженными изменениями размера волокон и участками некроза. Классификация различных разновидностей мышечной дистрофии зависит от топографии мышечной слабости, типа наследования и генов и белковых продуктов, идентифицированных для различных клинических типов дистрофии.
Классификация различных разновидностей мышечной дистрофии зависит от топографии мышечной слабости, типа наследования и генов и белковых продуктов, идентифицированных для различных клинических типов дистрофии.
Следуя этому определению и анализируя несколько работ, посвященных первичному BSS, включая гистологический анализ, кажется уместным заключить, что первичный идиопатический BSS можно включить в группу прогрессирующих мышечных дистрофий с поздним началом. Действительно, при первичном идиопатическом BSS электромиографические исследования преимущественно выявляют миопатический паттерн. Что еще более важно, наследственные случаи обнаруживаются во всех исследованиях, но генетических и молекулярных исследований по-прежнему недостаточно, чтобы оценить способ наследования и, в конечном итоге, ответственный за дефицит белка.
К какой группе признанных типов прогрессирующих мышечных дистрофий обоснованно относится BSS? Поздние формы врожденной миопатии не являются исключением [36], но они обычно не вовлекают аксиальную мускулатуру. Однако недавно сообщалось о таком случае [8]. У 66-летней женщины развился BSS, связанный с болью и слабостью мышц тазового пояса. Биопсия паравертебральных мышц выявила в дополнение к жировой инволюции аномалии волокон типа 1, которые при электронной микроскопии убедительно свидетельствовали о врожденной миопатии. Аналогичный случай также был описан Serratrice et al. [36]. У их пациента биопсия мышц показала параспинальные отпечатки пальцев с преобладанием волокон типа 1. С другой стороны, как уже упоминалось, 40% из 49пациенты, проанализированные в наиболее важной серии литературы [19], имели умеренную жировую инфильтрацию задних мышц бедер на КТ мышц конечностей. У трех из них были поражены обе средние ягодичные мышцы. В семи из восьми случаев, описанных Serratrice et al. [36] была выполнена биопсия мышц конечностей (четырехглавой или дельтовидной мышцы), и был выявлен миопатический паттерн без соответствующих клинических симптомов. В совокупности эти данные показывают, что в некоторых случаях преобладающие аксиальные миопатические поражения распространяются за пределы мышц-разгибателей позвоночника, особенно в мышцах конечностей и пояса.
Однако недавно сообщалось о таком случае [8]. У 66-летней женщины развился BSS, связанный с болью и слабостью мышц тазового пояса. Биопсия паравертебральных мышц выявила в дополнение к жировой инволюции аномалии волокон типа 1, которые при электронной микроскопии убедительно свидетельствовали о врожденной миопатии. Аналогичный случай также был описан Serratrice et al. [36]. У их пациента биопсия мышц показала параспинальные отпечатки пальцев с преобладанием волокон типа 1. С другой стороны, как уже упоминалось, 40% из 49пациенты, проанализированные в наиболее важной серии литературы [19], имели умеренную жировую инфильтрацию задних мышц бедер на КТ мышц конечностей. У трех из них были поражены обе средние ягодичные мышцы. В семи из восьми случаев, описанных Serratrice et al. [36] была выполнена биопсия мышц конечностей (четырехглавой или дельтовидной мышцы), и был выявлен миопатический паттерн без соответствующих клинических симптомов. В совокупности эти данные показывают, что в некоторых случаях преобладающие аксиальные миопатические поражения распространяются за пределы мышц-разгибателей позвоночника, особенно в мышцах конечностей и пояса. Затем можно предположить, что эта ограниченная аксиальная миопатия с поздним началом может быть связана с одним из основных типов мышечных дистрофий, возможно, с группой конечностно-поясной мышечной дистрофии. Однако необходимы дальнейшие исследования для уточнения нозологии, а также патогенеза этого синдрома, которые в настоящее время остаются неизвестными.
Затем можно предположить, что эта ограниченная аксиальная миопатия с поздним началом может быть связана с одним из основных типов мышечных дистрофий, возможно, с группой конечностно-поясной мышечной дистрофии. Однако необходимы дальнейшие исследования для уточнения нозологии, а также патогенеза этого синдрома, которые в настоящее время остаются неизвестными.
BSS сообщается как сопутствующий признак нескольких неврологических заболеваний. В основном они включают расстройства двигательных нейронов, двигательные расстройства и расстройства центральной нервной системы. Несколько случаев BSS наблюдались при ранних проксимальных формах бокового амиотрофического склероза [36]. О нейрогенном происхождении недостаточности мышц-разгибателей позвоночника свидетельствуют сопутствующие периферические мышечные атрофии и другие классические признаки дисфункции передних отделов позвоночника. роговые клетки.
Недавние отчеты показали, что большинство BSS соматического неврологического происхождения возникает в результате поражения и дисфункции базальных ганглиев, скопления ядер в коре головного мозга, включая хвостатое ядро, скорлупу, бледное тело и черную субстанцию. Эта сложная система, помимо прочего, выполняет функцию координации постуральных рефлексов при сгибании и разгибании, что позволяет принимать и поддерживать вертикальное положение [9].]. Эта функция опосредована нейротрансмиттером дофамином, вырабатываемым частью черной субстанции. Роль дофамина имеет решающее значение для всех функций нарушений базальных ганглиев, которые включают классическую форму болезни Паркинсона (БП) и «Паркинсон-плюс-синдромы», такие как множественная системная атрофия и надъядерный паралич [1]. Ключевая роль системы базальных ганглиев в поддержании осевой позы убедительно подтверждается ассоциацией БП и камптокормии с хрусталиковыми и скорлуповыми поражениями [27].
Эта сложная система, помимо прочего, выполняет функцию координации постуральных рефлексов при сгибании и разгибании, что позволяет принимать и поддерживать вертикальное положение [9].]. Эта функция опосредована нейротрансмиттером дофамином, вырабатываемым частью черной субстанции. Роль дофамина имеет решающее значение для всех функций нарушений базальных ганглиев, которые включают классическую форму болезни Паркинсона (БП) и «Паркинсон-плюс-синдромы», такие как множественная системная атрофия и надъядерный паралич [1]. Ключевая роль системы базальных ганглиев в поддержании осевой позы убедительно подтверждается ассоциацией БП и камптокормии с хрусталиковыми и скорлуповыми поражениями [27].
Склонность наклонять туловище вперед является признанным признаком болезни Паркинсона. Постуральный тонус сильно изменен при БП с общей позицией при сгибании. При стоянии или ходьбе голова и туловище больного слегка наклонены вперед. Камптокормия при БП определяется как большое переднее сгибание туловища на 45° и более [2, 3]. В некотором смысле BSS при БП представляет собой карикатурное преувеличение обычного прогиба назад, связанного с аксиальной дистонией, которая является отличительной чертой паркинсонизма [10, 17, 29]., 39].
В некотором смысле BSS при БП представляет собой карикатурное преувеличение обычного прогиба назад, связанного с аксиальной дистонией, которая является отличительной чертой паркинсонизма [10, 17, 29]., 39].
В исследованиях были предприняты попытки описать клинические характеристики пациентов с БП и BSS, а также характеристики BSS при БП [2, 3, 25]. Некоторые признаки являются общепризнанными: пожилой возраст, длительное течение паркинсонизма, развитие согнутой позы всегда следует за первыми симптомами паркинсонизма. Камптокормия обычно проявляется прогрессивно в течение года и более, но иногда и в течение нескольких недель [2, 3, 25]. Сгибание туловища сильно выражено и у значительной части пациентов связано со сколиозом [42]. Следует отметить, что BSS при БП также может выявляться у ограниченной группы пациентов с диссоциированной формой БП, при которой аксиальная дистония является преобладающим выявляющим симптомом. Авторы настоящей статьи сталкивались с такими пациентами с нормальной паравертебральной МРТ и очень тонкими признаками паркинсонизма. В единственном литературном исследовании случай-контроль Bloch et al. [3] сравнили выбранную выборку пациентов с БП и BSS с подобранными пациентами с PD без BSS. Основные характеристики, выявленные у пациентов с БП и BSS, включали аксиальную ригидность, постуральную нестабильность и нарушения походки, все признаки соответствовали аксиальной дистонии туловища с чрезмерной активацией мышц брюшной стенки. Лечение леводопой не влияет на камптокормию. Однако ригидность, тремор и акинезия, также присутствующие у пациентов с БП с BSS, по крайней мере частично реагируют на дофаминовую терапию [2, 3, 25]. Это дихотомическое действие дофамина предполагает, что БП с BSS представляет собой специфическую форму паркинсонизма, при которой возникает дополнительная недофаминергическая нейрональная дисфункция в базальных ганглиях и системе ствола мозга [3].
В единственном литературном исследовании случай-контроль Bloch et al. [3] сравнили выбранную выборку пациентов с БП и BSS с подобранными пациентами с PD без BSS. Основные характеристики, выявленные у пациентов с БП и BSS, включали аксиальную ригидность, постуральную нестабильность и нарушения походки, все признаки соответствовали аксиальной дистонии туловища с чрезмерной активацией мышц брюшной стенки. Лечение леводопой не влияет на камптокормию. Однако ригидность, тремор и акинезия, также присутствующие у пациентов с БП с BSS, по крайней мере частично реагируют на дофаминовую терапию [2, 3, 25]. Это дихотомическое действие дофамина предполагает, что БП с BSS представляет собой специфическую форму паркинсонизма, при которой возникает дополнительная недофаминергическая нейрональная дисфункция в базальных ганглиях и системе ствола мозга [3].
Точная распространенность BSS при БП точно не известна. В разных исследованиях оценивались разные показатели. Лепутр и др. [25] набрали 23 последовательных случая BSS из 700 пациентов, что дало гипотетическую распространенность около 3%. Ажер и др. [2] обнаружили 21 случай BSS из 164 PD, что дает распространенность 12%. В более позднем исследовании Tiple et al. обнаружили распространенность в пределах 6,9%. В этом последнем исследовании 275 последовательных пациентов прошли скрининг на BSS путем клинической оценки, а пациенты, у которых был положительный результат скрининга на камптокормию, впоследствии были обследованы с помощью гониометрического анализа. Достоверность клинического обследования при оценке камптокормии (сгибание вперед > 45°) оценивали в выборке с использованием гониометрических измерений в качестве стандарта. Клиническое обследование показало 100% чувствительность и 90% специфичность в диагностике камптокормии [42].
Ажер и др. [2] обнаружили 21 случай BSS из 164 PD, что дает распространенность 12%. В более позднем исследовании Tiple et al. обнаружили распространенность в пределах 6,9%. В этом последнем исследовании 275 последовательных пациентов прошли скрининг на BSS путем клинической оценки, а пациенты, у которых был положительный результат скрининга на камптокормию, впоследствии были обследованы с помощью гониометрического анализа. Достоверность клинического обследования при оценке камптокормии (сгибание вперед > 45°) оценивали в выборке с использованием гониометрических измерений в качестве стандарта. Клиническое обследование показало 100% чувствительность и 90% специфичность в диагностике камптокормии [42].
Аксиальная дистония считается причиной камптокормии при БП большинством исследователей [3, 17, 25, 29]. BSS и сколиоз могут представлять собой один конец спектра аномальных поз при БП, а другой конец — деформация полосатых кистей и стоп [1, 2]. Однако совсем недавно очаговая миопатия была продемонстрирована у некоторых пациентов с БП с помощью ЭМГ, КТ и МРТ, а также биопсии параспинальных мышц [6, 25, 35, 44]. В 2002 г. Wunderlich et al. [44] описали случай камптокормии у пациента с БП, клинические признаки которого включали боль и воспаление паравертебральных мышц, сопровождавшиеся значительным повышением уровня креатинкиназы. Данные МРТ и биопсии характерны для очагового миозита. Очаговый миозит, впервые описанный в 1977 двумя независимыми исследователями, Cumming и Heffner [7, 13], представляет собой редкое заболевание, характеризующееся гипертрофией и воспалением одной мышцы или одной группы мышц. Патогенез не известен; эволюция обычно самоограничена, оставаясь локализованной. Сообщалось также о распространении полимиозита. Характерные гистологические признаки фокального миозита включают значительный перимизиальный и эндомизиальный воспалительный инфильтрат, связанный с некрозом, заметными вариациями размеров волокон и фиброзом [4]. После публикации Wunderlich несколько исследователей выполнили биопсию мышц позвоночника, когда на грудо-поясничной МРТ у пациентов с БП наблюдались аномалии сигнала.
В 2002 г. Wunderlich et al. [44] описали случай камптокормии у пациента с БП, клинические признаки которого включали боль и воспаление паравертебральных мышц, сопровождавшиеся значительным повышением уровня креатинкиназы. Данные МРТ и биопсии характерны для очагового миозита. Очаговый миозит, впервые описанный в 1977 двумя независимыми исследователями, Cumming и Heffner [7, 13], представляет собой редкое заболевание, характеризующееся гипертрофией и воспалением одной мышцы или одной группы мышц. Патогенез не известен; эволюция обычно самоограничена, оставаясь локализованной. Сообщалось также о распространении полимиозита. Характерные гистологические признаки фокального миозита включают значительный перимизиальный и эндомизиальный воспалительный инфильтрат, связанный с некрозом, заметными вариациями размеров волокон и фиброзом [4]. После публикации Wunderlich несколько исследователей выполнили биопсию мышц позвоночника, когда на грудо-поясничной МРТ у пациентов с БП наблюдались аномалии сигнала. За возможным исключением случая, описанного Charpentier et al. [6], рассматриваемый авторами как истинный очаговый миозит, случаи, описанные Shabitz, а затем Lepoutre, не соответствовали диагнозу очагового миозита [25, 35]. Аномалии, описанные Shabitz, включали хроническую воспалительную миопатию, неспецифические миопатические изменения или митохондриальную миопатию. Гистологические данные, о которых сообщил Lepoutre, в основном показали фиброз и жировую инфильтрацию. В настоящее время распространенность миопатических поражений при БП с камптокормией неизвестна; документов мало, и необходимы дальнейшие исследования для оценки точной роли мышечных изменений в развитии камптокормии при БП, а также их патогенеза.
За возможным исключением случая, описанного Charpentier et al. [6], рассматриваемый авторами как истинный очаговый миозит, случаи, описанные Shabitz, а затем Lepoutre, не соответствовали диагнозу очагового миозита [25, 35]. Аномалии, описанные Shabitz, включали хроническую воспалительную миопатию, неспецифические миопатические изменения или митохондриальную миопатию. Гистологические данные, о которых сообщил Lepoutre, в основном показали фиброз и жировую инфильтрацию. В настоящее время распространенность миопатических поражений при БП с камптокормией неизвестна; документов мало, и необходимы дальнейшие исследования для оценки точной роли мышечных изменений в развитии камптокормии при БП, а также их патогенеза.
Первоочередной задачей является информирование пациента об эволюции и терапевтических возможностях его заболевания.
Специфической фармакологической терапии первичной аксиальной миопатии не существует. Применение анальгетиков зависит от интенсивности болей в спине. Лечение остеопороза, часто связанного с BSS у этих пожилых пациентов, является обязательным для предотвращения остеопоротических переломов позвонков. Важно соблюдать общие принципы управления. Рекомендуется сбалансированное питание и снижение веса, если это необходимо. Следует избегать длительного постельного режима. Следует поощрять активность и ходьбу с тростью или ходунками. Физиотерапия, массаж, упражнения и пассивное движение являются важной частью общего лечения. Соответствующие легкие ортезы могут облегчить передвижение. Они не всегда хорошо переносятся. Как уже упоминалось, ответ на лечение, как правило, плохой, и обычно прогрессирующее ухудшение функциональной нетрудоспособности. Лечение вторичного BSS зависит от разновидности расстройства, вызывающего мышечную патологию. Например, воспалительные миопатии реагируют на стероиды, иногда связанные с терапией циклоспорином или иммуноглобулином [8]. Точно так же истинная гипотиреозная миопатия корректируется адекватным введением тиреоактивных веществ.
Лечение остеопороза, часто связанного с BSS у этих пожилых пациентов, является обязательным для предотвращения остеопоротических переломов позвонков. Важно соблюдать общие принципы управления. Рекомендуется сбалансированное питание и снижение веса, если это необходимо. Следует избегать длительного постельного режима. Следует поощрять активность и ходьбу с тростью или ходунками. Физиотерапия, массаж, упражнения и пассивное движение являются важной частью общего лечения. Соответствующие легкие ортезы могут облегчить передвижение. Они не всегда хорошо переносятся. Как уже упоминалось, ответ на лечение, как правило, плохой, и обычно прогрессирующее ухудшение функциональной нетрудоспособности. Лечение вторичного BSS зависит от разновидности расстройства, вызывающего мышечную патологию. Например, воспалительные миопатии реагируют на стероиды, иногда связанные с терапией циклоспорином или иммуноглобулином [8]. Точно так же истинная гипотиреозная миопатия корректируется адекватным введением тиреоактивных веществ. Другим примером является проксимальная миопатия остеомаляции, когда в дополнение к терапии кальцитриолом лечение должно быть адаптировано к различным причинам остеомаляции.
Другим примером является проксимальная миопатия остеомаляции, когда в дополнение к терапии кальцитриолом лечение должно быть адаптировано к различным причинам остеомаляции.
Фармакологическое и общее лечение камптокормии при болезни Паркинсона сочетается с лечением болезни Паркинсона. К сожалению, лечение леводопой, обычно активное при треморе, ригидности и акинезии, оказывает слабое или отрицательное влияние на камптокормию. Поскольку чрезмерная активация мышц брюшной стенки явно наблюдается у некоторых пациентов с БП с BSS, в одном исследовании [2] сообщается об эффектах инъекции ботулинического токсина (BTI) в прямую мышцу живота в попытке уменьшить гиперактивность мышц живота. У четырех из девяти пациентов, получавших лечение BTI, было заметное улучшение их согнутой осанки, сохранявшееся в течение примерно 3 месяцев после каждой инъекции. Поскольку подвздошно-поясничная мышца традиционно рассматривается как сгибатель поясничного отдела позвоночника, несколько пациентов с БП с BSS получали инъекции BTI в подвздошно-поясничную мышцу под контролем УЗИ с отрицательными результатами в двух исследованиях [33, 43]. В литературе очень мало данных о хирургическом лечении. Пояснично-грудная фиксация была выполнена в нашем учреждении по поводу BSS, связанного с аксиальной миопатией. Пациент, который умолял нас об операции, наконец, добился успешного клинического результата с адекватной коррекцией и костным спондилодезом через 1 год наблюдения, но за счет сложного, сложного и длительного реабилитационного периода. Этот случай указывает на то, что эта процедура может быть альтернативой консервативному лечению. Тем не менее, большинство пациентов с BSS — пожилые люди с сопутствующими заболеваниями, которые исключают возможность хирургического лечения для большинства из них. По нашему мнению, если речь идет об операции, то она должна быть ограничена пациентами, которые сильно мотивированы хорошим общим состоянием здоровья и информированы о том, что это основной вид операции с длительным послеоперационным периодом и риском местных и общих осложнений. Эти рекомендации можно также применить к BSS, связанным с PD.
В литературе очень мало данных о хирургическом лечении. Пояснично-грудная фиксация была выполнена в нашем учреждении по поводу BSS, связанного с аксиальной миопатией. Пациент, который умолял нас об операции, наконец, добился успешного клинического результата с адекватной коррекцией и костным спондилодезом через 1 год наблюдения, но за счет сложного, сложного и длительного реабилитационного периода. Этот случай указывает на то, что эта процедура может быть альтернативой консервативному лечению. Тем не менее, большинство пациентов с BSS — пожилые люди с сопутствующими заболеваниями, которые исключают возможность хирургического лечения для большинства из них. По нашему мнению, если речь идет об операции, то она должна быть ограничена пациентами, которые сильно мотивированы хорошим общим состоянием здоровья и информированы о том, что это основной вид операции с длительным послеоперационным периодом и риском местных и общих осложнений. Эти рекомендации можно также применить к BSS, связанным с PD. Сообщалось о двусторонней стимуляции субталамического ядра при БП у пациентов с BSS [2, 25, 45] с различными результатами, иногда с заметным улучшением [45].
Сообщалось о двусторонней стимуляции субталамического ядра при БП у пациентов с BSS [2, 25, 45] с различными результатами, иногда с заметным улучшением [45].
В настоящее время принято, что аксиальная миопатия является отдельной клинической единицей и является наиболее частой причиной камптокормии у пожилых пациентов [19]. При выявлении у пациента прогрессирующего искривления позвоночника следует применять алгоритм клинических, визуализационных, лабораторных и электрофизиологических исследований для исключения других возможных этиологий камптокормии. Клиническое обследование и сбор анамнеза подтверждают отсутствие сопутствующих признаков, особенно неврологических симптомов и признаков. Визуализирующие исследования включают в первую очередь обзорную рентгенографию для исключения поражений костей или системных заболеваний, таких как анкилозирующий спондилоартрит, ответственный за невправимое искривление позвоночника. КТ и предпочтительно МРТ паравертебральных мышц являются наиболее полезными диагностическими инструментами, демонстрирующими характерные аномалии первичной аксиальной миопатии, в отличие от мышечной атрофии, наблюдаемой у пожилых пациентов с остеоартритом или стенозом позвоночника. КТ или МРТ также должны исследовать мышцы плечевого и тазового пояса и мышцы конечностей, чтобы оценить возможное распространение миопатии. ЭМГ параспинальных мышц и конечностей является частью мышечной и неврологической оценки. Лабораторные исследования включают сывороточную креатинкиназу, скорость оседания и реактивность протеина-С, антитела к ацетилхолиновым рецепторам, исследования функции щитовидной железы, а также другие более специфические исследования для исключения миопатий, вторичных по отношению к различным заболеваниям, вызывающим патологические мышечные изменения. В сомнительных случаях, чтобы исключить какое-либо другое мышечное заболевание, следует провести биопсию паравертебральных мышц в месте, обозначенном с помощью КТ или МРТ, где аномальная мышца не полностью покрыта жировой тканью.
КТ или МРТ также должны исследовать мышцы плечевого и тазового пояса и мышцы конечностей, чтобы оценить возможное распространение миопатии. ЭМГ параспинальных мышц и конечностей является частью мышечной и неврологической оценки. Лабораторные исследования включают сывороточную креатинкиназу, скорость оседания и реактивность протеина-С, антитела к ацетилхолиновым рецепторам, исследования функции щитовидной железы, а также другие более специфические исследования для исключения миопатий, вторичных по отношению к различным заболеваниям, вызывающим патологические мышечные изменения. В сомнительных случаях, чтобы исключить какое-либо другое мышечное заболевание, следует провести биопсию паравертебральных мышц в месте, обозначенном с помощью КТ или МРТ, где аномальная мышца не полностью покрыта жировой тканью.
Мы хотели бы поблагодарить Мариз Лесаж за ее прекрасную секретарскую работу.
1. Ашур Р., Янкович Дж. Деформации суставов и скелета при болезни Паркинсона, множественной системной атрофии и прогрессирующем надъядерном параличе. Мов Беспорядок. 2006; 21:1856–1863. doi: 10.1002/mds.21058. [PubMed] [CrossRef] [Google Scholar]
Мов Беспорядок. 2006; 21:1856–1863. doi: 10.1002/mds.21058. [PubMed] [CrossRef] [Google Scholar]
2. Ажер С.Н., Янкович Дж. Камптокормия: патогенез, классификация и ответ на терапию. Неврология. 2005; 65: 355–359. doi: 10.1212/01.wnl.0000171857.09079.9ф. [PubMed] [CrossRef] [Google Scholar]
3. Bloch F, Houeto JL, Tezena du Montcel S, et al. Болезнь Паркинсона с камптокормией. J Neurol Нейрохирург Психиатрия. 2006; 77: 1223–1228. doi: 10.1136/jnnp.2006.087908. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
4. Bouchaud-Chabot A, Sicre J, Bardin Th, Kahn MF (1996). Очаговые миозиты. В: Кан М.Ф., Кунц и др. (ред.) L’actualité rhumatologique. Французское научное расширение. стр. 55–64
5. Bulke JA, Crolla D, Termote JL, et al. Компьютерная томография мышц. Мышечный нерв. 1981;4:67–72. doi: 10.1002/mus.880040112. [PubMed] [CrossRef] [Google Scholar]
6. Charpentier P, Dauphin A, Stojkovic T, et al. Болезнь Паркинсона, камптокормия и очаговый параспинальный миозит. Преподобный Нейрол. 2005; 161:459–463. doi: 10.1016/S0035-3787(05)85077-5. [PubMed] [CrossRef] [Google Scholar]
Преподобный Нейрол. 2005; 161:459–463. doi: 10.1016/S0035-3787(05)85077-5. [PubMed] [CrossRef] [Google Scholar]
7. Cumming W, Weiser R, Teoh R, et al. Локализованный узловой миозит: клинико-патологический вариант полимиозита. Кью Мед. 1977; 46: 531–546. [PubMed] [Академия Google]
8. Делси В., Хачулла Э., Мишон-Пастрель У. и соавт. La camptocormie: знак осевой миопатии. По поводу замечаний. Преподобный Мед Интерне. 2002; 23: 144–154. doi: 10.1016/S0248-8663(01)00530-6. [PubMed] [CrossRef] [Google Scholar]
9. Dietz V, Zylstra W, Assaiante C, et al. Контроль равновесия при болезни Паркинсона. Осанка походки. 1993; 1: 77–84. doi: 10.1016/0966-6362(93)-V. [CrossRef] [Google Scholar]
10. Djaldetti R, Mosber G, Galili R, Sroka H, et al. Камптокормия у больных болезнью Паркинсона: характеристика и возможный патогенез необычного явления. Мов Беспорядок. 1999;14:443–447. doi: 10.1002/1531-8257(199905)14:3<443::AID-MDS1009>3.0.CO;2-G. [PubMed] [CrossRef] [Google Scholar]
11. Ehrenstein MR, Stoll T, Edwards JCW. Не все сутулости связаны с остеопорозом. Энн Рам Дис. 1996; 55: 21–28. doi: 10.1136/ard.55.1.21. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Ehrenstein MR, Stoll T, Edwards JCW. Не все сутулости связаны с остеопорозом. Энн Рам Дис. 1996; 55: 21–28. doi: 10.1136/ard.55.1.21. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Эмери AEH. Мышечные дистрофии. БМЖ. 1998; 317: 991–995. [Бесплатная статья PMC] [PubMed] [Google Scholar]
13. Heffner R, Armbrustmacher V, Eanle K. Очаговый миозит. Рак. 1977;40:301–306. doi: 10.1002/1097-0142(197707)40:1<301::AID-CNCR2820400142>3.0.CO;2-N. [PubMed] [CrossRef] [Google Scholar]
14. Hilliquin P, Menkes CJ, Laoussadi S, et al. Camptocormie du sujet age: Une nouvelle entité par atteinte des paravertebaux мышц. Рев Рум Мал Остеоартик. 1992; 59: 169–175. [PubMed] [Google Scholar]
15. Hund E, Heckl R, Goebel H, et al. Миозит с тельцами включения, проявляющийся изолированным парезом эрекции позвоночника. Неврология. 1995; 45: 993–994. [PubMed] [Академия Google]
16. Херст А.Ф. Согнутая спина солдат. БМЖ. 1918; 2: 621–623. doi: 10.1136/bmj. 2.3023.621. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
2.3023.621. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
17. Янкович Дж., Тинтнер Р. Дистония и паркинсонизм. Расстройство, связанное с болезнью Паркинсона. 2001; 8: 109–121. doi: 10.1016/S1353-8020(01)00025-6. [PubMed] [CrossRef] [Google Scholar]
18. Карковски К. Старая и новая камптокормия. Позвоночник. 1999; 24:1494–1498. doi: 10.1097/00007632-199907150-00017. [PubMed] [CrossRef] [Академия Google]
19. Laroche M, Curtas P (2008) Полезность компьютерной томографии при синдроме искривления позвоночника (личное сообщение)
20. Laroche M, Delisle MB. Примитивная камптокормия является паравертебральной миопатией. Rev Rhum Mal остеоартроз. 1994; 61: 481–484. [PubMed] [Google Scholar]
21. Laroche M, Delisle MB, Aziza R, et al. Является ли камптокормия первичным мышечным заболеванием? Позвоночник. 1995; 20:1011–1016. doi: 10.1097/00007632-199505000-00007. [PubMed] [CrossRef] [Google Scholar]
22. Laroche M, Delisle MB, Mazieres B, et al. Локализованная миопатия в спиномозговых мышцах: единственная причина развития кифозного кифоза у взрослых. Rev Rhum Mal остеоартроз. 1991;58:829–838. [PubMed] [Google Scholar]
Локализованная миопатия в спиномозговых мышцах: единственная причина развития кифозного кифоза у взрослых. Rev Rhum Mal остеоартроз. 1991;58:829–838. [PubMed] [Google Scholar]
23. Laroche M, Ricq G, Delisle MB. Синдром искривления позвоночника: компьютерная томография и изокинетическая оценка. Мышечный нерв. 2002; 25: 189–193. doi: 10.1002/mus.10016. [PubMed] [CrossRef] [Google Scholar]
24. Laroche M, Rousseau H, Mazieres B, et al. Intérêt де ла томоденситометрия данс ла мышечной патологии. Рев Рум Мал Остеоартик. 1989; 56: 433–439. [PubMed] [Google Scholar]
25. Lepoutre AC, Devos D, Blanchard-Dauphin A. Специфическая клиническая картина камптокормии при болезни Паркинсона. J Neurol Нейрохирург Психиатрия. 2006;77:1229–1234. doi: 10.1136/jnnp.2005.083998. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
26. Mahjneh I, Marconi G, Paetau A, et al. Осевая миопатия — нераспознанная сущность. Дж Нейрол. 2002; 249:730–734. doi: 10.1007/s00415-002-0701-9. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
27. Ньевес А.В., Миясаки Дж.М., Ланг А.Е. Острое начало дистонической камптокормии, вызванной поражением хрусталика. Мов Беспорядок. 2001; 16: 177–180. doi: 10.1002/1531-8257(200101)16:1<177::AID-MDS1035>3.0.CO;2-C. [PubMed] [CrossRef] [Академия Google]
28. Poullin P, Daumen-Legre V, Serratrice G. Camptocormie du sujet age Rev Rhum Mal Osteoartic. 1993; 60: 159–1661. [PubMed] [Google Scholar]
29. Reichel G, Kirchhofer U, Stenner A. Камптокормия-сегментарная дистония. Предложение нового определения старой болезни. Нервенарзт. 2001; 72: 281–285. doi: 10.1007/s001150050751. [PubMed] [CrossRef] [Google Scholar]
30. Ricker K, Koch MC, Lehmann-Horn F, et al. Проксимальная миотоническая миопатия. Клинические признаки мультисистемного расстройства, сходного с миотонической дистрофией. Арх Нейрол. 1995;52:25–31. [PubMed] [Google Scholar]
31. Ricq G, Laroche M. Cyphose lombaire acquise de l’adulte par myopathie примитивных мышц паравертебро.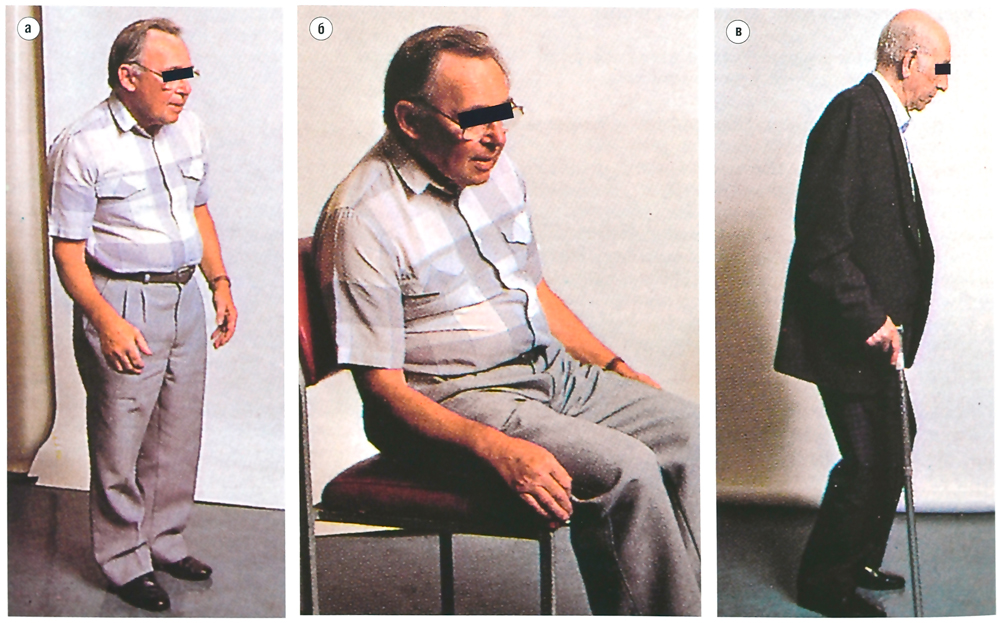 Эпидемиологические аспекты томоденситометрии и эволюции. Группа из 23 пациентов. Рев Рум Мал Остеоартик. 2000;67:908–913. doi: 10.1016/S1169-8330(00)00034-X. [CrossRef] [Google Scholar]
Эпидемиологические аспекты томоденситометрии и эволюции. Группа из 23 пациентов. Рев Рум Мал Остеоартик. 2000;67:908–913. doi: 10.1016/S1169-8330(00)00034-X. [CrossRef] [Google Scholar]
32. Rolland Y, Laroche M (1997) Cyphoses lombaires acquises révélatrices d’une maladie de Steinert. Рахис 9:115–118
33. Сальватори FM. Инъекция ботулотоксина в подвздошно-поясничную мышцу при камптокормии. Мов Беспорядок. 2009; 24:316. [PubMed] [Google Scholar]
34. Sandler SA. Камптокормия или функциональная искривление спины. Психосомат Мед. 1947; 9: 197–204. [PubMed] [Google Scholar]
35. Schabitz WR, Glatz K, Schuhan C, et al. Сильное сгибание туловища вперед при болезни Паркинсона: фокальная миопатия параспинальных мышц, имитирующая камптокормию. Мов Беспорядок. 2003; 18: 408–414. doi: 10.1002/mds.10385. [PubMed] [CrossRef] [Академия Google]
36. Serratrice G, Poujet J, Pelissier JF. Синдром искривления позвоночника. J Neurol Нейрохирург Психиатрия. 1996; 60: 51–54. doi: 10.1136/jnnp.60.1.51. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
doi: 10.1136/jnnp.60.1.51. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
37. Serratrice J, Weiler PJ, Pouget J, Serratrice G. Une call méconnue de camptocormie: la myopathie myotonique proximale. Пресс Мед. 2000;29:1121–1123. [PubMed] [Google Scholar]
38. Serratrice G, Pelissier JF, Cros J. Les atteintes musculaires des osteomalacies. Рев Рум Мал Остеоартик. 1978;45:621–630. [PubMed] [Google Scholar]
39. Slawek J, Derejko M, Lass P. Камптокормия как форма дистонии при болезни Паркинсона. Евр Дж Нейрол. 2003; 10:107–108. doi: 10.1046/j.1468-1331.2003.00503_1.x. [PubMed] [CrossRef] [Google Scholar]
40. Souques A (1914–1915) Контрактуры или псевдоконтрактуры истеро-травматических. Rev Neurol 28:430–431
41. Сукес А., Розанофф-Салов Б. (1914–1915). La camptocormie, искривление туловища, последовательные травматизмы туловища и лопаток, морфологические соображения. Преподобный Нейрол 28: 937–939
42. Tiple D, Fabbrini G, Ottaviani D, et al. Камптокормия при болезни Паркинсона: эпидемиологическое и клиническое исследование. J Neurol Нейрохирург Психиатрия. 2009; 80: 145–148. doi: 10.1136/jnnp.2008.150011. [PubMed] [CrossRef] [Google Scholar]
Камптокормия при болезни Паркинсона: эпидемиологическое и клиническое исследование. J Neurol Нейрохирург Психиатрия. 2009; 80: 145–148. doi: 10.1136/jnnp.2008.150011. [PubMed] [CrossRef] [Google Scholar]
43. Coelin R, Raible A, Gasser T, et al. Инъекция ботулотоксина в подвздошно-поясничную мышцу под контролем УЗИ при камптокормии. Мов Беспорядок. 2008; 23:889–892. doi: 10.1002/mds.21967. [PubMed] [CrossRef] [Google Scholar]
44. Wunderlich S, Csoti I, Bliners K, et al. Камптокормия при болезни Паркинсона, имитирующая очаговый миозит параспинальных мышц. Мов Беспорядок. 2002;17:598–600. doi: 10.1002/mds.10110. [PubMed] [CrossRef] [Google Scholar]
45. Yamada K, Goto S, Matsuzaki K, et al. Облегчение камптокормии путем двусторонней стимуляции субталамических ядер у пациента с болезнью Паркинсона. Расстройство, связанное с паркинсонизмом. 2006;12(6):372–375. doi: 10.1016/j.parkreldis.2006.02.003. [PubMed] [CrossRef] [Google Scholar]
Презентация, этиология, диагностика и лечение камптокормии — полный текст — European Neurology 2010, Vol.
 64, № 1
64, № 1 Камптокормия (синдром искривления позвоночника, истерический кифоз) — аномалия, характеризующаяся выраженным сгибанием грудопоясничного отдела позвоночника вперед, которое обычно усиливается при ходьбе или стоянии и полностью исчезает в положении лежа. Камптокормия может быть обусловлена заболеваниями центральной нервной системы, такими как болезнь Паркинсона, дистония, мультисистемная атрофия или болезнь Альцгеймера, вследствие заболеваний периферической нервной системы, таких как первичная миопатия, вторичная миопатия, заболевание двигательных нейронов, миастения или хроническая воспалительная демиелинизирующая полинейропатия , из-за побочных эффектов медикаментозного лечения, из-за грыжи диска, артрита или травмы позвоночника или из-за паранеоплазии. Лишь в редких случаях камптокормия может быть связана с психическим заболеванием. Диагноз ставится на основании клинических данных, визуализации головного мозга или позвоночника, игольчатой электромиографии или биопсии мышц. Варианты лечения ограничены и часто бесполезны и основаны на консервативных мерах, таких как психотерапия, физиотерапия, использование ортезов, лекарств, инъекции ботулинического токсина, отмена возбудителей, электрошоковая терапия или инвазивные меры, такие как хирургическая коррекция или глубокая стимуляция мозга. . Итог в целом справедлив. Некоторые пациенты получают пользу от терапии, в то время как другие не реагируют на лечение и постепенно становятся неподвижными.
Варианты лечения ограничены и часто бесполезны и основаны на консервативных мерах, таких как психотерапия, физиотерапия, использование ортезов, лекарств, инъекции ботулинического токсина, отмена возбудителей, электрошоковая терапия или инвазивные меры, такие как хирургическая коррекция или глубокая стимуляция мозга. . Итог в целом справедлив. Некоторые пациенты получают пользу от терапии, в то время как другие не реагируют на лечение и постепенно становятся неподвижными.
Введение
Камптокормия, также известная как синдром искривленного позвоночника или истерический кифоз, представляет собой тяжелую инвалидизирующую, неизменяющуюся, приобретенную постуральную аномалию, обусловленную различными причинами, характеризующуюся непроизвольным наклоном вперед грудопоясничного отдела позвоночника [1]. ,2]. Термин камптокормия происходит от греческих слов «камптос» (сгибаться) и «кормос» (хобот) [3]. Аномальная осанка приводит к поясничному кифозу и увеличивается или видна только тогда, когда пациент стоит или ходит [3,4]. Камптокормия чаще всего возникает из-за поражения поперечнополосатых мышц позвоночника, из-за поражения центральной нервной системы (ЦНС) или из-за некоторых редких состояний (таблица 1). Камптокормию следует отличать от синдрома Пизы (плевротонус), характеризующегося тоническим сгибанием туловища и головы в одну сторону наряду со сколиозом. Этот обзор призван обобщить и обсудить недавние результаты и перспективы на будущее, касающиеся клинических проявлений, этиологии, диагностики и лечения камптокормии.
Камптокормия чаще всего возникает из-за поражения поперечнополосатых мышц позвоночника, из-за поражения центральной нервной системы (ЦНС) или из-за некоторых редких состояний (таблица 1). Камптокормию следует отличать от синдрома Пизы (плевротонус), характеризующегося тоническим сгибанием туловища и головы в одну сторону наряду со сколиозом. Этот обзор призван обобщить и обсудить недавние результаты и перспективы на будущее, касающиеся клинических проявлений, этиологии, диагностики и лечения камптокормии.
Таблица 1
Условия, связанные с камптокормией
История
Камптокормия была впервые задокументирована в 17 веке испанским художником Франсиско де Сурбараном. «Функционально искривленный позвоночник» впервые описал Brodie в 1818 г. [5]. Следующее описание под термином «функционально изогнутая спина» было опубликовано тем же автором спустя 19 лет [6,7]. Термин камптокормия был впервые введен в 1914 году французскими неврологами Суке и Розановым-Салоффом, которые описали аномалию у солдат Первой мировой войны, травмированных контузией [8,9]. ]. Первый описанный солдат был ранен пулей, вошедшей по подмышечному краю лопатки и вышедшей около позвоночника, в результате чего туловище согнулось почти под прямым углом [9]. Для «poilu» (прозвище французского солдата Первой мировой войны) это состояние было известно как «cintrage» (боль). Мужчину «вылечили» наложением гипсовых корсетов [9]. В 1919 г. еще два случая были описаны Roussy и Lhermitte [10]. Первым был пехотинец, подброшенный в воздух разорвавшимся снарядом, который испытал сильную боль и после прихода в сознание остался сутулым вправо [10]. Его также вылечили гипсовым корсетом. Второй случай был у «егеря», который испытал респираторный дистресс, мутизм и камптокормию после того, как его похоронили во время взрыва. Он выздоровел после одного сеанса электролечения [10]. Хотя эти случаи были классифицированы как истерические, одна только травматическая травма может в достаточной степени объяснить камптокормию [11]. Связь между камптокормией и болезнью Паркинсона была впервые описана Djaldetti et al.
]. Первый описанный солдат был ранен пулей, вошедшей по подмышечному краю лопатки и вышедшей около позвоночника, в результате чего туловище согнулось почти под прямым углом [9]. Для «poilu» (прозвище французского солдата Первой мировой войны) это состояние было известно как «cintrage» (боль). Мужчину «вылечили» наложением гипсовых корсетов [9]. В 1919 г. еще два случая были описаны Roussy и Lhermitte [10]. Первым был пехотинец, подброшенный в воздух разорвавшимся снарядом, который испытал сильную боль и после прихода в сознание остался сутулым вправо [10]. Его также вылечили гипсовым корсетом. Второй случай был у «егеря», который испытал респираторный дистресс, мутизм и камптокормию после того, как его похоронили во время взрыва. Он выздоровел после одного сеанса электролечения [10]. Хотя эти случаи были классифицированы как истерические, одна только травматическая травма может в достаточной степени объяснить камптокормию [11]. Связь между камптокормией и болезнью Паркинсона была впервые описана Djaldetti et al. [12] в 1999. Камптокормия, обусловленная генетическим заболеванием, впервые описана у больного миотонической дистрофией 2 типа, несущего мутацию гена ZNF9 [13]. О первом пациенте с мультисистемной атрофией (МСА) и камптокормией сообщил Reichel et al. [14] в 2001 г.
[12] в 1999. Камптокормия, обусловленная генетическим заболеванием, впервые описана у больного миотонической дистрофией 2 типа, несущего мутацию гена ZNF9 [13]. О первом пациенте с мультисистемной атрофией (МСА) и камптокормией сообщил Reichel et al. [14] в 2001 г.
Частота
Данных о частоте камптокормии немного. В одноцентровом эпидемиологическом исследовании 275 последовательных амбулаторных пациентов с болезнью Паркинсона распространенность камптокормии составила 6,9% [15]. Возникновение камптокормии в этом исследовании было связано с тяжестью болезни Паркинсона [15].
Клиническая картина
Камптокормия клинически характеризуется чрезмерным непроизвольным сгибанием туловища из-за прогрессирующей слабости мышц-разгибателей позвонков [16]. Камптокормия усиливается при стоянии и ходьбе [17] и уменьшается в положении лежа или на спине [18,19,20]. В целом ряде случаев камптокормия связана с болью в пояснице [1, 3, 7, 21, 22, 23, 24], но в других случаях она безболезненна [19]. Камптокормия может быть связана с сопутствующей слабостью большой ягодичной мышцы и бедра и коленным сгибанием [3]. Камптокормия связана с синдромом висячей головы только в единичных случаях [25,26], например, у пациентов с миотонической дистрофией 1 типа [16], МСА или постэнцефалитным синдромом Паркинсона [26]. Почти все пациенты с камптокормией имеют спондилоартроз, что делает его фактором риска развития камптокормии [27]. В исследовании 16 пациентов средний возраст начала камптокормии составил 65 лет, а средний возраст появления неврологических нарушений — 52 года [28]. Почти 69% пациентов имели болезнь Паркинсона, 25% — дистонию и один синдром Жиля де ла Туретта [28]. Семейный анамнез может быть положительным в отношении заболевания мышц в 50% случаев [23].
Камптокормия может быть связана с сопутствующей слабостью большой ягодичной мышцы и бедра и коленным сгибанием [3]. Камптокормия связана с синдромом висячей головы только в единичных случаях [25,26], например, у пациентов с миотонической дистрофией 1 типа [16], МСА или постэнцефалитным синдромом Паркинсона [26]. Почти все пациенты с камптокормией имеют спондилоартроз, что делает его фактором риска развития камптокормии [27]. В исследовании 16 пациентов средний возраст начала камптокормии составил 65 лет, а средний возраст появления неврологических нарушений — 52 года [28]. Почти 69% пациентов имели болезнь Паркинсона, 25% — дистонию и один синдром Жиля де ла Туретта [28]. Семейный анамнез может быть положительным в отношении заболевания мышц в 50% случаев [23].
Этиология
Для объяснения этиологии и патомеханизмов, лежащих в основе камптокормии, возникли две точки зрения. Первая рассматривает камптокормию как расстройство ЦНС, приводящее к фокальной дистонии позвоночника [27]. Согласно этой гипотезе, структурой ЦНС, которая должна быть поражена, является полосатое тело и его проекции на ретикулоспинальный тракт или таламус [27]. Аргументами в пользу этой гипотезы являются положительное влияние глубокой стимуляции мозга на камптокормию в единичных случаях [27] и уменьшение объема среднего мозга и моста у пациентов с болезнью Паркинсона и камптокормией. Вторая гипотеза связывает камптокормию с поражением периферической нервной системы (ПНС), в частности с миопатией антигравитационных мышц, связанной с разгибанием туловища [27]. Эта гипотеза подтверждается миопатическими электромиографиями (ЭМГ), гиподенсивностью на МРТ мышц, миопатическими изменениями при биопсии мышц и случайным улучшением на фоне приема стероидов [27]. Камптокормия чаще всего возникает из-за органических заболеваний и лишь изредка является проявлением психического расстройства [28,29].].
Согласно этой гипотезе, структурой ЦНС, которая должна быть поражена, является полосатое тело и его проекции на ретикулоспинальный тракт или таламус [27]. Аргументами в пользу этой гипотезы являются положительное влияние глубокой стимуляции мозга на камптокормию в единичных случаях [27] и уменьшение объема среднего мозга и моста у пациентов с болезнью Паркинсона и камптокормией. Вторая гипотеза связывает камптокормию с поражением периферической нервной системы (ПНС), в частности с миопатией антигравитационных мышц, связанной с разгибанием туловища [27]. Эта гипотеза подтверждается миопатическими электромиографиями (ЭМГ), гиподенсивностью на МРТ мышц, миопатическими изменениями при биопсии мышц и случайным улучшением на фоне приема стероидов [27]. Камптокормия чаще всего возникает из-за органических заболеваний и лишь изредка является проявлением психического расстройства [28,29].].
Органические расстройства
Расстройства ЦНС
Расстройством ЦНС, наиболее часто сообщаемым в связи с камптокормией, является болезнь Паркинсона [1,12]. Клинические особенности камптокормии при болезни Паркинсона включают пожилой возраст, преимущественно мужской пол, большую продолжительность заболевания и раннее вовлечение аксиальной оси [3]. Камптокормия обычно развивается после появления симптомов Паркинсона. Лишь в единичных случаях камптокормия может быть начальным проявлением болезни Паркинсона [30]. Камптокормия при болезни Паркинсона начинает развиваться в возрасте от 60 до 70 лет [3], а латентный период, с которым возникает камптокормия после начала болезни Паркинсона, составляет 5–10 лет [1,31]. Камптокормия чаще всего обнаруживается у пациентов с более тяжелой болезнью Паркинсона. Камптокормия при болезни Паркинсона связана либо с ЦНС, либо с ПНС. Аргументы в пользу ЦНС-причины заключаются в том, что камптокормия возникает вместе с расстройствами ЦНС, что тяжесть камптокормии при болезни Паркинсона связана с уменьшением объема среднего мозга и моста [32], что у половины пациентов с паркинсонизмом с камптокормией развивается синдром беспокойных ног [32], что у больных паркинсонизмом с камптокормией наблюдается повышенная мышечная активность при полисомнографии, что свидетельствует о поражении центральной регуляции движений во время сна [32], что паркинсонизм у больных камптокормией часто сочетается с дистонией [28], что могут быть дополнительные, не дисфункцию дофаминергических нейронов в базальных ганглиях или стволе головного мозга у пациентов с паркинсонизмом с камптокормией [3], а также то, что некоторые пациенты с камптокормией реагируют на глубокую стимуляцию мозга.
Клинические особенности камптокормии при болезни Паркинсона включают пожилой возраст, преимущественно мужской пол, большую продолжительность заболевания и раннее вовлечение аксиальной оси [3]. Камптокормия обычно развивается после появления симптомов Паркинсона. Лишь в единичных случаях камптокормия может быть начальным проявлением болезни Паркинсона [30]. Камптокормия при болезни Паркинсона начинает развиваться в возрасте от 60 до 70 лет [3], а латентный период, с которым возникает камптокормия после начала болезни Паркинсона, составляет 5–10 лет [1,31]. Камптокормия чаще всего обнаруживается у пациентов с более тяжелой болезнью Паркинсона. Камптокормия при болезни Паркинсона связана либо с ЦНС, либо с ПНС. Аргументы в пользу ЦНС-причины заключаются в том, что камптокормия возникает вместе с расстройствами ЦНС, что тяжесть камптокормии при болезни Паркинсона связана с уменьшением объема среднего мозга и моста [32], что у половины пациентов с паркинсонизмом с камптокормией развивается синдром беспокойных ног [32], что у больных паркинсонизмом с камптокормией наблюдается повышенная мышечная активность при полисомнографии, что свидетельствует о поражении центральной регуляции движений во время сна [32], что паркинсонизм у больных камптокормией часто сочетается с дистонией [28], что могут быть дополнительные, не дисфункцию дофаминергических нейронов в базальных ганглиях или стволе головного мозга у пациентов с паркинсонизмом с камптокормией [3], а также то, что некоторые пациенты с камптокормией реагируют на глубокую стимуляцию мозга. Аргументы в пользу ПНС происхождения камптокормии при болезни Паркинсона заключаются в том, что аксиальные мышцы могут проявлять миопатические признаки на ЭМГ или биопсии мышц [1] и что МРТ аксиальных мышц может показать атрофию и жировое замещение грудопоясничных мышц [33]. Нарушения ЦНС, связанные с камптокормией, в дополнение к болезни Паркинсона включают MSA [2,34,35], болезнь Альцгеймера [36], нарушения базальных ганглиев [14] и абдоминальную сегментарную дистонию [37]. Из-за частой ассоциации камптокормии с болезнью Паркинсона [3,19] или дистонии [28], некоторые авторы относят камптокормию даже к сегментарной форме дистонии [14,38].
Аргументы в пользу ПНС происхождения камптокормии при болезни Паркинсона заключаются в том, что аксиальные мышцы могут проявлять миопатические признаки на ЭМГ или биопсии мышц [1] и что МРТ аксиальных мышц может показать атрофию и жировое замещение грудопоясничных мышц [33]. Нарушения ЦНС, связанные с камптокормией, в дополнение к болезни Паркинсона включают MSA [2,34,35], болезнь Альцгеймера [36], нарушения базальных ганглиев [14] и абдоминальную сегментарную дистонию [37]. Из-за частой ассоциации камптокормии с болезнью Паркинсона [3,19] или дистонии [28], некоторые авторы относят камптокормию даже к сегментарной форме дистонии [14,38].
Нарушения ПНС
Состояния ПНС, связанные с камптокормией, включают первичные миопатии, такие как миотоническая дистрофия типа 1 [16,21] и типа 2 [39], дисферлинопатия [24], немалиновая миопатия [20], аксиальная миопатия [7,40 ,41], или митохондриальной миопатии (таблица 1) [42]. Вторичные миопатии с камптокормией включают гипотиреоидную миопатию [43], дерматомиозит, полимиозит [43,44], фокальный или сегментарный миозит [33,45,46], миозит с включениями [3] или тяжелую миастению (таблица 1) [47]. Часто наблюдаемые миопатические аномалии на ЭМГ или биопсии мышц у пациентов с паркинсонизмом с камптокормией объясняются скорее хроническими сокращениями антигравитационных мышц, участвующих в компенсаторном разгибании туловища, чем первичной миопатией [48]. Однако, почему гиперактивная мышца развивает миопатические изменения, остается спекулятивным. Из-за частой ассоциации камптокормии с миопатией некоторые авторы обычно рассматривают камптокормию как первичную опоясывающую миопатию с субклиническим поражением мышц таза и плечевого пояса [49].].
Часто наблюдаемые миопатические аномалии на ЭМГ или биопсии мышц у пациентов с паркинсонизмом с камптокормией объясняются скорее хроническими сокращениями антигравитационных мышц, участвующих в компенсаторном разгибании туловища, чем первичной миопатией [48]. Однако, почему гиперактивная мышца развивает миопатические изменения, остается спекулятивным. Из-за частой ассоциации камптокормии с миопатией некоторые авторы обычно рассматривают камптокормию как первичную опоясывающую миопатию с субклиническим поражением мышц таза и плечевого пояса [49].].
Нарушения ПНС, кроме миопатии, связанной с камптокормией, включают боковой амиотрофический склероз [50], хроническую воспалительную демиелинизирующую полинейропатию [51] или поясничную грыжу диска [52]. К настоящему времени обнаружены мутации у пациентов с камптокормией: ген RYR1 при аксиальной миопатии [53], ген DMPK при миотонической дистрофии 1 [16,21], ZFP9 при миотонической дистрофии 2 типа [39], ген дисферлина при дисферлинопатии и ген паркина. ген при болезни Паркинсона [54].
ген при болезни Паркинсона [54].
Наркотики
Редкими причинами камптокормии являются побочные эффекты терапевтических препаратов. Среди них наибольшее значение имеют нейролептические и противопаркинсонические препараты (таблица 1). Среди нейролептиков камптокормию чаще всего вызывал оланзапин [55]. L -ДОФА индуцировал или усугублял камптокормию в единичных случаях [12], но также может иметь положительный эффект в случаях, когда она вызвана болезнью Паркинсона [19, 56] или MSA (см. ниже). У одного пациента камптокормия была вызвана донепезилом [57]. У нескольких пациентов камптокормия была вызвана передозировкой вальпроевой кислоты [58]. Имеются также сведения о том, что системные кортикостероиды могут вызывать камптокормию [перс. общ.]. Если эти препараты отменяются, камптокормия может улучшиться.
Разное
У отдельных пациентов камптокормия была связана с травмой [59, 60], артритом [60] или злокачественными новообразованиями (таблица 1) [61]. В последнем случае камптокормия интерпретировалась как проявление паранеопластического синдрома.
Психические расстройства
Хотя камптокормия первоначально описывалась как конверсионное расстройство у военнослужащих [29,62,63], психогенная камптокормия встречается редко [29,64]. В частности, в раннем описании аномалии она интерпретировалась как форма истерии, возникающая у лиц с низкой самооценкой и путаницей идентичности, садомазохистским поведением по отношению к военным властям и импотенцией [11]. Камптокормия также была описана в связи с синдромом Жиля де ла Туретта [28], маниакально-депрессивным расстройством [65] или психогенным состоянием [29].].
Диагностика
Поскольку этиология камптокормии весьма неоднородна, в начале диагностической работы необходимо проводить исследования в разных направлениях. Как правило, диагноз может быть установлен на основании клинических данных, биохимических исследований крови, визуализации головного мозга, ЭМГ или биопсии мышц.
Биология
Существует ряд химических параметров крови, которые полезны при диагностике камптокормии. Среди них скорость оседания крови, С-реактивный белок, электролиты, такие как кальций и фосфор, креатинкиназа, альдолаза или витамин D. Для диагностики метаболических миопатий определение лактата и пирувата во время стандартизированных упражнений может быть дополнительной помощью. .
Среди них скорость оседания крови, С-реактивный белок, электролиты, такие как кальций и фосфор, креатинкиназа, альдолаза или витамин D. Для диагностики метаболических миопатий определение лактата и пирувата во время стандартизированных упражнений может быть дополнительной помощью. .
Визуализация
КТ головного мозга может показать атрофию, кальцификацию базальных ганглиев, лакуны базальных ганглиев, чечевицеобразные поражения или уменьшение объема среднего мозга или моста [32]. МРТ черепа может показать аномалии сигнала базальных ганглиев у небольшого числа пациентов с камптокормией и болезнью Паркинсона [22]. МРТ позвоночных мышц может показать признаки ограниченной миопатии, такие как различная степень атрофии и жирового замещения грудопоясничных параспинальных мышц [66]. Эти изменения аналогичны наблюдаемым при мышечной дистрофии [67]. Локализованные изменения от отека с усилением контраста считаются ранним признаком, тогда как атрофия или жировая дистрофия считаются поздними изменениями [1,3,68].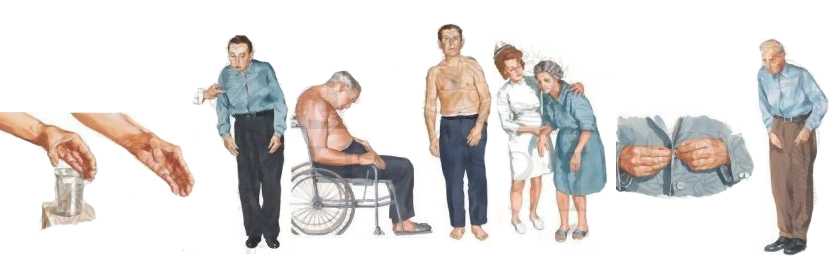 Некоторые авторы трактуют эти изменения скорее как вторичные, чем как причину камптокормии [52]. КТ спинных мышц может показать атрофию и гиподенсивность мышц, что интерпретируется как жировая инволюция [69].].
Некоторые авторы трактуют эти изменения скорее как вторичные, чем как причину камптокормии [52]. КТ спинных мышц может показать атрофию и гиподенсивность мышц, что интерпретируется как жировая инволюция [69].].
Игольная электромиография
В зависимости от основной причины ЭМГ может быть нормальной, нейрогенной или миогенной. Миогенный паттерн может быть зарегистрирован даже у пациентов с болезнью Паркинсона [1]. Игольчатая ЭМГ паравертебральных мышц также может выявить обильные фибрилляции, положительные острые волны или причудливые высокочастотные разряды [33].
Мышечная биопсия
Мышечная биопсия может быть нормальной или может показать легкие миопатические признаки, воспалительные признаки, указывающие на фокальную воспалительную миопатию (очаговый миозит), или дистрофические признаки [67]. Также может быть обширный диффузный или дольчатый фиброз как единственный вариант обнаружения у пациентов с камптокормией по сравнению с контрольной группой [68]. Мышечная биопсия у пациентов с болезнью Паркинсона с камптокормией может быть разделена на три группы: некротическая миопатия, воспалительная миопатия или митохондриальная миопатия [70]. Миопатические изменения у пациентов с болезнью Паркинсона включают аномальное изменение размера волокон, увеличение внутренних ядер, увеличение соединительной ткани или беспорядок миофибрилл или жировую дистрофию [1,31]. У пациентов с прогрессирующей болезнью Паркинсона и камптокормией биопсия мышц может выявить терминальную миопатию с аутофагическими вакуолями, хроническую воспалительную миопатию, неспецифические миопатические изменения или митохондриальную миопатию [33]. В единичных случаях также могут наблюдаться отложения амилоида и рваные красные волокна [перс. общ.].
Мышечная биопсия у пациентов с болезнью Паркинсона с камптокормией может быть разделена на три группы: некротическая миопатия, воспалительная миопатия или митохондриальная миопатия [70]. Миопатические изменения у пациентов с болезнью Паркинсона включают аномальное изменение размера волокон, увеличение внутренних ядер, увеличение соединительной ткани или беспорядок миофибрилл или жировую дистрофию [1,31]. У пациентов с прогрессирующей болезнью Паркинсона и камптокормией биопсия мышц может выявить терминальную миопатию с аутофагическими вакуолями, хроническую воспалительную миопатию, неспецифические миопатические изменения или митохондриальную миопатию [33]. В единичных случаях также могут наблюдаться отложения амилоида и рваные красные волокна [перс. общ.].
Анализ походки
Кинематический, кинетический и биомеханический анализы могут выявить преувеличенный наклон таза вперед во время конечного положения при ходьбе в вертикальном положении. Однако в позе с наклоном вперед наклон таза вперед может быть значительно меньше [71]. Некоторые авторы предполагают, что поза с экстремальным наклоном вперед является компенсаторным механизмом для уменьшения чрезмерного наклона таза [71].
Некоторые авторы предполагают, что поза с экстремальным наклоном вперед является компенсаторным механизмом для уменьшения чрезмерного наклона таза [71].
Лечение
Варианты лечения камптокормии ограничены и часто бесполезны [72]. Как правило, варианты лечения можно классифицировать как консервативные или инвазивные (таблица 2). Консервативные меры включают психотерапию, физиотерапию, применение лекарств, введение ботулотоксина, отмену препаратов, вызывающих заболевание, или электрошоковую терапию. К инвазивным лечебным мероприятиям относятся хирургические методы или глубокая стимуляция головного мозга. Лечением выбора является терапия основного заболевания, а в случае отсутствия средств, модифицирующих заболевание, единственным выбором являются ортезы, физиотерапия и, в конечном итоге, анальгетики [4].
Таблица 2
Лечение камптокормии
Психотерапия
Существует ряд психотерапевтических методик, которые можно применять к больным камптокормией психогенного происхождения. К ним относятся психообразование в отношении вторичной выгоды, предложения по улучшению осанки, положительное подкрепление или поведенческая терапия [56]. Убеждающее перевоспитание особенно применялось в случаях Первой мировой войны, но эта психологическая терапия была скорее аддитивной, чем убеждающей [11].
К ним относятся психообразование в отношении вторичной выгоды, предложения по улучшению осанки, положительное подкрепление или поведенческая терапия [56]. Убеждающее перевоспитание особенно применялось в случаях Первой мировой войны, но эта психологическая терапия была скорее аддитивной, чем убеждающей [11].
Физиотерапия, ортезы
Классические ортезы и физиотерапия часто малоэффективны, часто плохо переносятся [4] и от них быстро отказываются [73]. Однако применение переднеторакотазового дистракционного ортеза приводит к повышению качества жизни на 90% [4]. В единичных случаях физиотерапия и ортезы могут облегчить боль в пояснице [7].
L -ДОФА
В большинстве случаев при прогрессирующей болезни Паркинсона камптокормия L -ДОФА-устойчивый [1,74]. Однако в единичных случаях камптокормии, связанной с болезнью Паркинсона, дистонией или MSA, было показано, что введение L -ДОФА приносит пользу [62,74,75]. В зависимости от исследуемой когорты до 20% больных паркинсонизмом с камптокормией получают пользу от терапии L -ДОФА [3]. У больного МСА с преимущественным паркинсонизмом камптокормия и болезнь Паркинсона заметно улучшились на фоне L -ДОФА [74]. У больного с болезнью Паркинсона коррекция дофаминергической терапии карбидопой-леводопой и энтакарпоном привела не только к улучшению течения болезни Паркинсона, но и камптокормии [76].
У больного МСА с преимущественным паркинсонизмом камптокормия и болезнь Паркинсона заметно улучшились на фоне L -ДОФА [74]. У больного с болезнью Паркинсона коррекция дофаминергической терапии карбидопой-леводопой и энтакарпоном привела не только к улучшению течения болезни Паркинсона, но и камптокормии [76].
Иммуноглобулины
Опубликовано мало данных, демонстрирующих положительный эффект иммуноглобулинов (ВВИГ) при камптокормии [25]. 81-летний мужчина с подтвержденной воспалительной миопатией параспинальных мышц испытал резкое улучшение на фоне лечения ВВИГ [25]. ВВИГ эффективны только в случаях воспалительной миопатии.
Ботулинический токсин
Было показано, что инъекции ботулотоксина в прямые мышцы живота эффективны в единичных случаях, когда камптокормия была вызвана фокальной дистонией [28,38]. Инъекции ботулинического токсина в подвздошно-поясничные мышцы также могут уменьшить камптокормию [34]. Однако у других пациентов с паркинсон-ассоциированной камптокормией введение ботулинического токсина в подвздошно-поясничную мышцу оказалось неэффективным [72]. Ботулинический токсин может быть эффективен не только у пациентов с фокальной дистонией, но и у пациентов с болезнью Паркинсона [77].
Ботулинический токсин может быть эффективен не только у пациентов с фокальной дистонией, но и у пациентов с болезнью Паркинсона [77].
Электросудорожная терапия
У одного пациента с камптокормией, вызванной оланзапином, отмена препарата и применение L -ДОФА вряд ли были эффективными, но электросудорожная терапия была успешно опробована [61].
Разное
Пациенты с лекарственной камптокормией обычно реагируют на отмену нейролептиков или снижение суточных доз. В единичных случаях воспалительной миопатии параспинальных мышц может помочь назначение стероидов [27]. Стероиды для лечения камптокормии при болезни Паркинсона, напротив, не показали положительного эффекта [17]. Применение антихолинергических средств, амантадина, агонистов дофамина, миорелаксантов или тетрабеназина обычно малоэффективно [52].
Глубокая стимуляция мозга
В единичных случаях, когда камптокормия связана с болезнью Паркинсона или сегментарной дистонией, двусторонняя паллидная высокочастотная стимуляция глубокого мозга [62,78,79] или двусторонняя стимуляция субталамического ядра [80,81] могут иметь полезный эффект. Терапевтический эффект глубокой стимуляции мозга свидетельствует о том, что, по крайней мере, в единичных случаях камптокормия действительно является заболеванием ЦНС, обусловленным поражением полосатого тела, его ретикулоспинальной и таламической проекций [27]. У пациента с хронической инвалидизирующей болезнью Паркинсона камптокормия резко улучшилась после двусторонней субталамической глубокой стимуляции мозга [79].]. Для паллидной стимуляции электроды для глубокой стимуляции головного мозга стереотаксически имплантируют во внутренний бледный шар [82]. Длительная паллидарная стимуляция приводит к значительному функциональному улучшению при отсутствии каких-либо побочных эффектов, связанных с лечением [82].
Терапевтический эффект глубокой стимуляции мозга свидетельствует о том, что, по крайней мере, в единичных случаях камптокормия действительно является заболеванием ЦНС, обусловленным поражением полосатого тела, его ретикулоспинальной и таламической проекций [27]. У пациента с хронической инвалидизирующей болезнью Паркинсона камптокормия резко улучшилась после двусторонней субталамической глубокой стимуляции мозга [79].]. Для паллидной стимуляции электроды для глубокой стимуляции головного мозга стереотаксически имплантируют во внутренний бледный шар [82]. Длительная паллидарная стимуляция приводит к значительному функциональному улучшению при отсутствии каких-либо побочных эффектов, связанных с лечением [82].
Хирургия
В случаях, когда консервативные меры неэффективны, пациентам может помочь задняя грудопоясничная фиксация, которую может потребоваться дополнить передним межтеловым спондилодезом [83].
Заключение
Камптокормия в подавляющем большинстве случаев является органическим заболеванием, либо проявлением поражения ЦНС, либо следствием поражения периферических нервов или скелетных мышц. Лишь в редких случаях камптокормия вызывается психическим расстройством. Лекарственные препараты, травма или ортопедические проблемы могут оказывать свое влияние. Поскольку камптокормия возникает из-за ряда различных заболеваний, начальным шагом в лечении камптокормии является выявление основной причины. Лечение, как правило, должно быть направлено на основную этиологию и патомеханизм. Общие меры, такие как физиотерапия, ортезы или ботулинический токсин, могут быть полезны в единичных случаях. Только при эффективном лечении основной причины можно ожидать существенного терапевтического эффекта. Если лечение камптокормии неэффективно, больным рано или поздно потребуются приспособления для ходьбы и, в последнюю очередь, кресло-коляска. Поскольку возможности охарактеризовать патофизиологию камптокормии при болезни Паркинсона с помощью доступных технологий ограничены, для полного понимания постуральных феноменов и разработки эффективного лечения требуется животная модель аномальной позы.
Лишь в редких случаях камптокормия вызывается психическим расстройством. Лекарственные препараты, травма или ортопедические проблемы могут оказывать свое влияние. Поскольку камптокормия возникает из-за ряда различных заболеваний, начальным шагом в лечении камптокормии является выявление основной причины. Лечение, как правило, должно быть направлено на основную этиологию и патомеханизм. Общие меры, такие как физиотерапия, ортезы или ботулинический токсин, могут быть полезны в единичных случаях. Только при эффективном лечении основной причины можно ожидать существенного терапевтического эффекта. Если лечение камптокормии неэффективно, больным рано или поздно потребуются приспособления для ходьбы и, в последнюю очередь, кресло-коляска. Поскольку возможности охарактеризовать патофизиологию камптокормии при болезни Паркинсона с помощью доступных технологий ограничены, для полного понимания постуральных феноменов и разработки эффективного лечения требуется животная модель аномальной позы.
Авторское право: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или любую систему хранения и поиска информации, без письменного разрешения издателя. .
Дозировка препарата: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор препарата и дозировка, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации. Тем не менее, в связи с продолжающимися исследованиями, изменениями в правительственных постановлениях и постоянным потоком информации, касающейся лекарственной терапии и реакций на лекарства, читателю настоятельно рекомендуется проверять вкладыш в упаковке для каждого лекарства на предмет любых изменений в показаниях и дозировке, а также для дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендуемый агент является новым и/или редко используемым лекарственным средством.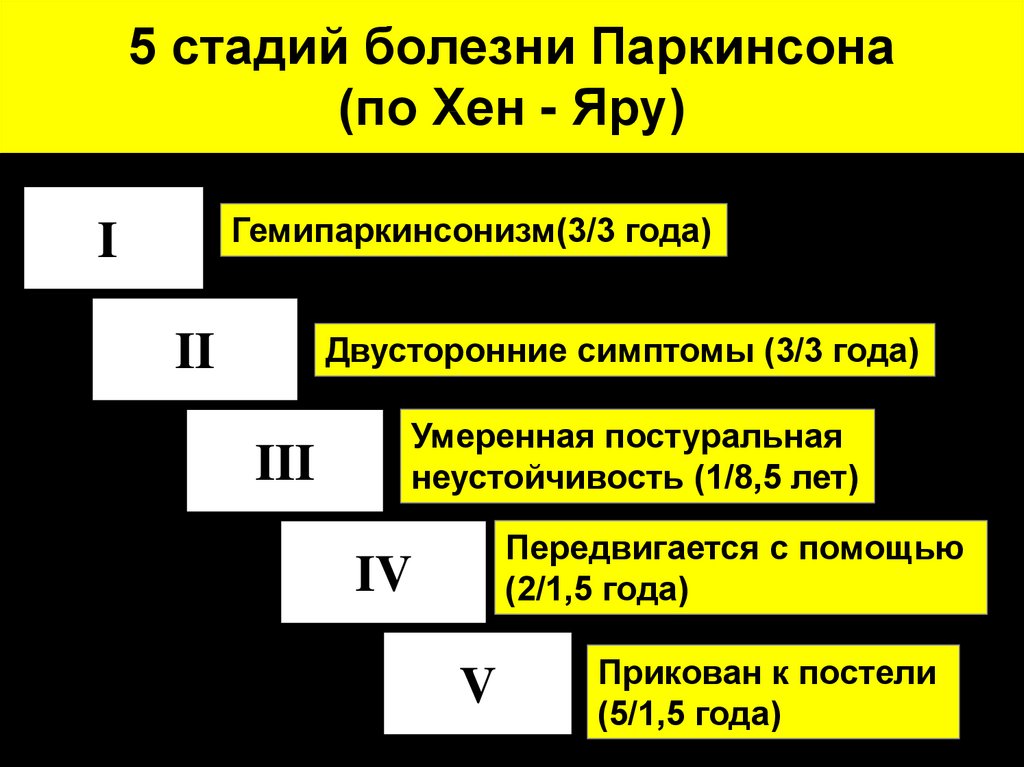
Отказ от ответственности: заявления, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и участникам, а не издателям и редакторам. Появление рекламы и/или ссылок на продукты в публикации не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор(ы) отказываются от ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в содержании или рекламе.
27. Неспособность встать исправлена: камптокормия, редкая причина искривления позвоночника | Достижения ревматологии на практике
Фильтр поиска панели навигации Успехи ревматологии в практикеЭтот выпускЖурналыБританского общества ревматологовМедицина и здоровьеКнигиЖурналыOxford Academic Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Успехи ревматологии в практикеЭтот выпускЖурналыБританского общества ревматологовМедицина и здоровьеКнигиЖурналыOxford Academic Термин поиска на микросайте
Расширенный поиск
Журнальная статья
Йик Лонг Ман,
Йик Лонг Ман
Ищите другие работы этого автора на:
Оксфордский академический
Google ученый
Майкл Роуз,
Майкл Роуз
Ищите другие работы этого автора на:
Оксфордский академический
Google ученый
Джеральд Коукли
Джеральд Кокли
Ищите другие работы этого автора на:
Оксфордский академический
Google ученый
Достижения ревматологии на практике , том 2, выпуск suppl_1, сентябрь 2018 г.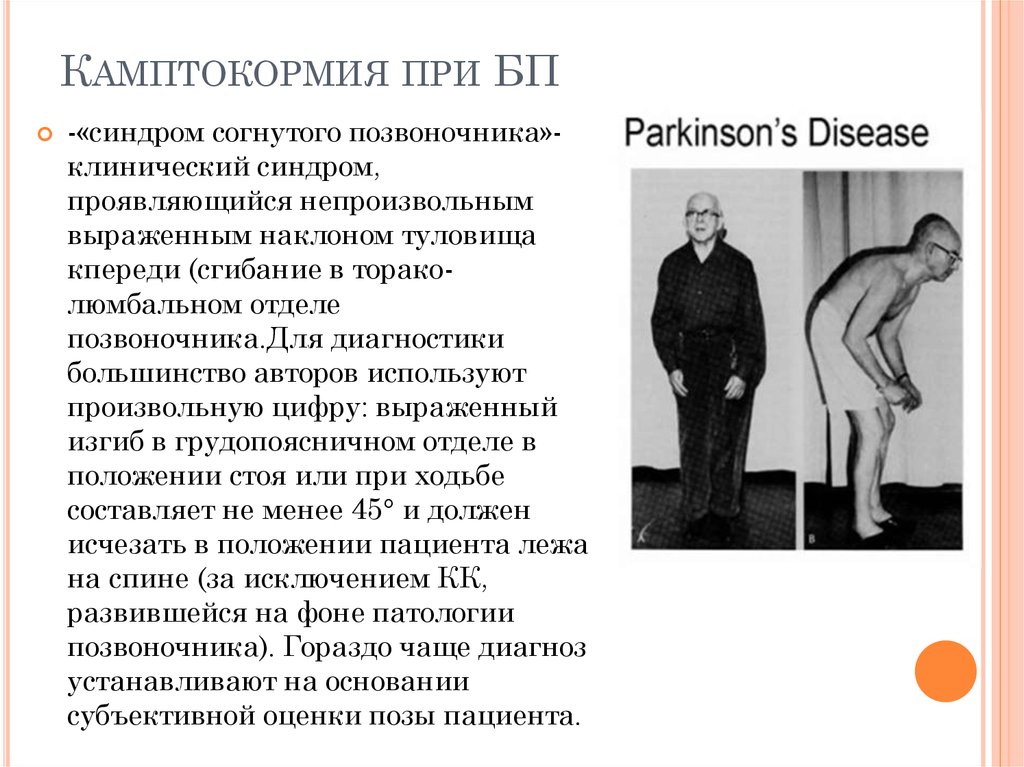 , rky033.018, https://doi.org/10.1093/rap/rky033.018
, rky033.018, https://doi.org/10.1093/rap/rky033.018
Опубликовано:
20 сентября 2018
Фильтр поиска панели навигации Успехи ревматологии в практикеЭтот выпускЖурналыБританского общества ревматологовМедицина и здоровьеКнигиЖурналыOxford Academic Термин поиска мобильного микросайта
Закрыть
Фильтр поиска панели навигации Успехи ревматологии в практикеЭтот выпускЖурналыБританского общества ревматологовМедицина и здоровьеКнигиЖурналыOxford Academic Термин поиска на микросайте
Расширенный поиск
Введение: К ревматологам часто обращаются пожилые пациенты с болями в спине и усилением грудного кифоза. Обычно это связано с переломами позвонков, вторичными по отношению к остеопорозу. Мы представляем случай камптокормии, редкой причины искривления позвоночника, при которой наблюдается повышенное сгибание грудопоясничного отдела позвоночника вперед вследствие слабости разгибателей паравертебральных мышц. Поразительно, что эта деформация полностью исчезает в положении лежа на спине.
Обычно это связано с переломами позвонков, вторичными по отношению к остеопорозу. Мы представляем случай камптокормии, редкой причины искривления позвоночника, при которой наблюдается повышенное сгибание грудопоясничного отдела позвоночника вперед вследствие слабости разгибателей паравертебральных мышц. Поразительно, что эта деформация полностью исчезает в положении лежа на спине.
Описание случая: 85-летний бывший танцор был направлен в ревматологическую клинику с ухудшением сутулости, которое развилось в течение года. Ее лечащий врач был обеспокоен тем, что у нее могли быть остеопоротические переломы позвонков. Ее сутулость была настолько сильной, что она не могла смотреть прямо перед собой, и это оказало серьезное влияние на ее повседневную деятельность. У нее были легкие боли в грудном отделе спины. Она не сообщила об отсутствии неврологических симптомов. При осмотре у нее был искривленный позвоночник с выраженным кифозом. Следует отметить, что деформация позвоночника полностью разрешилась, когда она лежала на кушетке на спине. У нее было нормальное неврологическое обследование верхних и нижних конечностей, хотя была заметная титубация головы. Исследования включали простые рентгенограммы и МРТ позвоночника. Они показали дегенеративные изменения и незначительный стеноз позвоночного канала на нескольких уровнях, но никаких признаков переломов позвонков, объясняющих искривление позвоночника, не обнаружено. Был предложен диагноз камптокормия, и она была направлена к неврологу для дальнейшего обследования. Мнение невролога заключалось в том, что у нее была камптокормия, вторичная по отношению к дистонии, ввиду ригидности затылочных мышц и вертения головы, и ей дали ко-карелдопу для купирования симптомов. Также была организована МРТ головы, которая показала тонкие, неспецифические изменения Т2 в базальных ганглиях и таламусах на двусторонней основе, что, скорее всего, свидетельствует об ишемии мелких сосудов.
У нее было нормальное неврологическое обследование верхних и нижних конечностей, хотя была заметная титубация головы. Исследования включали простые рентгенограммы и МРТ позвоночника. Они показали дегенеративные изменения и незначительный стеноз позвоночного канала на нескольких уровнях, но никаких признаков переломов позвонков, объясняющих искривление позвоночника, не обнаружено. Был предложен диагноз камптокормия, и она была направлена к неврологу для дальнейшего обследования. Мнение невролога заключалось в том, что у нее была камптокормия, вторичная по отношению к дистонии, ввиду ригидности затылочных мышц и вертения головы, и ей дали ко-карелдопу для купирования симптомов. Также была организована МРТ головы, которая показала тонкие, неспецифические изменения Т2 в базальных ганглиях и таламусах на двусторонней основе, что, скорее всего, свидетельствует об ишемии мелких сосудов.
Обсуждение: Камптокормия также известна как синдром искривления позвоночника; характерной чертой является сильное сгибание грудопоясничного отдела позвоночника вперед, которое присутствует при ходьбе или стоянии с полным разрешением в положении лежа.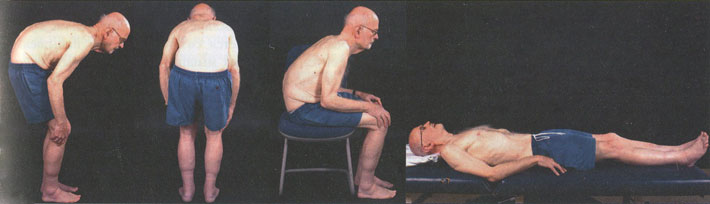 Это связано со слабостью разгибателей паравертебральных мышц. Переломы позвонков, вторичные по отношению к остеопорозу, часто встречаются в ревматологической клинике и проявляются болями в спине и усилением грудного кифоза. Обычно это подтверждается при визуализации. Однако при отсутствии каких-либо переломов позвонков при визуализации необходимо рассматривать альтернативные диагнозы. Кроме того, если наблюдается разрешение искривления позвоночника в положении лежа на спине, следует рассмотреть диагноз камптокормии. Есть много причин камптокормии, но наиболее известная связь связана с болезнью Паркинсона. Обычно это происходит у пациентов с более тяжелой болезнью Паркинсона. Другие расстройства центральной нервной системы, связанные с камптокормией, включают дистонию, мультисистемную атрофию и болезнь Альцгеймера. Это также может быть связано с заболеваниями периферической нервной системы, включая тяжелую миастению и хроническую воспалительную демиелинизирующую полинейропатию. Интересно, что в редких случаях оно может быть вызвано психическими расстройствами и хорошо известно как конверсионное расстройство у травмированных военнослужащих.
Это связано со слабостью разгибателей паравертебральных мышц. Переломы позвонков, вторичные по отношению к остеопорозу, часто встречаются в ревматологической клинике и проявляются болями в спине и усилением грудного кифоза. Обычно это подтверждается при визуализации. Однако при отсутствии каких-либо переломов позвонков при визуализации необходимо рассматривать альтернативные диагнозы. Кроме того, если наблюдается разрешение искривления позвоночника в положении лежа на спине, следует рассмотреть диагноз камптокормии. Есть много причин камптокормии, но наиболее известная связь связана с болезнью Паркинсона. Обычно это происходит у пациентов с более тяжелой болезнью Паркинсона. Другие расстройства центральной нервной системы, связанные с камптокормией, включают дистонию, мультисистемную атрофию и болезнь Альцгеймера. Это также может быть связано с заболеваниями периферической нервной системы, включая тяжелую миастению и хроническую воспалительную демиелинизирующую полинейропатию. Интересно, что в редких случаях оно может быть вызвано психическими расстройствами и хорошо известно как конверсионное расстройство у травмированных военнослужащих. Диагноз ставится на основании клинических данных при обследовании с поддержкой визуализации, электромиографии или биопсии мышц для выявления основной причины камптокормии. Таким образом, лечение направлено на лечение основного заболевания, которое обычно включает дальнейшее направление к неврологу и общие меры, включая физиотерапию и ортезы.
Диагноз ставится на основании клинических данных при обследовании с поддержкой визуализации, электромиографии или биопсии мышц для выявления основной причины камптокормии. Таким образом, лечение направлено на лечение основного заболевания, которое обычно включает дальнейшее направление к неврологу и общие меры, включая физиотерапию и ортезы.
Ключевые моменты обучения: Этот случай подчеркивает важность учета неврологических нарушений при обследовании пациента с симптомами со стороны опорно-двигательного аппарата. При отсутствии переломов позвонков рассмотрите камптокормию как причину искривления позвоночника и проверьте, улучшается ли состояние в положении лежа на спине на кушетке для осмотра. Также важно искать любые другие неврологические признаки, которые указывают на основной диагноз, поскольку контроль основного диагноза является ключом к лечению камптокормии и снижению заболеваемости.
Раскрытие информации: Y. Man: Нет. М.



 1007070707063
1007070707063  Неспособность стоять исправлена: камптокормия, редкая причина искривления позвоночника, 9 лет.0181 Rheumatology Advances in Practice , том 2, выпуск suppl_1, сентябрь 2018 г., rky033.018, https://doi.org/10.1093/rap/rky033.018
Неспособность стоять исправлена: камптокормия, редкая причина искривления позвоночника, 9 лет.0181 Rheumatology Advances in Practice , том 2, выпуск suppl_1, сентябрь 2018 г., rky033.018, https://doi.org/10.1093/rap/rky033.018