Опросник качества жизни sf 36: The SF-36 walk-wheel: a simple modification of the SF-36 physical domain improves its responsiveness for measuring health status change in spinal cord injury
Русскоязычная версия опросника для оценки качества жизни больных с периферической полинейропатией: валидация и перспективы применения | Комелягина
Качество жизни (КЖ) является интегральной характеристикой физического, психологического, эмоционального и социального функционирования больного, основанной на его субъективном восприятии [1]. Учитывая многофакторность понятия, составляющими компонентами КЖ являются: психологическое, социальное, физическое и духовное благополучие. Основной целью оценки КЖ является возможность дальнейшего воздействия на его параметры. Для этого выявляются и анализируются факторы, значимо влияющие на КЖ. Для оценки компонентов КЖ (за исключением духовного, так как, несмотря на важнейшую роль этого компонента, методов его оценки в настоящее время не существует) применяются различные опросники. В каждом опроснике есть разделы, оценивающие физическое состояние и психосоциальный статус пациента. Если опросник оценивает КЖ вне связи с возрастом, полом, состоянием здоровья, то он относится к неспецифическим. Наиболее известные неспецифические опросники – это предложенный ВОЗ опросник WHOQOL, европейский EQ-5D. Также к неспецифическим относится опросник SF-36, включая его производные, такие как короткая форма SF-36 и SF-12. Отличием данного опросника от других неспецифических является то, что он оценивает КЖ человека в связи с состоянием его здоровья, но без учета конкретной нозологии. Так как мы анализируем КЖ пациентов для того чтобы в дальнейшем попытаться улучшить его, то информации, полученной при анализе неспецифических опросников, бывает недостаточно для выполнения такой задачи. По этой причине разрабатываются и валидируются специфические опросники, вопросы которых учитывают специфику того или иного заболевания. Например, опросник QVM применяется для оценки КЖ у больных с мигренью, KDQOL-SFTM оценивает КЖ у больных, находящихся на лечении диализом и т.д. В этой связи работ по специфической оценке КЖ у больных с диабетической периферической нейропатией (ДПН) и нейропатической формой синдрома диабетической стопы (нСДС) нет.
Наиболее известные неспецифические опросники – это предложенный ВОЗ опросник WHOQOL, европейский EQ-5D. Также к неспецифическим относится опросник SF-36, включая его производные, такие как короткая форма SF-36 и SF-12. Отличием данного опросника от других неспецифических является то, что он оценивает КЖ человека в связи с состоянием его здоровья, но без учета конкретной нозологии. Так как мы анализируем КЖ пациентов для того чтобы в дальнейшем попытаться улучшить его, то информации, полученной при анализе неспецифических опросников, бывает недостаточно для выполнения такой задачи. По этой причине разрабатываются и валидируются специфические опросники, вопросы которых учитывают специфику того или иного заболевания. Например, опросник QVM применяется для оценки КЖ у больных с мигренью, KDQOL-SFTM оценивает КЖ у больных, находящихся на лечении диализом и т.д. В этой связи работ по специфической оценке КЖ у больных с диабетической периферической нейропатией (ДПН) и нейропатической формой синдрома диабетической стопы (нСДС) нет. В имеющихся публикациях КЖ у данной категории больных оценивается при помощи неспецифичных опросников, таких как SF-36, SF-12. В этих работах показатели КЖ у больных с болевой формой ДПН, незаживающими язвами и ампутациями значимо хуже, чем у больных СД, сопоставимых по возрасту и полу, но без этих осложнений [2, 3]. Следует отметить, что полученные данные достаточно легко прогнозируемы. Действительно, вполне ожидаемо, что у пациентов с болевыми ощущениями или незаживающей раной на стопе физическое состояние, а также психологический статус будут хуже, чем у пациентов без осложнений нижних конечностей. Поэтому больший интерес представляют данные, сравнивающие показатели КЖ у однородных групп больных, в нашем случае при наличии у сравниваемых групп осложнений нижних конечностей. На эту тему есть ряд публикаций. Показано, что показатели КЖ у мобильных пациентов с ампутацией конечности (пользующихся протезом) лучше, чем у пациентов с открытыми язвенными дефектами (нСДС), но хуже, чем у больных СД без осложнений со стороны нижних конечностей [4, 5].
В имеющихся публикациях КЖ у данной категории больных оценивается при помощи неспецифичных опросников, таких как SF-36, SF-12. В этих работах показатели КЖ у больных с болевой формой ДПН, незаживающими язвами и ампутациями значимо хуже, чем у больных СД, сопоставимых по возрасту и полу, но без этих осложнений [2, 3]. Следует отметить, что полученные данные достаточно легко прогнозируемы. Действительно, вполне ожидаемо, что у пациентов с болевыми ощущениями или незаживающей раной на стопе физическое состояние, а также психологический статус будут хуже, чем у пациентов без осложнений нижних конечностей. Поэтому больший интерес представляют данные, сравнивающие показатели КЖ у однородных групп больных, в нашем случае при наличии у сравниваемых групп осложнений нижних конечностей. На эту тему есть ряд публикаций. Показано, что показатели КЖ у мобильных пациентов с ампутацией конечности (пользующихся протезом) лучше, чем у пациентов с открытыми язвенными дефектами (нСДС), но хуже, чем у больных СД без осложнений со стороны нижних конечностей [4, 5]./121/121.jpg) В данном аспекте имеет значение уровень ампутации: у пациентов, которым выполнены ампутации пальцев, трансметатарзальные или ниже колена, показатели КЖ лучше, чем у пациентов с открытыми ранами. Но у пациентов с ампутациями выше колена КЖ значительно хуже, чем у пациентов с открытыми ранами [6]. Как указывалось выше, все вышеперечисленные исследования выполнялись с применением неспецифических опросников, не способных учесть специфику осложнения и выяснить, какие именно параметры КЖ задействованы и как на них можно повлиять. Кроме того, необходимо четко оценивать состояние пациента в зависимости от показателей физического и психо-социального статуса и КЖ. Это не одно и то же. КЖ не измеряет степень снижения показателей здоровья. Этот показатель оценивается самим пациентом и может не совпадать с показателями здоровья [7].
В данном аспекте имеет значение уровень ампутации: у пациентов, которым выполнены ампутации пальцев, трансметатарзальные или ниже колена, показатели КЖ лучше, чем у пациентов с открытыми ранами. Но у пациентов с ампутациями выше колена КЖ значительно хуже, чем у пациентов с открытыми ранами [6]. Как указывалось выше, все вышеперечисленные исследования выполнялись с применением неспецифических опросников, не способных учесть специфику осложнения и выяснить, какие именно параметры КЖ задействованы и как на них можно повлиять. Кроме того, необходимо четко оценивать состояние пациента в зависимости от показателей физического и психо-социального статуса и КЖ. Это не одно и то же. КЖ не измеряет степень снижения показателей здоровья. Этот показатель оценивается самим пациентом и может не совпадать с показателями здоровья [7].
Учитывая важность и социальную значимость таких осложнений СД, как ДПН и нСДС, был разработан и валидирован опросник NeuroQol для оценки параметров КЖ у больных с ДПН./164/164.jpg) Было продемонстрировано, что шкалы NeuroQol в значительно большей степени, чем шкалы SF-12, ассоциированы с тяжестью ДПН, обеспечивая тем самым более полную информацию о взаимосвязи ДПН с показателями КЖ [8].
Было продемонстрировано, что шкалы NeuroQol в значительно большей степени, чем шкалы SF-12, ассоциированы с тяжестью ДПН, обеспечивая тем самым более полную информацию о взаимосвязи ДПН с показателями КЖ [8].
Автором и разработчиком оригинальной версии является Vileikyte Loreta (Вилейкюте Лорета), представляющая Королевскую клинику г.Манчестер (Manchester Royal Infirmary, Manchaster, UK) в соавторстве с Peyrot Mark (Пейрот Марк) из Центра социальных исследований, Лойола Колледж, Балтимор, Мериленд, Bundy Christhin (Банди Кристин) из Королевской клиники г. Манчестер, Rubin Richard (Рубин Ричард) из Университета Джона Хопкинса, Балтимор, Мериленд, Leventhal Howard (Левентхол Говард) из Университета Руджерса, Нью-Джерси. Разрешение на проведение процедуры валидации русскоязычной версии получено официально от основного автора Вилейкюте Л.
Цель исследования
Цель исследования состояла в валидации русскоязычной версии специфического опросника NeuroQol для оценки качества жизни больных с ДПН.
Материалы и методы
В исследовании принял участие 371 пациент, который обратился за помощью в отделения/кабинеты диабетической стопы медицинских учреждений Департамента здравоохранения города Москвы. После подробного и тщательного сбора анамнеза и жалоб всем пациентам проводилась оценка периферической чувствительности и магистрального кровотока.
Все участники исследования добровольно приняли решение о прохождении обследования в рамках исследования и лично подписали информированное согласие, согласно правилам GCP. Протокол исследования был утвержден на заседании локального этического комитета.
Оценка периферической чувствительности
Состояние периферической чувствительности определялось степенью выраженности болевой симптоматики и нарушений чувствительности нижних конечностей.
Для определения степени выраженности болевой симптоматики применялась шкала Нейропатического симптоматического счета (шкала НСС). При этом каждой жалобе (симптому) присваивался 1 балл, если он присутствовал, и 2 балла, если усиливался ночью. Сумма баллов отражала состояние больного по шкале НСС [9].
Сумма баллов отражала состояние больного по шкале НСС [9].
Для оценки состояния чувствительности нижних конечностей проводился клинический неврологический осмотр с исследованием сенсорной и моторной функций периферических нервов. Сенсорная функция оценивалась при помощи стандартных методик исследования различных видов чувствительностей (тактильной, вибрационной, болевой, температурной). Моторная функция оценивалась при помощи исследования коленных и ахилловых рефлексов.
Для оценки тактильной чувствительности применялась методика с использованием монофиламента весом 10 г (5.07 Semmes-Weinstein). Исследование проводилось в положении пациента лежа на спине, в спокойном, расслабленном состоянии. На подошвенной поверхности стоп в определенных точках (подошвенная поверхность 1-го пальца, проекции 1-го и 5-го плюснефаланговых сочленений) исследователь прикасался монофиламентом. Тактильная чувствительность считалась ненарушенной, если пациент ощущал два из трех прикосновений. Тактильная чувствительность нарушена, если пациент не ощущал два прикосновения из трех [10].
Болевая чувствительность была исследована при помощи «тупой» иглы. Исследование проводилось на тыльной поверхности 1-го пальца обеих стоп. Болевая чувствительность считалась не нарушенной, если пациент чувствовал боль от укола.
Температурную чувствительность оценивали при помощи термического наконечника тип-терм (Thip-term). Исследование проводилось на тыльной поверхности 1-го пальца обеих стоп. Температурная чувствительность считалась не нарушенной, если пациент ощущал разницу температур в исследуемых точках.
Вибрационную чувствительность оценивали при помощи биотезиометра. Исследование проводилось на тыльной поверхности 1-го пальца в области плюснефалангового сочленения. При исследовании уточнялся момент, когда пациент начинал чувствовать вибрацию прибора. Вибрационная чувствительность считалась не нарушенной, если пациент начинал чувствовать вибрацию при показаниях шкалы, прибора равных 7–9 В (Вольт).
Оценка коленных и ахилловых рефлексов проводилась по стандартной методике при помощи неврологического молоточка.

Для определения степени тяжести ДПН проводилась количественная оценка имеющихся расстройств в соответствии со шкалой нейропатического дисфункционального счета (НДС), разработанной M.J. Young в 1986 г. и рекомендованной исследовательской группой Neurodiab при Европейской ассоциации по изучению диабета. При расчете по шкале НДС каждому виду чувствительности присваивается определенный балл в зависимости от выявленного уровня нарушения. В дальнейшем для каждого вида чувствительных нарушений вычисляется средняя величина баллов по двум ногам (табл. 1). Значения шкалы НДС от 0 до 4 баллов свидетельствуют об отсутствии либо наличии у пациента начальных признаков ДПН, от 5 до 13 баллов – соответствуют умеренно выраженной нейропатии, НДС ≥14 баллам соответствует выраженной ДПН [9].
Пациент относится к группе высокого риска развития СДС, если он:
- не ощущает прикосновения монофиламента более чем в одной точке, либо
- не чувствует боли при уколе «тупой» иглой тыльной поверхности 1-го пальца;
- не чувствует вибрацию при исследовании камертоном или вибрационная чувствительность по показаниям биотезиометра ≥25 В (10).

Оценка состояния магистрального кровотока нижних конечностей
В качестве скрининга нарушения магистрального кровотока исследовалась пульсация на передней и задней тибиальных артериях путем их пальпации. Выявленное отсутствие или ослабление пульсации на указанных сосудах в ряде случаев подтверждалось инструментально с вычислением лодыжечно-плечевого индекса (ЛПИ=АД в исследуемой артерии/АД в плечевой артерии). В норме ЛПИ≥0,9, но <1,5. Магистральный кровоток нижних конечностей считался нарушенным при отсутствии пульсации хотя бы на одной из тибиальных артерий и/или ЛПИ<0,8.
По результатам осмотра оценивалось соответствие пациента критериям включения и исключения, после чего предлагалось заполнить опросник по оценке КЖ.
Критерии включения пациентов в исследование- СД 1 или 2 типа (СД1 и СД2).
- Возраст >18 лет.
- Наличие объективных признаков ДПН средней и тяжелой степени выраженности: вибрационная чувствительность >25 Вольт, и/или снижение/отсутствие тактильной чувствительности при исследовании монофиламентом весом 10 г, и/или шкала НДС≥10 баллов.
/24/1.png)
- Способность понять и ответить на вопросы предлагаемого опросника.
- Отсутствие пульсации на одной и более тибиальных артериях.
- ЛПИ<0,8.
- Оперативное восстановление магистрального кровотока за 6 месяцев до включения в исследование.
- Ампутации нижних конечностей выше уровня голеностопного сустава.
- Неспособность понять и ответить на вопросы предлагаемого опросника.
Заполнение опросников больными без нейропатии не проводилось, так как в работе валидировали не новый опросник, а уже созданный, прошедший процедуру подтверждения внешней специфичности.
Валидация опросника
Обязательной процедуре валидации подвергаются опросники, разработанные впервые, а также при адаптации уже валидированных опросников к языковым и культурным особенностям той или иной страны. В последнем случае валидация состоит из следующих этапов: перевод, предварительное тестирование, оценка надежности, оценка валидности.
На первом этапе проводился перевод опросника с английского на русский язык двумя независимыми переводчиками. После обсуждения полученных переводов и устранения различий (при их наличии) была создана первая промежуточная версия опросника. На следующем этапе эта версия была переведена на английский язык также двумя независимыми переводчиками – 2-я промежуточная версия опросника. Окончательная корректировка проводилась при сравнении оригинальной версии со 2-й промежуточной. Выявленные неточности были устранены. В результате создана окончательная версия, при помощи которой проводилось предварительное (пилотное) тестирование. Его целью было провести интервьюирование небольшого количества пациентов и выяснить, насколько понятны задаваемые вопросы. В пилотном тестировании приняли участие 27 пациентов, которые охарактеризовали вопросы опросника как понятные, ясно и четко сформулированные. Сложностей с заполнением не было ни у одного пациента.
Оценка надежности опросникаНадежность – это способность опросника давать постоянные и точные измерения. Для определения этого параметра вычисляется коэффициент α Кронбаха. Значения ≥0,7 для групповых исследований считаются удовлетворительными.
Для определения этого параметра вычисляется коэффициент α Кронбаха. Значения ≥0,7 для групповых исследований считаются удовлетворительными.
Критериальная валидность – выявление взаимосвязей шкал опросника с каким-либо внешним критерием – определяется при помощи вычисления коэффициента корреляции шкал опросника с каким-либо внешним критерием. В нашем случае это выраженность болевого синдрома, степень выраженности объективных нарушений чувствительности, наличие язвенного дефекта на момент заполнения опросника.
Конструктная валидность – один из наиболее важных показателей валидности опросника, позволяющий оценить, насколько структура опросника позволяет достоверно измерить то, что он должен измерить. Для оценки конструктной валидности выполняется факторный анализ.
Структура опросника NeuroQol
Опросник состоит из 28 вопросов, объединенных в 6 шкал. Каждая шкала содержит от 3 до 7 вопросов (табл. 2).
Три шкалы – боли (жжение, покалывание, стреляющая боль и т. д.), субъективного снижения или отсутствия чувствительности (онемение и т.д.), диффузных сенсомоторных нарушений (нестабильность походки, слабость в руках и т.д.) оценивают степень выраженности симптомов ДПН и отражают физическое состояние больного. Четыре шкалы – ограничение ежедневной активности (возможность работать, выполнять домашнюю работу или работу в саду/огороде и т.д.), физической/эмоциональной зависимости от других (насколько сильно осложнения стоп влияли на ваши взаимоотношения с близкими людьми, изменилась ли ваша роль в семье из-за осложнений со стороны стоп и т.д.), эмоций (осложнения со стороны стоп превратили мою жизнь в сражение, я не уверен в себе из-за этих осложнений и т.д.) выявляют психосоциальное функционирование. Заключительный вопрос касался общей оценки качества своей жизни. Пациенту предлагалось 5 вариантов ответа, сформированных по принципу шкалы Ликерта (все время, часто, иногда, редко, никогда). Каждому ответу присваивался балл от 1 до 5.
д.), субъективного снижения или отсутствия чувствительности (онемение и т.д.), диффузных сенсомоторных нарушений (нестабильность походки, слабость в руках и т.д.) оценивают степень выраженности симптомов ДПН и отражают физическое состояние больного. Четыре шкалы – ограничение ежедневной активности (возможность работать, выполнять домашнюю работу или работу в саду/огороде и т.д.), физической/эмоциональной зависимости от других (насколько сильно осложнения стоп влияли на ваши взаимоотношения с близкими людьми, изменилась ли ваша роль в семье из-за осложнений со стороны стоп и т.д.), эмоций (осложнения со стороны стоп превратили мою жизнь в сражение, я не уверен в себе из-за этих осложнений и т.д.) выявляют психосоциальное функционирование. Заключительный вопрос касался общей оценки качества своей жизни. Пациенту предлагалось 5 вариантов ответа, сформированных по принципу шкалы Ликерта (все время, часто, иногда, редко, никогда). Каждому ответу присваивался балл от 1 до 5.
Результаты
Клиническая характеристика обследованной группы представлена в табл.
 3.
3.В исследовании принял участие 371 пациент. Средний возраст больных составил 60,5±10,4 лет, среди них женщин было 69%. СД2 был у 87% обследованных со средней продолжительностью заболевания 13,3±9,1 лет и уровнем HbA1c 8,2±1,3 %. 38% пациентов ранее обучались в школе для больных СД. Выраженность болевой симптоматики (шкала НСС) составила 4 балла. Средний уровень вибрационной чувствительности составил 35,5±14,7 Вольт (норма 7–10 В), средний уровень баллов шкалы НДС 11,6±5,5, что соответствует средней и тяжелой степени выраженности ДПН. У 44% пациентов на момент заполнения опросника были открытые язвенные дефекты стоп, у 37% – нейропатические язвенные дефекты в анамнезе.
На первом этапе валидации опросника NeuroQol проводилась оценка его надежности при помощи вычисления коэффициента внутренней согласованности (коэффициент α Кронбаха) для каждой шкалы. В табл. 4 представлены полученные результаты.
По всем шкалам значения коэффициента α Кронбаха превышают значение 0,8, что соответствует хорошим показателям и говорит о том, что опросник надежен. Дополнительный анализ на избыточность русскоязычной версии опросника путем пошагового исключения каждого компонента шкал с коэффициентом α Кронбаха ≥0,9 не проводился в связи с малым количеством пунктов в данных шкалах (3 и 4 соответственно).
Дополнительный анализ на избыточность русскоязычной версии опросника путем пошагового исключения каждого компонента шкал с коэффициентом α Кронбаха ≥0,9 не проводился в связи с малым количеством пунктов в данных шкалах (3 и 4 соответственно).
Для определения критериальной валидности вычислялся коэффициент корреляции Спирмена (r) между шкалами опросника и внешними параметрами, такими, как выраженность болевой симптоматики (шкала НСС), степень тяжести периферической нейропатии (шкала НДС) и наличие язвенного дефекта на стопе/стопах на момент заполнения опросника. Результаты анализа представлены в табл. 5.
Полученные результаты демонстрируют наличие значимой корреляции между шкалами опросника и степенью тяжести нейропатии. Отрицательный знак коэффициента корреляции говорит о том, что выраженность того или иного признака обратно пропорциональна баллам шкалы. Так, например, чем более выражен болевой синдром, тем меньшее количество баллов в шкале боли. Следует отметить, что не обнаружено связи между степенью тяжести нейропатии (шкала НДС) и шкалой боли опросника. Это подтверждает факт, что у больных с объективными признаками выраженного снижения чувствительности болевая симптоматика не является доминирующей. При этом у данной категории больных такая жалоба как онемение конечностей присутствует значительно чаще. Об этом свидетельствует значимая корреляция между шкалой НДС и шкалой субъективного снижения или отсутствия чувствительности в стопах опросника. Субъективный показатель степени выраженности болевой симптоматики (шкала НСС) имеет значимую связь со всеми шкалами опросника, относящимися к физической составляющей, и с одной шкалой эмоций психосоциального функционирования. При этом объективное снижение чувствительности (шкала НДС) значимо ассоциировано только с ощущением онемения (шкала субъективного снижения или отсутствия чувствительности) физической составляющей опросника качества жизни и двумя шкалами психосоциального функционирования. Полученные данные говорят о том, что различные проявления и степень тяжести ДПН по-разному влияют на физическую и психосоциальную составляющие КЖ.
Это подтверждает факт, что у больных с объективными признаками выраженного снижения чувствительности болевая симптоматика не является доминирующей. При этом у данной категории больных такая жалоба как онемение конечностей присутствует значительно чаще. Об этом свидетельствует значимая корреляция между шкалой НДС и шкалой субъективного снижения или отсутствия чувствительности в стопах опросника. Субъективный показатель степени выраженности болевой симптоматики (шкала НСС) имеет значимую связь со всеми шкалами опросника, относящимися к физической составляющей, и с одной шкалой эмоций психосоциального функционирования. При этом объективное снижение чувствительности (шкала НДС) значимо ассоциировано только с ощущением онемения (шкала субъективного снижения или отсутствия чувствительности) физической составляющей опросника качества жизни и двумя шкалами психосоциального функционирования. Полученные данные говорят о том, что различные проявления и степень тяжести ДПН по-разному влияют на физическую и психосоциальную составляющие КЖ. Таким образом, выявленные показатели демонстрируют адекватную критериальную валидность NeuroQol.
Таким образом, выявленные показатели демонстрируют адекватную критериальную валидность NeuroQol.
Психометрическая оценка опросника (конструктная валидность) проводилась с помощью факторного анализа методом выделения главных компонент с варимакс вращением. Отбирались факторы, собственные значения которых превышали единицу. Факторный анализ проводился отдельно для шкал, составляющих физическое функционирование, и шкал, относящихся к психосоциальному компоненту. Выбранные факторы объясняют 65% совокупной дисперсии. Результаты представлены в табл. 6.
Согласно полученным данным, выделены следующие факторы, относящиеся к физической составляющей качества жизни: «боль», «снижение чувствительности», «нарушение баланса». Психосоциальная составляющая КЖ представлена факторами, характеризующими ежедневную активность и межличностные взаимоотношения («активность и взаимоотношения»), эмоциональный фон («эмоции») и ощущение неуверенности, возникающее из-за осложнений стоп («неуверенность»).
Вопросы, входящие в тот или иной фактор, т.е. имеющие большую факторную нагрузку, хорошо интерпретируются и не противоречат заложенному в них смыслу. Например, фактор «боль» содержит только вопросы, касающиеся болевых ощущений. Фактор «активность и взаимоотношения» объединил вопросы шкал «ограничение ежедневной активности» и «физическая/эмоциональная зависимость от других», а в такие факторы, как «эмоции» и «неуверенность» вошли вопросы из шкалы эмоций опросника. Все вышеизложенное подтверждает валидность опросника с точки зрения его структуры.
Показатели КЖ у больных с ДПН, исследованные при помощи специфического опросника NeuroQol
При общей оценке своего КЖ по пятибалльной системе оценили его как «отличное» и «очень хорошее» 1,4% пациентов, как «хорошее» – 24,4%, как «не очень хорошее» – 62%, как «плохое» – 10,7 % (рис. 1).
При сравнительном исследовании общей оценки КЖ на момент заполнения опросника свое КЖ как «хорошее» оценили 28,7% больных с наличием открытой раны на стопе и 21,5% – без ран, как «не очень хорошее» – 60% пациентов с нСДС и 67% без язвенных дефектов, как «плохое» – 12,6% больных с нСДС и 9% без ран (рис. 2). Полученные различия статистически не значимы.
2). Полученные различия статистически не значимы.
Для выявления предикторов определенного уровня КЖ был проведен порядковый регрессионный анализ. В качестве зависимой переменной использовался уровень КЖ, а независимыми предикторами выступали выявленные факторы. Также учитывался факт наличия или отсутствия язвенного дефекта на момент заполнения опросника (табл. 7).
В процессе анализа не было выявлено зависимости уровня КЖ от наличия открытой раны на момент заполнения опросника. Состояния, сопровождающиеся нарушением устойчивости, онемением, неспособностью ощущать предметы и/или разницу между холодным и горячим, не влияли на общую оценку качества жизни пациентом. Также не влияло на качество жизни ощущение неуверенности в себе. Из физических факторов значимое влияние на КЖ оказывала только болевая симптоматика. Согласно полученным данным, на уровень КЖ значимо воздействовали факторы, относящиеся к психосоциальной сфере: снижение ежедневной активности, межличностные отношения, физическая и эмоциональная зависимость от близких, при этом, как было указано выше, независимо от наличия или отсутствия открытой раны.
Заключение
Представленные данные показывают, что русскоязычная версия опросника NeoroQol является надежной и валидной. Данный опросник может использоваться для оценки КЖ у больных с признаками ДПН, включая оценку эффективности различных методов лечения осложнения. Одной из особенностей работы является однородность исследуемой выборки. У всех пациентов были объективные признаки ДПН средней и тяжелой степени выраженности. В процессе анализа было выявлено, что общая оценка КЖ этой соматически тяжелой категории больных не зависит от наличия язвенного дефекта. Субъективная оценка КЖ у пациентов с наличием язвенных дефектов статистически не отличалась от показателей у пациентов без открытых ран на стопах. На основании проведенного анализа получило подтверждение отмеченное выше утверждение, что субъективная оценка КЖ не является аналогом измерения физического и психоэмоционального статуса пациента. В данном аспекте следует отметить, что все пациенты, принявшие участие в исследовании, получали квалифицированную помощь в специализированных центрах Москвы. Такая помощь предполагает частый мониторинг состояния больного и наличие положительного эффекта лечения в большинстве случаев. Пациент чувствует, что о нем заботятся, он не брошен и это, безусловно, не может не влиять на его оценку КЖ. Полученные данные согласуются с имеющимися в литературе сведениями о том, что показатели КЖ у пациентов, получающих специализированное лечение, значимо выше, чем у таких же пациентов, но наблюдающихся в обычных клиниках [11]. Одним из несомненных преимуществ использования NeuroQol является возможность выявить факторы, которые значимо ухудшают КЖ. Такими факторами в нашей работе явились болевая симптоматика и психоэмоциональное состояние больного. При этом снижение физического функционирования больного, связанное с нарушением баланса и чувством онемения, не влияло на оценку КЖ.
Такая помощь предполагает частый мониторинг состояния больного и наличие положительного эффекта лечения в большинстве случаев. Пациент чувствует, что о нем заботятся, он не брошен и это, безусловно, не может не влиять на его оценку КЖ. Полученные данные согласуются с имеющимися в литературе сведениями о том, что показатели КЖ у пациентов, получающих специализированное лечение, значимо выше, чем у таких же пациентов, но наблюдающихся в обычных клиниках [11]. Одним из несомненных преимуществ использования NeuroQol является возможность выявить факторы, которые значимо ухудшают КЖ. Такими факторами в нашей работе явились болевая симптоматика и психоэмоциональное состояние больного. При этом снижение физического функционирования больного, связанное с нарушением баланса и чувством онемения, не влияло на оценку КЖ.
В заключение следует отметить, что полученные данные позволяют оценить СД диабетом, осложненным ДПН и нСДС. Наши данные свидетельствуют о том, что более важными факторами являются не физические, а межличностные и психосоциальные составляющие.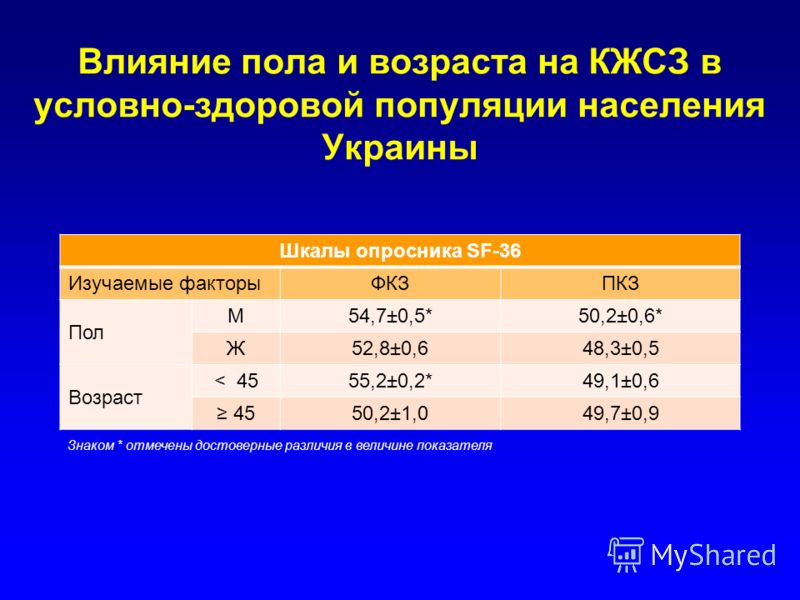 Именно на эти компоненты должны быть направлены усилия специалистов для улучшения КЖ данной категории больных.
Именно на эти компоненты должны быть направлены усилия специалистов для улучшения КЖ данной категории больных.
Информация о финансировании и конфликте интересов
Работа проводилось в рамках бюджетного финансирования НИР ГБУЗ «Эндокринологический диспансер Департамента здравоохранения города Москвы».
Авторы заявляют об отсутствии потенциальных и явных конфликтов интересов, связанных с проведенным исследованием и публикацией его результатов.
опросник SF-36 | bloodjournal
КЛИНИКА, ДИАГНОСТИКА И ЛЕЧЕНИЕ ЛИМФОИДНЫХ ОПУХОЛЕЙ качество жизни, лимфома Ходжкина, молодые взрослые, опросник SF-36, подростки, протокол DAL-HD-90m
Е.Г. Аршанская1,2, С.В. Семочкин2,3, А.Г. Румянцев2,3
1 ГУЗ «ГКБ им. С.П. Боткина», Москва, Российская Федерация
2 ФГБУ «ФНКЦ детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» МЗ РФ, Москва, Российская Федерация
3 ГБОУ ВПО «Российский национальный медицинский исследовательский университет им. Н.И. Пирогова» МЗ РФ, Москва, Российская Федерация
Н.И. Пирогова» МЗ РФ, Москва, Российская Федерация
РЕФЕРАТ
Ухудшение качества жизни (КЖ) и поздние осложнения противоопухолевой терапии лимфомы Ходжкина (ЛХ) представляют важную медицинскую проблему, поскольку касаются, как правило, молодых людей с большой продолжительностью предстоящей жизни.
Цель. Оценить КЖ пациентов с длительными ремиссиями ЛХ после программной терапии по педиатрическому протоколу DAL-HD-90m.
Пациенты и методы. В исследование включено 56 пациентов с ЛХ в возрасте 22–41 год (медиана возраста 27,5 года). Лиц мужского пола было 22, женского — 34. Всем больным проводилось лечение по поводу ЛХ по протоколу DAL-HD-90m в период с 1997 по 2007 г. Для сравнения подобрана группа из 94 человек в возрасте 22–46 лет (медиана 28 лет) без онкологических и других хронических заболеваний. Среди них мужчин было 44, женщин — 50. КЖ оценено с помощью опросника общего профиля SF-36, который позволяет генерировать 8 отдельных шкал и 2 итоговых индекса, характеризующих состояние здоровья (0 — наихудший статус, 100 — наилучший). Все пациенты имели продолжительность полной ремиссии ЛХ не менее 5 лет.
Все пациенты имели продолжительность полной ремиссии ЛХ не менее 5 лет.
Результаты. Дефицит КЖ у пациентов с длительными ремиссиями ЛХ по сравнению со здоровыми сверстниками подтвержден по большинству шкал физического и психического здоровья. Наиболее существенным (отклонение 10 баллов и более) было снижение показателей общего здоровья — 53,4 (95% ДИ 47,8–59,1)
vs 72,3 (95% ДИ 68,8–75,8; p < 0,001), жизненной активности — 54,7 (95% ДИ 50,4–59,1) vs 72,2 (95% ДИ 69,3–75,2; p < 0,001) и психического здоровья — 57,4 (95% ДИ 53,5–61,4) vs 71,7 (95% ДИ 68,6–74,8; p < 0,001) соответственно. Пациенты в возрасте 18,5 года и старше на момент диагностики ЛХ (метод ROC-кривых; p = 0,047) имели более низкие показатели КЖ, что было документировано по снижению общего здоровья — 48,3 (95% ДИ 41,3–55,2) vs 60,9 (95% ДИ 51,6–70,2; p = 0,027) и жизненной активности — 50,3 (95% ДИ 44,7–55,9) vs 61,1 (95% ДИ 51,6–70,2; p = 0,013) соответственно.
Заключение. Для пациентов, излеченных в подростковом и молодом возрасте от ЛХ, характерно значимое снижение показателей КЖ по сравнению со здоровыми сверстниками. Возраст к началу терапии 18,5 года и более служит независимым прогностическим фактором, определяющим степень ограничения физического и психического благополучия в отдаленный период.
Ключевые слова: лимфома Ходжкина, качество жизни, подростки, молодые взрослые, протокол DAL-HD-90m, опросник SF-36
Читать статью в PDF
ЛИТЕРАТУРА
- Злокачественные новообразования в России в 2012 г. (заболева- емость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Пе- тровой. М.: ФГБУ «МНИОИ им. П.А. Герцена» МЗ РФ, 2014. [Sostoyaniye onkologicheskoy pomoshchi naseleniyu Rossii v 2012 g. Pod red. A.D. Kaprina, V.V. Starinskogo, G.V. Petrovoy (Status of oncological care for population of Russia in 2012. Ed. by A.D.Kaprin, V.V. Starinsky, and G.V. Petrova). M.: FGBU MNIO im. P.A. Gertsena Minzdravsotsrazvitiya Rossii 2014.]
- Morton L.M., Wang S.S., Devesa S.S. et al. Lymphoma incidence patterns by WHO subtype in the United States, 1992–2001. Blood 2006; 107(1): 265–76.
- Румянцев А.Г., Птушкин В.В., Семочкин С.В. Пути улучшения ре- зультатов лечения злокачественных опухолей у подростков и молодых взрослых. Онкогематология 2011; 1: 20–30. [Rumyantsev A.G., Ptushkin V.V., Semochkin S.V. Approaches to improvement of treatment outcomes in adolescents and young adults with malignancies. Onkogematologiya 2011; 1: 20–30. (In Russ.)].
- Evens A.M., Hutchings M., Diehl V. Treatment of Hodgkin lymphoma: the past, present, and future. Nat. Clin. Pract. Oncol. 2008; 5(9): 543–56.
- Sasse S., Klimm B., Gorgen H. et al. Comparing long-term toxicity and efficacy of combined modality treatment including extended- or involved-field radiotherapy in early-stage Hodgkin’s lymphoma. Ann. Oncol. 2012; 23(11): 2953–9.
- Robison L.L., Green D.M., Hudson M. et al. Long-term outcomes of adult survivors of childhood cancer. Cancer 2005; 104(11): 2557–64.
- Shah A.B., Hudson M.M., Poquette C.A. et al. Long-term follow-up of patients treated with primary radiotherapy for supradiaphragmatic Hodgkin’s disease at St.
 Jude Children’s Research Hospital. Int. J. Radiat. Oncol. Biol. Phys. 1999; 44(4): 867–77.
Jude Children’s Research Hospital. Int. J. Radiat. Oncol. Biol. Phys. 1999; 44(4): 867–77. - Феоктистов Р.И., Румянцева Ю.В., Абугова Ю.Г. и др. Результаты лечения детей и подростков с лимфомой Ходжкина: данные многоцентро- вого исследования. Онкогематология 2010; 1: 31–6. [Feoktistov R.I., Rumyantseva Yu.V., Abugova Yu.G., et al. Treatment outcomes in children and adolescents with Hodgkin’s lymphoma: data of multicenter study. Onkogematologiya 2010; 1: 31–6. (In Russ.)].
- Schellong G., Riepenhausen M., Bruch C. et al. Late valvular and other cardiac diseases after different doses of mediastinal radiotherapy for Hodgkin disease in children and adolescents: report from the longitudinal GPOH followup project of the German-Austrian DAL-HD studies. Pediatr. Blood Cancer 2010; 55(6): 1145–52.
- Демина Е.А., Пылова И.В., Шмаков Р.Г., Перилова Е.Е. Поздние ослож- нения терапии больных лимфомой Ходжкина. Совр. онкол. 2006; 1: 36–43. [Demina Ye.A., Pylova I.V., Shmakov R.G.
/56/56_2.jpg) , Perilova Ye.Ye. Late complications of therapy in patients with Hodgkin’s lymphoma. Sovr. onkol. 2006; 1: 36–43. (In Russ.)]. 11. Ng A.K., LaCasce A., Travis L.B. Long-term complications of lymphoma and its treatment. J. Clin. Oncol. 2011; 29(14): 1885–92.
, Perilova Ye.Ye. Late complications of therapy in patients with Hodgkin’s lymphoma. Sovr. onkol. 2006; 1: 36–43. (In Russ.)]. 11. Ng A.K., LaCasce A., Travis L.B. Long-term complications of lymphoma and its treatment. J. Clin. Oncol. 2011; 29(14): 1885–92. - Gil-Fernandez J., Ramos C., Tamayo T. et al. Quality of life and psychological well-being in Spanish long-term survivors of Hodgkin’s disease: results of a controlled pilot study. Ann. Hematol. 2003; 82(1): 14–8.
- Khimani N., Chen Y.H., Mauch P.M. et al. Influence of new late effects on quality of life over time in Hodgkin lymphoma Survivors: a longitudinal survey study. Ann. Oncol. 2013; 24(1): 226–30.
- Hjermstad M.J., Fossa S.D., Oldervoll L. et al. Fatigue in long-term Hodgkin’s disease survivors: a follow-up study. J. Clin. Oncol. 2005; 23(27): 6587–95.
- Ruffer J.U., Flechtner H., Tralls P. et al. Fatigue in long-term survivors of Hodgkin’s lymphoma; a report from the German Hodgkin Lymphoma Study Group (GHSG).
 Eur. J. Cancer 2003; 39(15): 2179–86.
Eur. J. Cancer 2003; 39(15): 2179–86. - Новик А.А., Ионова Т.И. Руководство по исследованию качества жизни в медицине. Под ред. Ю.Л. Шевченко, 2-е изд. М.: Олма Медиагрупп, 2007. [Novik A.A., Ionova T.I. Rukovodstvo po issledovaniyu kachestva zhizni v meditsine. Pod red. Yu.L. Shevchenko, 2-e izd. (Manual on evaluation of quality of life in medicine. Ed by.: Yu.L. Shevchenko, 2nd ed.) M.: Olma Mediagrup, 2007]
- Давыдкин И.Л., Булгакова С.В., Шафиева И.А. Подходы к реаби- литации пациентов в Самарском областном межведомственном центре профилактики остеопороза. Аллергол. и иммунол. 2007; 8(1): 276. [Davydkin I.L., Bulgakova S.V., Shafiyeva I.A. Approaches to rehabilitation of patients in Samara regional interdisciplinary center for osteoporosis prevention. Allergol. i immunol. 2007; 8(1): 276. (In Russ.)].
- Semochkin S.V., Arshanskaya E.G., Bobkova M.M., Rumiantsev A.G. A long-term follow-up report on the modified pediatric protocol DAL-HD-90 for adolescents and young adults with Hodgkin lymphoma.
 Pediatr. Blood Cancer 2012; 59(6): 1042.
Pediatr. Blood Cancer 2012; 59(6): 1042. - Семочкин С.В., Лория С.С., Румянцев А.Г., Сотников В.М. Лечение лимфомы Ходжкина у подростков и молодых взрослых. Онкогематология 2008; 1: 18–26. [Semochkin S.V., Loriya S.S., Rumyantsev A.G., Sotnikov V.M. Management of Hodgkin’s lymphoma in adolescents and young adults. Onkogematologiya 2008; 1: 18–26. (In Russ.)].
- Ware J.E., Kosinski M. Interpreting SF-36 summary health measures: a response. Qual. Life Res. 2001; 10(5): 405–13.
- Van Tulder M.W., Aaronson N.K., Bruning P.F. The quality of life of longterm survivors of Hodgkin’s disease. Ann. Oncol. 1994; 5(2): 153–8.
- Loge J.H., Abrahamsen A.F., Ekeberg O., Kaasa S. Reduced healthrelated quality of life among Hodgkin’s disease survivors: a comparative study with general population norms. Ann. Oncol. 1999; 10(1): 71–7.
- Mols F., Vingerhoets A.J., Coebergh J.W. et al. Better quality of life among 10–15 year survivors of Hodgkin’s lymphoma compared to 5–9 year survivors: a population-based study.

|
|
|||||
Название вопросникаКраткая форма медицинского обследования MOS, состоящая из 36 пунктов (MOS SF-36) ОписаниеОбщий показатель качества жизни, связанный со здоровьем. Инструмент широко используется для оценки HRQL в различных группах населения 4 . РазработчикAL Stewart, R Hays, JE Ware and RAND Corporation 2 . Адрес
Электронная почта MOTrust@worldnet. URL-адресwww.outcomes-trust.org Стоимость и доступностьСвяжитесь с Medical Outcomes Trust или RAND Corporation АдминистрацияЯ, интервьюер Время завершить5 минут Количество позиций36 Домены и категории8 Наименование категорий/доменовФизическое функционирование; ролевые ограничения из-за физического здоровья проблемы; телесная боль; социальное функционирование; общее психическое здоровье; ролевые ограничения из-за эмоциональных проблем, жизненных сил, энергии или усталость; общие представления о здоровье. Масштабирование предметов Переменная шкала для различных вопросов, включая: Отлично,
очень хороший, хороший, справедливый, плохой; Ограничено много, ограничено немного, не
вообще ограничено; Да нет; Совсем нет, чуть-чуть, умеренно, совсем
немного, чрезвычайно; Нет, очень легкая, легкая, средняя, тяжелая, очень
серьезный; Все время, большую часть времени, большую часть времени,
иногда, немного времени, никогда; и
другие. Подсчет очковОценка по 8 доменам и компонент общего физического и психического здоровья суммарные баллы Надежность
Срок действияПосле поправки на возраст были значительные, но слабые корреляции между ОФВ1, % прогнозируемого и субшкалами SF-36, включая физическое функционирование, ограничения физической роли, боль, общее восприятие здоровья и изменение состояния здоровья 9 . Продемонстрирована дискриминантная валидность путем дифференциации между пациентами 5 степеней астмы серьезность 9 . ОперативностьСообщено Исследовательское использованиеСообщено Клиническое применениеСообщено 6 Комментарии Острая версия (1-недельный период отзыва) также использовалась в
астма
7
. ЯзыкОригинал: английский (США) Переводы: голландский, испанский 8 , Шведский, французский, немецкий, итальянский, датский, японский Каталожные номера
Дата информациимарт 1999 г. |
|||||
|
Copyright © 2007 Американское торакальное общество · Требования к веб-сайту |
|||||
Краткая форма 36 (SF-36) — SCIRE Professional
Перейти к содержимомуХанна Гудингс2022-07-19T11:22:52-07:00
- Общий показатель состояния здоровья, введенный в 1992 г., переведенный на различные языки и используемый во всем мире.
- Предназначен для применения ко всем состояниям здоровья и оценки концепций здоровья, которые представляют собой основные человеческие ценности и имеют отношение к функциональному состоянию и благополучию человека.

- содержит 36 вопросов, охватывающих восемь доменов:
1) Физическое функционирование
2) Ролевые ограничения из-за проблем с физическим здоровьем
3) Телесная боль
4) Общее состояние здоровья
5) Жизнеспособность
6) Социальное функционирование
7) Ролевые ограничения из-за эмоциональных проблем
8) Психическое здоровье
- содержит 36 вопросов, охватывающих восемь доменов:
- Ответы основаны на шкале Лайкерта. Используются как стандартная (4 недели), так и острая (1 неделя) версии отзыва. Версия 2 опросника SF-36 была выпущена в 1996 г., и были внесены некоторые изменения в формат, формулировку вопросов и варианты ответов.
Клинические соображения
- SF-36 является наиболее широко используемым обследованием состояния здоровья и применялось при ТСМ. Он широко использовался для различения, оценки и прогнозирования результатов при различных состояниях здоровья, но требуется дополнительная работа для изучения достоверности вопросов и предлагаемых модификаций вопросов для популяции пациентов с ТСМ.

- Считается, что вопросы, связанные с ходьбой и подъемом по лестнице, нечувствительны к людям с полной травмой спинного мозга.
Домен ICF
Качество жизни
Инструкции по использованию и подсчету баллов
Администрирование
Ведется интервьюером или самостоятельно.
Количество предметов
36
Оборудование
Нет
Подсчет очков
- В руководстве (которое необходимо приобрести) есть алгоритм подсчета очков для преобразования оценок предметов в систему подсчета очков от 0 до 100.
- Также используется оценка на основе нормы, где средний балл для генеральной совокупности равен 50 при стандартном отклонении 10 (алгоритм оценки описан вручную).
- SF-36 также может быть оценен с использованием двух суммарных баллов, физического и умственного компонентов, которые основаны на норме.
Языки
SF-36 переведен более чем на 50 языков.2007/ST102/Untitled-1.gif)
Требуется обучение
Нет
Доступность
Можно узнать, связавшись с Quality Metric (www.qualitymetric.com). Покупка руководств, а также использование инструментов требует затрат (в зависимости от того, как они будут использоваться).
Статистические свойства
Количество исследований, сообщающих о психометрических свойствах: 11
Интерпретируемость
MCID: не установлено при ТСМ, но для выборки пациентов с остеоартритом нижних конечностей (n=142, средний возраст: 65,1 года, 70,5% женщин, 61,5% страдали остеоартрозом коленного сустава, 35,2% принимали НПВП или анальгетики):
| Подшкалы SF-36: | MCID при ухудшении | MCID для улучшения |
|---|---|---|
| Телесная боль | 7,2 | 7,8 |
| Физическая функция | 5,3 | 3,3 |
| Обзор физических компонентов | 2,0 | 2,0 |
Ссылка: Angst et al. 2001. «Наименьшие обнаруживаемые и минимальные клинически важные различия реабилитационного вмешательства с их последствиями для требуемых размеров выборки с использованием инструментов измерения качества жизни WOMAC и SF-36 у пациентов с остеоартритом нижних конечностей» Arthritis Care & Research, 45 (4), 384–391. SEM и MDC: показатель SF-36 SEM и MDC (рассчитано на основе данных Lin et al., 2007):
2001. «Наименьшие обнаруживаемые и минимальные клинически важные различия реабилитационного вмешательства с их последствиями для требуемых размеров выборки с использованием инструментов измерения качества жизни WOMAC и SF-36 у пациентов с остеоартритом нижних конечностей» Arthritis Care & Research, 45 (4), 384–391. SEM и MDC: показатель SF-36 SEM и MDC (рассчитано на основе данных Lin et al., 2007):
| Подшкалы SF-36: | СЭМ | МДЦ |
|---|---|---|
| Физическое функционирование | 21,4 | 59,4 |
| Физическая роль | 14,7 | 40,8 |
| Телесная боль | 7,4 | 20,6 |
| Общее состояние здоровья | 7,9 | 21,8 |
| Живучесть | 4,6 | 12,7 |
| Социальное функционирование | 5,9 | 16,3 |
| Эмоциональная роль | 4.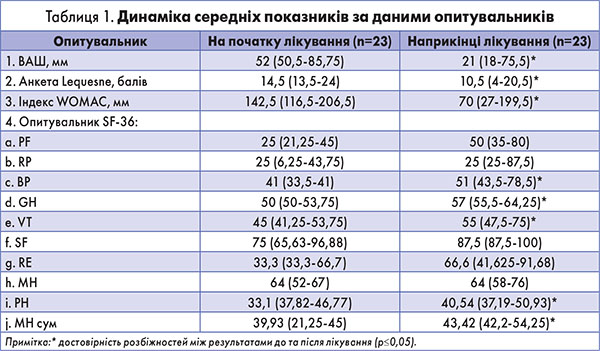 1 1 |
11,3 |
| Психическое здоровье | 7,4 | 20,6 |
- Имеются опубликованные данные и нормы для некоторых состояний здоровья, а также для населения в целом (Канада и США).
- Более высокие баллы указывают на более высокий уровень здоровья.
- Необходимы дальнейшие исследования по использованию SF-36 для людей с ТСМ, чтобы понять, как они отвечают на вопросы, чтобы гарантировать достоверность данных.
- В настоящее время нормативные данные для населения с ТСМ не сообщались
- Опубликованные данные о популяции пациентов с ТСМ доступны для сравнения (см. раздел «Интерпретируемость» на странице сведений об исследовании).
Надежность
- Внутренняя согласованность варьируется от умеренной до высокой для общего SF-36 (коэффициент Кронбаха = 0,82) и подшкал:
- Физическое функционирование (а Кронбаха = 0,91-0,98)
- Физическая роль (коэффициент Кронбаха а = 0,94)
- Телесная боль (а Кронбаха = 0,79)
- Общее состояние здоровья (коэффициент Кронбаха а = 0,79-0,82)
- Живучесть (коэффициент Кронбаха а = 0,76)
- Социальное функционирование (а Кронбаха = 0,72)
- Роль Эмоциональная (коэффициент Кронбаха а = 0,89)
- Психическое здоровье (а Кронбаха = 0,78)
- Межэкспертная и внутриэкспертная надежность варьируется от умеренной до высокой для подшкал SF-36: (межэкспертная ICC, внутриэкспертная ICC)
- Физическое функционирование (0,67, 0,71)
- Физическая роль (0,90, 0,89)
- Телесная боль (0.
 70, 0.87)
70, 0.87) - Общее состояние здоровья (0,41, 0,87)
- Живучесть (0,86, 0,93)
- Социальное функционирование (0,52, 0,93)
- Роль Эмоциональная (0,98, 0,99)
- Психическое здоровье (0,57, 0,77)
(Forchheimer et al. 2004, King & Roberts 2002, Lin 2007, Luther et al. 2006, Van Leeuwen et al. 2012)
Срок действия
- Корреляция умственной сводки SF-36 высока с пунктами Системы наблюдения за поведенческими факторами риска (Pearson r = от -0,650 до -0,761), низкая с качеством благополучия (Pearson r=0,116) и низкая с инструментальной деятельностью Повседневная жизнь (г Пирсона = 0,262).
- Корреляция физической сводки SF-36 умеренная с элементами системы наблюдения за поведенческими факторами риска (r = от -0,458 до -0,489 Пирсона), качеством благополучия (r = 0,417 Пирсона) и инструментальной деятельностью в повседневной жизни (r Пирсона). =-0,357)
- Способность SF-36 различать подгруппы по возрасту, образованию, семейному положению, занятости, времени, прошедшему после травмы, степени травмы и способности к самообслуживанию была проверена с использованием U-критерия Манна-Уитни.
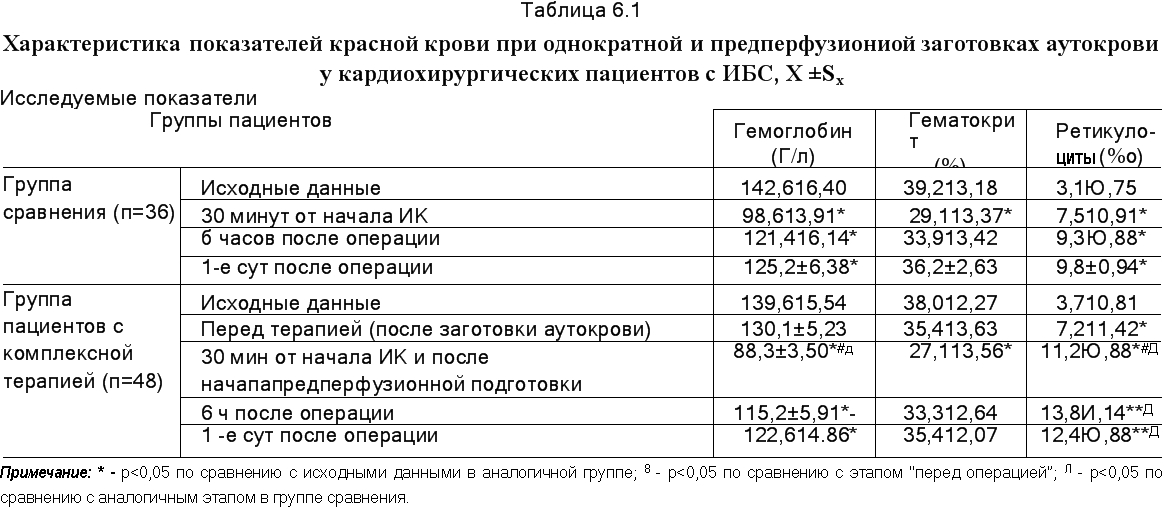
- Домены SF-36 имели значительную дискриминационную валидность между занятостью и способностью заботиться о себе; дискриминантная способность отличалась от других характеристик. В целом домены SF-36 значительно различались между подгруппами по 2-4 характеристикам.
(Forchheimer et al. 2004, King & Roberts 2002, Lin 2007, Luther et al. 2006, Van Leeuwen et al. 2012, Andresen et al. 1999, Bonne-Lee et al. 2008, Miller et al. 2008, Raichle et al., 2006, Anton et al., 2006, Horner-Johnson et al., 2010)
Оперативность
- Значительно более низкие баллы для лиц с травмой спинного мозга, чем в группе без инвалидности, были зарегистрированы в отношении физического функционирования, телесной боли и ролевой физической домены.
- Тем не менее, все элементы подшкалы жизнеспособности показали значительное положительное дифференциальное функционирование для людей с ТСМ при контроле общих показателей физического здоровья.
(Lin 2007, Bonne-Lee et al./17.jpg) 2008, Horner-Johnson et al. 2010)
2008, Horner-Johnson et al. 2010)
Эффект пола/потолка
- Эффекты пола и потолка, указанные для SF-36.
- 3 субшкалы (ролевое физическое, социальное функционирование, ролевая эмоция) продемонстрировали максимальный эффект от 22,5 до 75,3%.
- 2 субшкалы (физическое функционирование и ролевое физическое) показали эффекты пола 24,2% и 36,3% соответственно.
(King & Roberts 2002, Van Leeuwen et al. 2012, Andresen et al. 1999, Lin 2007, Bonne-Lee et al. 2008)
Рецензент
Доктор Бен Мортенсон, Броди Сакакибара, Джон Чжу, Джереми Мак, Риса Фокс
Дата , Браунсон, Калифорния. Эффективность инструментов оценки качества жизни, связанных со здоровьем, у пациентов с травмами спинного мозга. Arch Phys Med Rehabil, 1999; 80: 877-84.
http://www.ncbi.nlm.nih.gov/pubmed/10453762
Антон Х.А., Миллер В.К., Таунсон А.Ф. Измерение усталости у лиц с травмой спинного мозга. Arch Phys Med Rehabil 2008; 89: 538-542.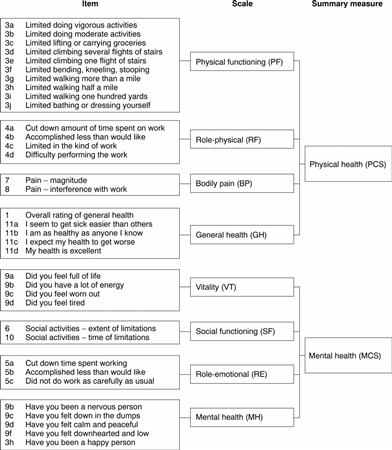
http://www.ncbi.nlm.nih.gov/pubmed/18295634
Ataoğlu E, Tiftik T, Kara M, Tunç H, Ersöz M, Akkuş S. Влияние хронической боли на качество жизни и депрессию у пациентов с травмой спинного мозга. Спинной мозг. 2013;51(1):23-6.
http://www.ncbi.nlm.nih.gov/pubmed/22547044
Bonne-Lee B, King MT, Simpson JM, Haran MJ, Stockler MR, Marial O, Salkeld G. Валидность, оперативность и минимальная важность разница по шкале полезности для здоровья SF-6D в популяции пациентов с травмами спинного мозга. Значение для здоровья, 2008 г.; 11(4): 680-688.
http://www.ncbi.nlm.nih.gov/pubmed/18194406
Forchheimer M, McAweene M, Tate DG. Применение SF-36 среди лиц с травмой спинного мозга. Am J Phys Med Rehabil, 2004; 83: 390-395.
http://www.ncbi.nlm.nih.gov/pubmed/15100631
Голхасани-кештан Ф., Эбрахимзаде М.Х., Фаттахи А.С., Солтани-могхаддас С.Х., Омиди-кашани Ф. Валидация и кросс-культурная адаптация персидского версия короткой формы метода оценки и отчетности Крейга по гандикапу (CHART). Реабилитация инвалида. 2013;35(22):1909-14.
Реабилитация инвалида. 2013;35(22):1909-14.
http://www.ncbi.nlm.nih.gov/pubmed/23480647
Horner-Johnson W, Krahn GL, Suzuki R, Peterson JJ, Roid G, Hall T, Группа экспертов RRTC по измерению состояния здоровья. Дифференциальная эффективность предметов SF-36 у здоровых взрослых с функциональными ограничениями и без них. Arch Phys Med Rehabil 2010; 91: 570-5.
http://www.ncbi.nlm.nih.gov/pubmed/20382289
Кинг Дж.Т. и Робертс М.С. Валидность и надежность краткой формы-36 при шейной спондилотической миелопатии. Дж. Нейросург (позвоночник 2), 2002 г.; 97:180-185.
http://www.ncbi.nlm.nih.gov/pubmed/12296676
Lee BB, Simpson JM, King MT, Haran MJ, Marial O. Шаговое колесо SF-36: простая модификация SF- 36 физической области улучшает его способность реагировать на изменение состояния здоровья при повреждении спинного мозга. Спинной мозг. 2009;47(1):50-5.
http://www.ncbi.nlm.nih.gov/pubmed/18560375
Lin M-R, Hwang H-F, Chen C-Y, Chiu W-T. Сравнение краткой формы Всемирной организации здравоохранения «Качество жизни» и краткой формы-36 для лиц с травмами спинного мозга. Am J Phys Med Rehabil 2007; 86: 104–113.
Am J Phys Med Rehabil 2007; 86: 104–113.
http://www.ncbi.nlm.nih.gov/pubmed/17075363
Лютер С.Л., Кромри Дж., Пауэлл-Коуп Г., Розенберг Д., Нельсон А., Ахмед С., Куигли П. Пилотное исследование по модификации СФ Шкала физического функционирования -36 В для использования с ветеранами с травмой спинного мозга. Arch Phys Med Rehabil 2006; 87: 1059-1066.
http://www.ncbi.nlm.nih.gov/pubmed/16876550
McHorney C, Ware JJ, Lu R, CD S. Краткий обзор состояния здоровья MOS из 36 пунктов (SF-36): III. Тесты качества данных, предположений о масштабировании и надежности для различных групп пациентов. Мед уход 1994;32:40-66.
http://www.ncbi.nlm.nih.gov/pubmed/8277801
Миллер В.К., Антон Х.А., Таунсон А.Ф. Измерительные свойства шкалы CESD у лиц с травмой спинного мозга. Спинной мозг 2008; 46: 287-292.
http://www.ncbi.nlm.nih.gov/pubmed/17909558
Райхл К.А., Осборн Т.Л., Дженсен М.П., Карденас Д. Надежность и достоверность мер вмешательства при боли у людей с травмой спинного мозга. Журнал Боли, 2006; 7(3): 179-186.
Журнал Боли, 2006; 7(3): 179-186.
http://www.ncbi.nlm.nih.gov/pubmed/16516823
Silveira E, Taft C, Sundh V, Waern M, Palsson S, Steen B. Результаты исследования состояния здоровья SF-36 при скрининге депрессивных и тревожных расстройств у пожилых женщин Швеции. Качество жизни Res. 2005;14(5):1263-74.
http://www.ncbi.nlm.nih.gov/pubmed/16047502
Tramonti F, Gerini A, Stampacchia G. Индивидуальное и связанное со здоровьем качество жизни людей с травмой спинного мозга. Спинной мозг. 2014;52(3):231-5.
http://www.ncbi.nlm.nih.gov/pubmed/24343055
Уналан Х., Мисирлиоглу Т.О., Эрхан Б., Акюз М., Гундуз Б., Ирги Э., Арслан Х.Е., Балтаджи А., Аслан С., Паламар Д., Кутлу А., Майлеси Дж., Акарырмак У., Карамехметоглу С.С. Исследование валидности и надежности турецкой версии Измерения независимости спинного мозга-III. Спинной мозг. 2015;53(6):455-60.
http://www.ncbi.nlm.nih.gov/pubmed/25665539
van Leeuwen CMC, van der Woude LHV, Post MWM. Валидность подшкалы психического здоровья SF-36 у лиц с травмой спинного мозга.



 att.net
att.net 

 Медицинское обслуживание 1994;32:40-66.
Медицинское обслуживание 1994;32:40-66.  Б. Качество жизни при астме. Я.
Внутренняя согласованность и достоверность вопросника SF-36. Ам Дж
Respir Crit Care Med 1994;149:371-5.
Б. Качество жизни при астме. Я.
Внутренняя согласованность и достоверность вопросника SF-36. Ам Дж
Respir Crit Care Med 1994;149:371-5.